Основы биохимии - А. А. Анисимов 1986
Общая биохимическая характеристика живых организмов
Источники энергии для живых организмов, высокоэнергетические соединения
1.3.1. Источники энергии и углерода для живых организмов. Все живые организмы можно разделить на две большие группы в зависимости от того, в какой химической форме они получают углерод из окружающей среды. Автотрофы (от греч. авто — само, трофе — пища) — самостоятельно питающиеся — могут использовать в качестве единственного источника углерода оксид углерода (IV) С02, из которого они способны образовывать все свои углеродсодержащие соединения. К автотрофам относятся растения, фотосинтезирующие и хемосинтезирующие бактерии. Процесс хемосинтеза, т. е. ассимиляции СО2 за счет энергии, выделяемой при окислении неорганических соединений, впервые открыт в конце прошлого столетия С. Н. Виноградским.
Гетеротрофы (от греч. гетерос — другой, трофе — пища) должны получать углерод в виде готовых достаточно сложных органических соединений (например, углеводов). Сюда относятся животные и большинство микроорганизмов. Все гетеротрофные организмы способны ассимилировать небольшие количества СO2. Однако при этом он связывается путем карбоксилирования уже присутствующих в клетке карбоновых кетокислот, т. е. гетеротрофный организм нуждается в готовых органических соединениях.
Живые организмы можно также классифицировать по источникам получения энергии. Для большой группы фототрофов непосредственным энергетическим ресурсом является свет. Они используют энергию солнечного света для образования высокоэнергетических соединений, которые служат своеобразными аккумуляторами энергии. Сюда относятся высшие растения, водоросли, фотосинтезирующие бактерии.
Хемотрофы в качестве источника энергии используют окислительно-восстановительные реакции. Хемотрофами являются животные, большая часть микроорганизмов. Этот способ получения энергии свойствен и нефотосинтезирующим клеткам растений. Как фототрофы, так и хемотрофы можно, в свою очередь, разделить на группы в зависимости от того, какие вещества являются донорами электронов в окислительно-восстановительных процессах. У литотрофов таковыми служат неорганические соединения, у органотрофов — органические. Таким образом, в зависимости от используемых источников энергии и доноров электронов можно выделить четыре основных типа организмов (табл. 1.2).
Хемотрофные организмы группируют и по виду акцепторов электронов. В тех случаях, когда для окисления используется кислород, имеет место аэробный, или дыхательный, тип энергетики. При анаэробном типе энергетического обмена в роли окислителя выступает не кислород, а ряд других веществ, т. е. другие акцепторы электронов.
Многие организмы могут существовать как в аэробных, так и в анаэробных условиях. В аэробных условиях они используют в качестве акцептора электронов кислород, т. е. осуществляют процесс дыхания. В анаэробных условиях акцепторами электронов у них служат органические вещества, происходит брожение. Такие организмы называют факультативными анаэробами. К ним относится большинство органотрофных клеток (дрожжи, клетки высших организмов). При наличии в среде кислорода они предпочитают использовать его. Анаэробы, не способные использовать кислород, называются облигатными анаэробами, кислород для них ядовит. Поскольку весь свободный кислород, содержащийся в атмосфере Земли, образовался в результате процесса фотосинтеза, очевидно, что анаэробный тип энергетики является более древним, чем аэробный. Таким образом, брожение — процесс более древний, чем дыхание.
Таблица 1.2. Классификация организмов в зависимости от используемых источников энергии и доноров электронов
Типы организмов |
Источник энергии |
Доноры электронов |
Конечные акдепторы электронов |
Примеры организмов |
Фотолитотрофы |
Свет |
Неорганические соединения (Н2О, H2S, S) |
Зеленые клетки высших растений, синезеленые водоросли, цианобактерии, большинство пурпурных и зеленых серобактерий |
|
Фотоорганотрофы |
Свет |
Органические соединения |
— |
Несерные пурпурные бактерии, галобактерии |
Хемолитотрофы |
Окислительно-восстановительные реакции |
Неорганические соединения (H2S, H2, S, Fe2+, NH3) |
О2, СО2, SO2-4 |
Тионовые, сульфатвосстанавливающие, водородные, железные, метанобразующие и денитрифицирующие бактерии |
Хемоорганотрофы |
Окислительно-восстановительные реакции |
Органические соединения (например, глюкоза) |
О2 и органические соединения |
Все высшие животные, большая часть бактерий, грибы, нефотосинтезирующие клетки растений |
1.3.2. Высокоэнергетические соединения. Высокоэнергетическими соединениями являются АТФ и вещества, способные образовывать АТФ в ферментативных реакциях переноса групп без участия окислительных процессов. Такие соединения содержат в своей молекуле связи, при гидролизе которых высвобождается большое количество свободной энергии. Реакции протекают при различных условиях, оказывающих влияние на величину изменения свободной энергии. Поэтому в биохимии используют термин изменение стандартной свободной энергии — ∆G°. Под ним понимают изменение свободной энергии при стандартных условиях: давление 1 атм1, исходные концентрации субстратов — 1 М, температура 25°С. ∆G° при pH 7,0 обозначают ∆G°'. Величину ∆G° применяют для количественной характеристики как метаболических цепей, так и отдельных химических реакций; как и в термодинамике, знаком «минус» обозначается отдача энергии, а знаком «плюс» — ее принятие. Если величина ∆G° данной реакции имеет отрицательное значение, то реакция может происходить самопроизвольно с выделением свободной энергии — экзергоническая реакция. Если ∆G° — положительная величина, то реакция протекает с поглощением энергии (эндергоническая реакция). Среди реакций обмена веществ известны полностью эндергонические. Они зависят от притока свободной энергии извне (например, световой) или от других экзергонических реакций обмена веществ (например, окисления). В качестве посредника между процессами, связанными с генерированием и использованием энергии, функционирует система высокоэнергетических соединений. Величина стандартной свободной энергии гидролиза высокоэнергетических связей превышает —21 кДж⋅моль-1 (табл. 1.3), такие связи обозначают знаком ∽.
1 По международной системе единиц СИ давление измеряется в паскалях:
1 атм = 101,3 кПА. В биологии общепринято измерение давления в атмосферах.
Таблица 1.3. Стандартная свободная энергия гидролиза некоторых соединений (в кДж⋅моль-1)
Соединение |
Продукты |
∆G° (pH 7,0) |
Фосфоенолпируват3- |
Пируват- + НРО2-4 |
—61,9 |
1,3-Дифосфоглицерат4- |
3-Фосфоглицерат3- + НРО2-4 + Н+ |
—54,5 |
Креатинфосфат- |
Креатин+ + НРО2-4 |
—43,1 |
Ацетил фосфат2- |
Ацетат- + НРО2-4 + Н+ |
—47,7 |
Фосфоаргинин- |
Аргинин++ НРО2-4 |
—38,1 |
АТФ4- |
АДФ3- + НРО2-4 + Н+ |
—34,5 |
Глюкозо-1-фосфат2- |
Глюкоза + НРО2-4 |
—20,9 |
a-D-Глюкозо-6-фосфат2- |
а-D-Глюкоза + НРО2-4 |
—13,8 |
Глицерофосфат2- |
Глицерин + HPO2-4 |
—9,2 |
Высокоэнергетические соединения имеют, как правило, в своем составе высокоэнергетическую фосфатную группу и могут передавать ее другим веществам. Многочисленные эксперименты показали, что переносится не фосфатная группа 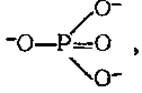 а фосфорильная
а фосфорильная 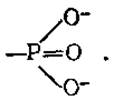 Хотя выражение «перенос фосфатных групп» общепринято, правильнее говорить о переносе фосфорильных групп. Высокоэнергетические фосфорильные группы обозначают ∽ Ф или ∽ Р.
Хотя выражение «перенос фосфатных групп» общепринято, правильнее говорить о переносе фосфорильных групп. Высокоэнергетические фосфорильные группы обозначают ∽ Ф или ∽ Р.
Различают пять основных типов высокоэнергетических соединений: рибонуклеозид-5'-дифосфаты и трифосфаты (АТФ, ГТФ, УТФ, ЦТФ, АДФ и др.), карбоксилфосфаты (например, ацетил-фосфат), ацилтиоловые эфиры (например, ацетилкоэнзим А), фосфорамидные соединения (креатинфосфат), енолфосфаты (фосфоенолпировиноградная кислота).
В центре энергетического обмена клетки стоит аденилатная система: АТФ и продукты ее гидролиза — АДФ, АМФ, ФH ФФH. Она подобна аккумулятору, который заряжается энергией от разных генераторов и снабжает ею множество машин и аппаратов (в живом организме им соответствуют органы, ткани, биохимические реакции). В этом плане «зарядка аккумулятора» состоит в синтезе АТФ:
![]()
а «разрядка аккумулятора» сопровождается гидролизом АТФ:
![]()
где E1и Е2 — ферменты, катализирующие соответствующие реакции.
В ходе гидролиза АТФ фосфорильная группа 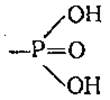 переносится на гидроксид-ион, при этом стандартная свободная энергия гидролиза при pH 7,0 составляет —34,5 кДж⋅моль-1. Для гидролиза концевой фосфорильной группы АДФ характерна близкая величина. Отщепление фосфорильной группы от АМФ характеризуется более низкой величиной —9,6 кДж⋅моль-1. Следовательно, высокоэнергетическими в молекуле АТФ являются лишь две последние фосфоангидридные связи. Однако следует учитывать, что в конкретных реакциях величина выделившейся энергии зависит от температуры, pH, концентраций субстратов и ионов магния.
переносится на гидроксид-ион, при этом стандартная свободная энергия гидролиза при pH 7,0 составляет —34,5 кДж⋅моль-1. Для гидролиза концевой фосфорильной группы АДФ характерна близкая величина. Отщепление фосфорильной группы от АМФ характеризуется более низкой величиной —9,6 кДж⋅моль-1. Следовательно, высокоэнергетическими в молекуле АТФ являются лишь две последние фосфоангидридные связи. Однако следует учитывать, что в конкретных реакциях величина выделившейся энергии зависит от температуры, pH, концентраций субстратов и ионов магния.
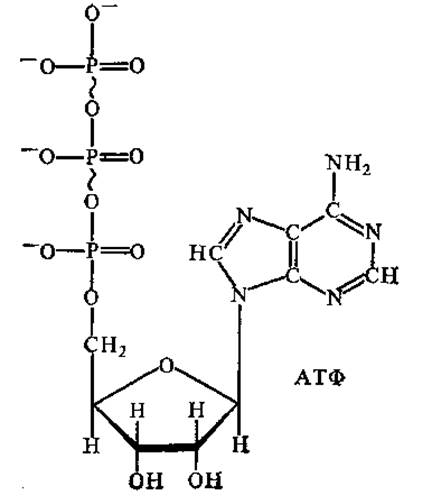
Основная часть адениловых нуклеотидов присутствует в клетке в виде комплексов с магнием MgATФ2- и МдАДФ-. Именно в этой форме они участвуют в большинстве ферментативных реакций, где играют роль доноров фосфорильных групп и энергии. Некоторое количество АТФ и АДФ присутствует в клетке в виде свободных анионов. При этом АТФ содержит четыре ОН-группы, способные к ионизации, т. е. имеет максимальный заряд АТФ4-, а АДФ — три ОН-группы, заряд — АДФ3-.
В молекуле АТФ заряды располагаются близко друг к другу, между ними возникает сильное отталкивание. Оно уменьшается при отщеплении концевой фосфорильной группы. Продукты реакции — НРО42- и АДФ3- не могут вновь воссоединиться, так как их сближению препятствует отталкивание одноименных зарядов. Это и обусловливает большую отрицательную величину стандартной свободной энергии гидролиза АТФ.
Следует также иметь в виду, что в концевой фосфоангидридной связи молекулы АТФ атомы фосфора и кислорода окружает большое число электронов. Они конкурируют друг с другом за энергетически наиболее выгодные орбитали. Конкуренция не позволяет всем электронам занять низкие энергетические уровни. В продуктах гидролиза АТФ—АДФ3- и НРО42- электроны занимают низкие энергетические уровни, что стабилизирует продукты, придает всей реакции необратимость. Этот фактор также обусловливает большую отрицательную величину ∆G° гидролиза АТФ.
АТФ по величине свободной энергии гидролиза занимает промежуточное положение между высокоэнергетическими и низкоэнергетическими фосфатсодержащими соединениями. В этом состоит уникальность АТФ, она служит посредником-переносчиком фосфорильных групп и энергии от высокоэнергетических соединений (в табл. 1.3 расположены выше АТФ) к низкоэнергетическим при синтезе последних (в табл. 1.3 расположены ниже АТФ).
В клетке никогда не происходит прямого переноса фосфорильных групп от высокоэнергетических соединений к низкоэнергетическим, практически все реакции переноса фосфорильных групп в клетке происходят с участием системы АТФ—АДФ в качестве посредника-переносчика. Другие нуклеозид-5'-трифосфаты (УТ Ф, ГТФ, ЦТФ) тоже являются высокоэнергетическими соединениями, но не играют в клетке такой универсальной роли, как АТФ, выполняют как доноры энергии узкоспециализированные функции: УТФ служит поставщиком фосфорила и энергии при синтезе полисахаридов, ЦТФ — при синтезе липидов, ГТФ избирательно ускоряет образование пептидной связи при биосинтезе белков.
Перенос фосфорильных групп и энергии с АТФ на другие соединения осуществляют ферменты, имеющие тривиальное, краткое рабочее название — киназы (например, гексокиназа, пируваткиназа; от греч. кинео — двигаю, перемещаю). Следовательно, киназа означает активатор, так как образование фосфорного эфира любого соединения приводит к активации этого соединения, увеличению его реакционной способности.
Все живые организмы улавливают энергию внешних энергетических ресурсов с помощью систем аккумуляции энергии и преобразуют ее в энергию высокоэнергетических соединений. Системы аккумуляций энергии делятся на два типа, отличающиеся принципами энергетического сопряжения. Первый тип — реакции фосфорилирования, не требующие нерастворимых мембранных структур, — субстратное (или немембранное) фосфорилирование. Образование АТФ при этом происходит путем переноса активного фосфорила с продукта окисления субстрата на АДФ. Например, образование АТФ при гликолизе, брожении. Второй тип — реакции фосфорилирования, протекающие в сопрягающих мембранах, — мембранное фосфорилирование. Образование АТФ происходит путем фосфорилирования АДФ неорганическим фосфатом за счет энергии электрохимического потенциала ионов водорода на мембране. Например, образование АТФ при фотосинтезе, или в аэробной фазе дыхания. Мембранное фосфорилирование протекает во внутренней мембране митохондрий, в мембранах тилакоидов хлоропластов, в хроматофорах фотосинтезирующих бактерий, в цитоплазматической мембране бактерий. Эти мембраны, несущие ферменты переноса электронов и сопряженного с ним фосфорилирования, называются сопрягающими мембранами.