Биологическая химия - Березов Т. Т., Коровкин Б. Ф. 1998
Гормоны
Простагландины
Термин «простагландины» был введен У. Эйлером, впервые показавшим, что в сперме человека и экстрактах из семенных пузырьков барана содержатся вещества, оказывающие выраженное вазопрессорное действие и вызывающие сокращение гладкой мускулатуры матки. Предположение У. Эйлера, что эти вещества являются специфическим секретом предстательной железы (prostata), не подтвердилось, поскольку, как теперь установлено, они содержатся во всех органах и тканях*. Тем не менее этот термин в литературе сохранился (синонимы: простатогландины, простагландины).
* Исключение составляет только вилочковая железа, на которую андрогены оказывают катаболическое действие.
В последнее десятилетие простагландины и родственные им биологически активные соединения (лейкотриены, простациклины, тромбоксаны) были предметом пристального внимания исследователей. Объясняется это тем, что, помимо широкого распространения в тканях, они оказывают сильное фармакологическое действие на множество физиологических функций организма, регулируя гемодинамику почек, сократительную функцию гладкой мускулатуры, секреторную функцию желудка, жировой, водносолевой обмен и др. Имеются данные о том, что простагландины, вероятно, не являются «истинными» гормонами, хотя некоторые авторы считают их «локальными, местными гормонами», однако было показано, что они модулируют действие гормонов. Биологические эффекты простагландинов, по-видимому, опосредованы через циклические нуклеотиды (см. далее).
В последнее время были подтверждены представления С. Бергстрёма и сотр., что предшественником всех простагландинов являются полиненасыщенные жирные кислоты, в частности арахидоновая кислота (и ряд ее производных, дигомо-у-линоленовая и пентаноевая кислоты, в свою очередь образующиеся в организме из линолевой и линоленовой кислот) (см. главу 11). Арахидоновая кислота после освобождения из фосфоглицеринов (фосфолипидов) биомембран под действием специфических фосфолипаз А (или С) в зависимости от ферментативного пути превращения дает начало простагландинам и лейкотриенам по схеме:
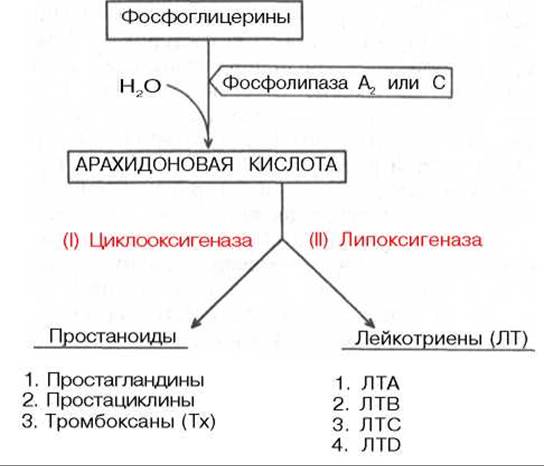
Первый путь получил наименование циклооксигеназного пути превращения арахидоновой кислоты, поскольку первые стадии синтеза простагландинов катализируются циклооксигеназой, точнее простагландин-синтазой (КФ 1.14.99.1). В настоящее время известны данные о биосинтезе основных простаноидов (рис. 8.3). Центральным химическим процессом биосинтеза является включение молекулярного кислорода (двух молекул) в структуру арахидоновой кислоты, осуществляемое специфическими оксигеназами, которые, помимо окисления, катализируют циклизацию с образованием промежуточных продуктов — простагландинэндоперекисей PG2[H2], обозначаемых PGG2 и PGH2; последние под действием простагландин-изомераз превращаются в первичные простагландины. Различают 2 класса первичных простагландинов: растворимые в эфире простагландины PGE и растворимые в фосфатном буфере простагландины PGF. Каждый из классов делится на подклассы: PGE1; PGE2; PGF1; PGF2 и т.д. Простациклины и тромбоксаны синтезируются из указанных промежуточных продуктов при участии отличных от изомераз ферментов. Детали механизма биосинтеза простаноидов пока до конца не выяснены, как и пути их окисления до конечных продуктов обмена.
* Простагландины и ферментные системы, катализирующие их биосинтез, не обнаружены только в эритроцитах человека. Следует, однако, отметить, что наибольшее количество простагландинов содержат органы и ткани, относящиеся к репродуктивной системе.
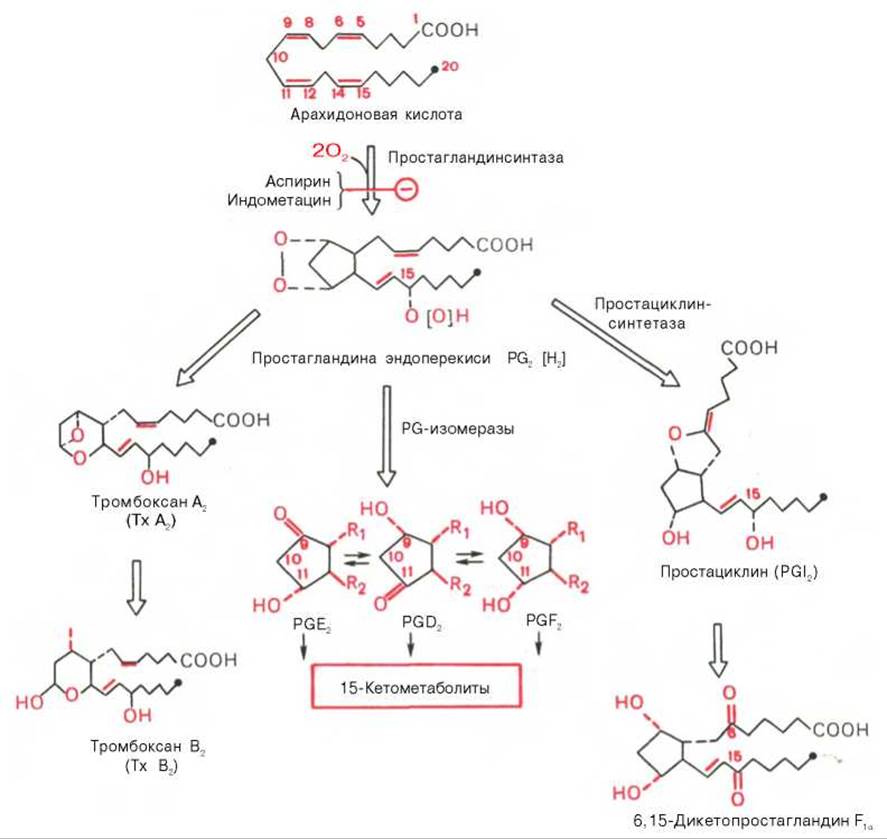
Рис. 8.3. Циклооксигеназный путь превращения арахидоновой кислоты.
R1 и R2 — боковые цепи, идентичные для всех трех простагландинов. Знаком ![]() обозначено блокирующее действие указанных веществ.
обозначено блокирующее действие указанных веществ.
Первичные простагландины синтезируются во всех клетках (за исключением эритроцитов), действуют на гладкие мышцы пищеварительного тракта, репродуктивные и респираторные ткани, на тонус сосудов, модулируют активность других гормонов, автономно регулируют нервное возбуждение, процессы воспаления (медиаторы), скорость почечного кровотока; биологическое действие их опосредовано путем регуляции синтеза цАМФ (см. далее).
Тромбоксан А, в частности тромбоксан А2 (ТхА2), синтезируется преимущественно в ткани мозга, селезенки, легких, почек, а также в тромбоцитах и воспалительной гранулеме из PGH2 под действием тромбоксансинтазы (см. рис. 8.3); из ТхА2 образуются остальные тромбоксаны. Они вызывают агрегацию тромбоцитов, способствуя тем самым тромбообразованию, и, кроме того, оказывают самое мощное сосудосуживающее действие из всех простагландинов.
Простациклин (PGI2) синтезируется преимущественно в эндотелии сосудов, сердечной мышце, ткани матки и слизистой оболочке желудка. Он расслабляет в противоположность тромбоксану гладкие мышечные волокна сосудов и вызывает дезагрегацию тромбоцитов, способствуя фибринолизу.
Следует указать также на особое значение соотношения в крови тромбоксаны/простациклины, в частности TxA2/PGI2 для физиологического статуса организма. Оказалось, что у больных, предрасположенных к тромбозам, имеется тенденция к смещению баланса в сторону агрегации; у больных, страдающих уремией, напротив, наблюдается дезагрегация тромбоцитов. Выдвинуто предположение о важности баланса TxA2/PGI2 для регуляции функции тромбоцитов in vivo, сердечно-сосудистого гомеостаза, тромботической болезни и т.д.
На рис. 8.3 представлены также пути катаболизма простаноидов. Начальной стадией катаболизма «классических» простагландинов является стереоспецифическое окисление ОН-группы у 15-го углеродного атома с образованием соответствующего 15-кетопроизводного. Фермент, катализирующий эту реакцию, — 15-оксипростагландиндегидрогеназа открыт в цитоплазме, требует наличия НАД или НАДФ. Тромбоксан инактивируется in vivo или путем химического расщепления до тромбоксана В2, или путем окисления дегидрогеназой либо редуктазой. Аналогично PGI2 (простациклин) быстро распадается до 6-кето-PGF1а in vitro, a in vivo инактивируется окислением 15-оксипростагландиндегидрогеназой с образованием 6,15-дикето-PGF1а.
Второй путь превращения арахидоновой кислоты — липоксигеназный путь (рис. 8.4) — отличается тем, что дает начало синтезу еще одного класса биологически активных веществ — лейкотриенов. Характерная особенность структуры лейкотриенов заключается в том, что она не содержит циклической структуры, хотя лейкотриены, как и простаноиды, построены из 20 углеродных атомов. В структуре лейкотриенов содержатся четыре двойные связи, некоторые из них образуют пептидолипидные комплексы с глутатионом или с его составными частями (лейкотриен D может далее превращаться в лейкотриен Е, теряя остаток глицина). Основные биологические эффекты лейкотриенов связаны с воспалительными процессами, аллергическими и иммунными реакциями, анафилаксией и деятельностью гладких мышц. В частности, лейкотриены способствуют сокращению гладкой мускулатуры дыхательных путей, пищеварительного тракта, регулируют тонус сосудов (оказывают сосудосуживающее действие) и стимулируют сокращение коронарных артерий. Катаболические пути лейкотриенов окончательно не установлены.
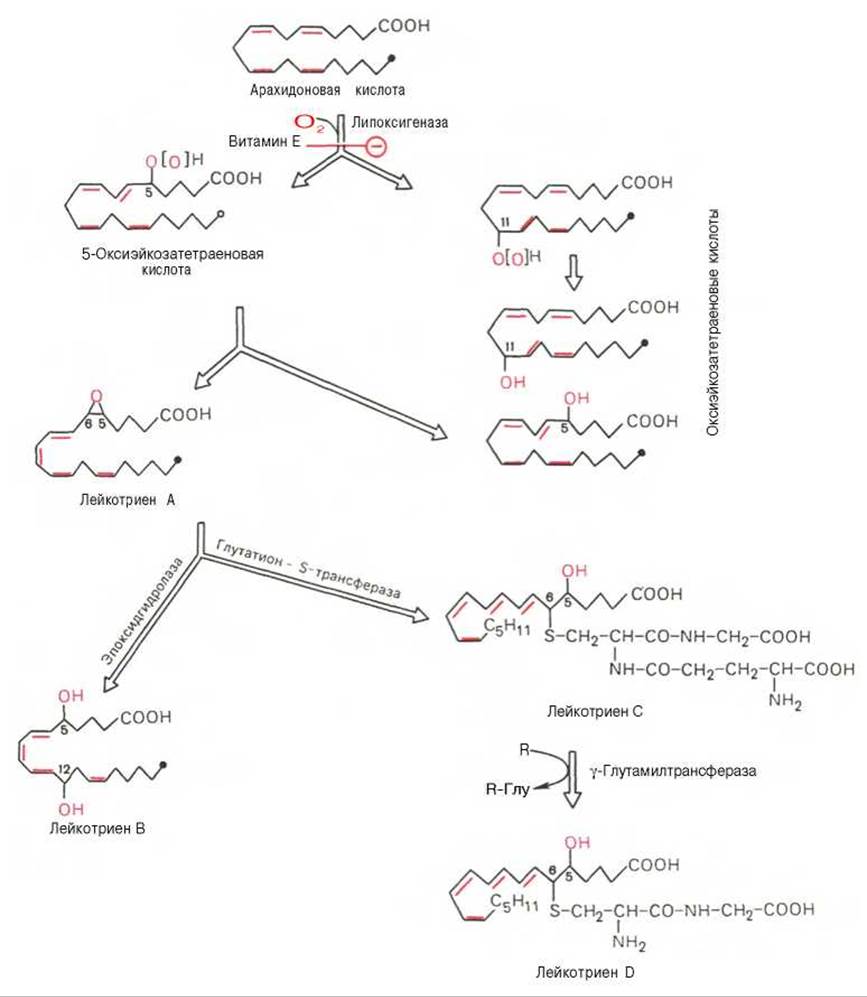
Рис. 8.4. Липоксигеназный путь превращения арахидоновой кислоты.
R - акцептор остатка глутаминовой кислоты. Знаком обозначено блокирующее действие витамина Е.
Таким образом, благодаря своему широкому распространению в тканях и высокой и разносторонней биологической активности простагландины (и вообще простаноиды) и лейкотриены находят все более широкое применение в медицинской практике в качестве лекарственных препаратов. Эти обстоятельства стимулируют проведение дальнейших исследований как по пути поиска новых простаноидов, так и по пути химического синтеза их аналогов с защищенными функциональными группами, более стабильными при введении в организм.