Биологическая химия - Березов Т. Т., Коровкин Б. Ф. 1998
Химия белков
Структурная организация белков
Методы определения N-концевой аминокислоты
Для определения природы N-концевой аминокислоты предложен ряд методов, в частности метод Сэнджера (F. Sanger), основанный на реакции арилирования полипептида 2,4-динитрофторбензолом (ДНФБ), что приводит к образованию окрашенного в желтый цвет 2,4-динитрофенильного производного N-концевой аминокислоты*. Раствор полипептида обрабатывают ДНФБ, который взаимодействует со свободной NH-группой N-концевой аминокислоты пептида.
* За разработку этого метода Ф. Сэнджер удостоен Нобелевской премии (1958). В 1980 г. он был удостоен второй раз Нобелевской премии вместе с У. Гилбертом и П. Бергом за разработку метода определения первичной структуры нуклеиновых кислот.
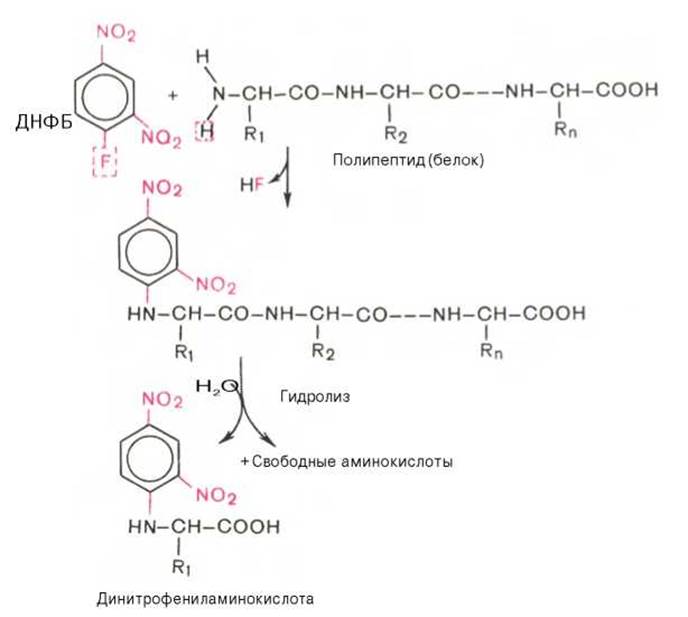
После кислотного гидролиза продукта реакции - динитрофенилпептида только одна N-концевая аминокислота оказывается связанной с реактивом в виде 2,4-динитрофениламинокислоты (стабильной при гидролизе). В отличие от других образовавшихся при гидролизе полипептида свободных аминокислот она желтого цвета. Ее идентифицируют методом хроматографии.
Для определения N-концевой аминокислоты значительно более широко применяется фенилтиогидантоиновый метод Эдмана благодаря своей высокой чувствительности и возможности многократного использования в одной и той же пробе. Фенилизотиоцианат реагирует со свободной а-NH2-группой N-концевой аминокислоты полипептида с образованием фенилтиокарбамоилпептида.

Обработка продукта реакции кислотой приводит к циклизации и освобождению фенилтиогидантоина N-концевой аминокислоты, природу которого устанавливают хроматографически. Укороченный на одну аминокислоту полипептид подвергают дальнейшему анализу.
Эту процедуру ступенчатого расщепления пептида с N-конца можно повторять многократно, идентифицируя последовательно одну аминокислоту за другой. Метод Эдмана используется в качестве химической основы для определения первичной структуры белков и пептидов. Он реализован в специальном приборе — секвенаторе (от англ. sequence — последовательность), работающем в автоматическом режиме и позволяющем определить последовательность аминокислот с N-конца пептида до 50—60 аминокислотных остатков.
Кроме этих реактивов, для определения чередования аминокислот используют цианат калия, 1-диметиламинонафтил-5-сульфонилхлорид - дансилхлорид и дабсилхлорид. Для этих же целей иногда применяют ферменты экзопептидазы, в частности аланин- и лейцинаминопептидазу. Эти ферменты разрывают пептидные связи с того конца полипептида, где имеется свободная NН2-группа, освобождая N-концевую аминокислоту (механизм действия экзопептидаз см. в главе 12).