БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ - Е. С. Северина - 2004
РАЗДЕЛ 11. ГОРМОНАЛЬНАЯ РЕГУЛЯЦИЯ ОБМЕНА ВЕЩЕСТВ И ФУНКЦИЙ ОРГАНИЗМА
IV. Регуляция обмена основных энергоносителей
Основные пищевые вещества (углеводы, жиры, белки) окисляются в организме с освобождением свободной энергии, которая используется в анаболических процессах и при осуществлении физиологических функций. Энергетическая ценность основных пищевых веществ выражается в килокалориях и составляет: для углеводов — 4 ккал/г, для жиров — 9 ккал/г, для белков — 4 ккал/г. Взрослому здоровому человеку в сутки требуется 2000 — 3000 ккал (8000 — 12 000 кДж) энергии.
При обычном ритме питания промежутки между приёмами пищи составляют 4 — 5 ч с 8 — 12-часовым ночным перерывом. Во время пищеварения и абсорбтивного периода (2— 4 ч) основные энергоносители, используемые тканями (глюкоза, жирные кислоты, аминокислоты), могут поступать непосредственно из пищеварительного тракта. В постабсорбтивном периоде и при голодании энергетические субстраты образуются в процессе катаболизма депонированных энергоносителей.
Изменения в потреблении энергоносителей и энергетических затратах координируются путём чёткой регуляции метаболических процессов в разных органах и системах организма, обеспечивающей энергетический гомеостаз.
Основную роль в поддержании энергетического гомеостаза играют гормоны инсулин и глюкагон, а также другие контринсулярные гормоны — адреналин, кортизол,йодтиронины и соматотропин. Инсулин- и глюкагон играют главную роль в регуляции метаболизма при смене абсорбтивного и постабсорбтивного периодов и при голодании.
А. Абсорбтивный период
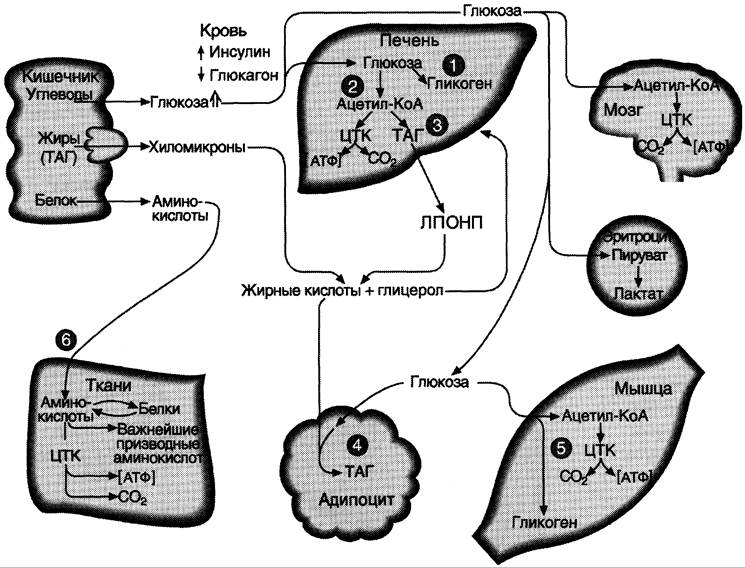
Абсорбтивный период характеризуется временным повышением концентрации глюкозы, аминокислот и жиров в плазме крови. Клетки поджелудочной железы отвечают на это повышение усилением секреции инсулина и снижением секреции глюкагона. Увеличение отношения инсулин/глюкагон вызывает ускорение использования метаболитов для запасания энергоносителей: происходит синтез гликогена, жиров и белков. Режим запасания включается после приёма пищи и сменяется режимом мобилизации запасов после завершения пищеварения. Тип метаболитов, которые потребляются, депонируются и экспортируются, зависит от типа ткани. Главные органы, связанные с изменениями потока метаболитов при смене режимов мобилизации и запасания энергоносителей, — печень, жировая ткань и мышцы (рис. 11-28).
Рис. 11-28. Пути использования основных энергоносителей в абсорбтивном периоде. 1 — биосинтез гликогена в печени; 2 — гликолиз; 3 — биосинтез ТАГ в печени; 4 — биосинтез ТАГ в жировой ткани; 5 — биосинтез гликогена в мышцах; 6 — биосинтез белков в разных тканях, в том числе в печени.
1. Изменения метаболизма в печени в абсорбтивном периоде
После приёма пищи печень становится главным потребителем глюкозы, поступающей из пищеварительного тракта. Почти 60 из каждых 100 г глюкозы, транспортируемой портальной системой, задерживается в печени. Увеличение потребления печенью глюкозы — не результат ускорения её транспорта в клетки (транспорт глюкозы в клетки печени не стимулируется инсулином), а следствие ускорения метаболических путей, в которых глюкоза превращается в депонируемые формы энергоносителей: гликоген и жиры.
При повышении концентрации глюкозы в гепатоцитах происходит активация глюкокиназы, превращающей глюкозу в глюкозо-6-фосфат. Глюкокиназа имеет высокое значение Кmдля глюкозы, что обеспечивает высокую скорость фосфорилирования при высоких концентрациях глюкозы. Кроме того, глюкокиназа не ингибируется глюкозо-6-фосфатом (см. раздел 7). Инсулин индуцирует синтез мРНК глюкокиназы. Повышение концентрации глюкозо-6-фосфата в гепатоцитах обусловливает ускорение синтеза гликогена. Этому способствуют одновременная инактивация гликогенфосфорилазы и активация гликогенсинтазы. Под влиянием инсулина в гепатоцитах ускоряется гликолиз в результате повышения активности и количества ключевых ферментов: глюкокиназы, фосфофруктокиназы и пируваткиназы. В то же время происходит торможение глюконеогенеза в результате инактивации фруктозо-1,6-бисфосфатазы и снижения количества фосфоенолпируваткарбоксикиназы — ключевых ферментов глюконеогенеза. Повышение концентрации глюкозо-6-фосфата в гепатоцитах в абсорбтивном периоде сочетается с активным использованием NАDРН для синтеза жирных кислот, что способствует стимуляции пентозофосфатного пути.
Ускорение синтеза жирных кислот обеспечивается доступностью субстратов (ацетил-КоА и NАDРН), образующихся при метаболизме глюкозы, а также активацией и индукцией ключевых ферментов синтеза жирных кислот (см. раздел 8 и табл. 11-7).
В абсорбтивном периоде в печени ускоряется синтез белков. Однако количество аминокислот, поступающих в печень из пищеварительного тракта, превышает возможности их использования для синтеза белков и других азотсодержащих соединений. Излишек аминокислот либо поступает в кровь и транспортируется в другие ткани, либо дезаминируется с последующим включением безазотистых остатков в общий путь катаболизма (см. раздел 9).
2. Изменения метаболизма в адипоцитах
Основная функция жировой ткани — запасание энергоносителей в форме триацилглицеролов. Под влиянием инсулина ускоряется транспорт глюкозы в адипоциты. Повышение внутриклеточной концентрации глюкозы и активация ключевых ферментов гликолиза обеспечивают образование ацетил-КоА и глицерол- 3-фосфата, необходимых для синтеза ТАГ. Стимуляция пентозофосфатного пути обеспечивает образование NADPH, необходимого для синтеза жирных кислот. Однако биосинтез жирных кислот de novo в жировой ткани человека протекает с высокой скоростью только после предшествующего голодания. При нормальном ритме питания для синтеза ТАГ используются в основном жирные кислоты, поступающие из ХМ и ЛПОНП под действием ЛП-липазы (см. раздел 8). Вместе с тем при увеличении отношения инсулин/глюкагон гормончувствительная ТАГ-липаза находится в дефосфорилированной неактивной форме, и процесс липолиза тормозится.
3. Изменение метаболизма в мышцах в абсорбтивном периоде
В абсорбтивном периоде под влиянием инсулина ускоряется транспорт глюкозы в клетки мышечной ткани. Глюкоза фосфорилируется и окисляется для обеспечения клетки энергией, а также используется для синтеза гликогена. Жирные кислоты, поступающие из ХМ и ЛПОНП, в этот период играют незначительную роль в энергетическом обмене мышц. Поток аминокислот в мышцы и биосинтез белков также увеличиваются под влиянием инсулина, особенно после приёма белковой пищи.
Б. Постабсорбтивный период
Постабсорбтивным состоянием называют период после завершения пищеварения до следующего приёма пищи. Если пища не принимается в течение суток и более, то это состояние определяют, как голодание. Типичным постабсорбтивным периодом считают состояние после 12-часового ночного перерыва в приёме пищи. В начале постабсорбтивного периода концентрация глюкозы в крови снижается, вследствие чего снижается секреция инсулина и повышается концентрация глюкагона. При снижении индекса инсулин/глюкагон ускоряются процессы мобилизации депонированных энергоносителей (рис. 11-29).
Рис. 11-29. Изменения метаболизма основных энергоносителей при смене абсорбтивного состояния на постабсорбтивное. КТ — кетоновые тела; ЖК — жирные кислоты.

В постабсорбтивном периоде изменения метаболизма направлены, главным образом, на поддержание концентрации в крови глюкозы, которая служит основным энергетическим субстратом для мозга и единственным источником энергии для эритроцитов. Основные изменения метаболизма в этот период происходят в печени и жировой ткани.
1. Изменения метаболизма в печени
В печени прежде всего ускоряется мобилизация гликогена (см. раздел 7). Однако запасы гликогена в печени истощаются в течение 18 — 24 ч голодания. Главным источником глюкозы по мере исчерпания запасов гликогена становится глюконеогенез, который начинает ускоряться через 4 — 6 ч после последнего приёма пищи. Субстратами для синтеза глюкозы служат глицерол, аминокислоты и лактат. При высокой концентрации глюкагона скорость синтеза жирных кислот снижается вследствие фосфорилирования и инактивации ацетил-КоА-карбоксилазы, а скорость β- окисления возрастает. Вместе с тем увеличивается снабжение печени жирными кислотами, которые транспортируются из жировых депо. Ацетил-КоА, образующийся при окислении жирных кислот, используется в печени для синтеза кетоновых тел.
2. Изменения метаболизма в жировой ткани
В жировой ткани при повышении концентрации глюкагона снижается скорость синтеза ТАГ и стимулируется липолиз. Стимуляция липолиза — результат активации гормончувствительной ТАГ-липазы адипоцитов под влиянием глюкагона. Жирные кислоты становятся важными источниками энергии в печени, мышцах и жировой ткани.
Таким образом, в постабсорбтивном периоде концентрация глюкозы в крови поддерживается на уровне 80 — 100 мг/дл, а уровень жирных кислот и кетоновых тел возрастает.
В. Изменение гормонального статуса и метаболизма при голодании
Голодание может быть кратковременным, в течение суток (I фаза), продолжаться в течение недели (II фаза) или нескольких недель (III фаза).
В отсутствие пищи в крови снижается уровень глюкозы, аминокислот и триацилглицеролов. Инсулин-глюкагоновый индекс снижается, и повышается концентрация контринсулярных гормонов, в первую очередь кортизола. В этих условиях возникает состояние, для которого характерно преобладание процессов катаболизма жиров, гликогена и белков на фоне общего снижения скорости метаболизма. Под влиянием контринсулярных гормонов в этот период происходит обмен субстратами между печенью, жировой тканью, мышцами и мозгом. Этот обмен служит двум целям: 1) поддержанию концентрации глюкозы в крови ддя обеспечения глюкозозависимых тканей (мозга, эритроцитов); 2) мобилизации других источников энергии, в первую очередь жиров, для обеспечения энергией всех других тканей. Вследствие переключения метаболизма на режим мобилизации энергоносителей даже после 5-6 нед голодания концентрация глюкозы в крови составляет не менее 60 мг/дл.
1. Обмен углеводов
Так как за счёт мобилизации гликогена обеспечивается только кратковременное голодание, основным источником глюкозы при длительном голодании служит глюконеогенез, а основными субстратами глюконеогенеза — аминокислоты, лактат и глицерол. При низкой концентрации инсулина глюкоза используется только инсулиннезависимыми тканями, в основном мозгом, эритроцитами. Обеспечение энергетических потребностей других тканей происходит за счёт жирных кислот и кетоновых тел.
2. Обмен жиров
Жирные кислоты, образующиеся в процессе мобилизации жиров в жировых депо, становятся основными источниками энергии для большинства органов в первый период голодания. Во II фазе мобилизация жиров продолжается, и концентрация жирных кислот в крови увеличивается в 3 — 4 раза по сравнению с постабсорбтивным состоянием. Синтез кетоновых тел начинается в первые дни голодания. Во II фазе голодания скорость синтеза кетоновых тел значительно возрастает. Концентрация кетоновых тел в крови в этот период может достигать 20 — 30 мг/дл (в норме 1-3 мг/дл). Используются кетоновые тела, в основном, в мышцах. В этот период голодания часть энергетических потребностей мозга обеспечивается кетоновыми телами, а скорость окисления кетоновых тел в мышцах снижается.
3. Обмен белков
В течение нескольких первых дней голодания быстро распадаются мышечные белки — основной источник субстратов для глюконеогенеза. При голодании более 3 нед скорость катаболизма белков стабилизируется и составляет примерно 20 г в сутки. В этот период увеличивается потребление мозгом кетоновых тел, а скорость глюконеогенеза снижается. Снижение скорости глюконеогенеза способствует сбережению белков. В этот период и для мозга кетоновые тела становятся значительным источником энергии. Однако для окисления кетоновых тел необходимы оксалоацетат и другие компоненты ЦТК. В норме они образуются из глюкозы и аминокислот, а при
голодании — только из аминокислот. При продолжительности голодания более 4 недель развиваются атрофические процессы, в результате которых происходит потеря значительного количества белков. В теле человека массой 70 кг масса белков составляет 15 кг. При потере 1/3 — 1/2 белков наступает смерть.