БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ - Е. С. Северина - 2004
РАЗДЕЛ 13. МЕТАБОЛИЗМ ГЕМА И ОБМЕН ЖЕЛЕЗА
Гем является простетической группой многих белков: гемоглобина, миоглобина, цитохромов митохондриальной ЦПЭ, цитохрома Р450, участвующего в микросомальном окислении. Ферменты каталаза, пероксидаза, цитохромоксидаза содержат гем в качестве кофермента.
Все клетки организма имеют гемсодержащие белки, поэтому синтез гема идёт во всех клетках, за исключением эритроцитов, не имеющих, как известно, белоксинтезирующей системы.
При распаде гема в клетках РЭС образуется жёлчный пигмент билирубин. Дальнейший катаболизм билирубина в печени, кишечнике и почках приводит к образованию конечных продуктов распада гема стеркобилина и уробилина, содержащихся, соответственно, в кале и моче. Железо, освобождающееся при распаде гема, снова используется для синтеза железосодержащих белков.
I. Строение и биосинтез гема
А. Строение гема
Гем состоит из иона двухвалентного железа и порфирина (рис. 13-1). В основе структуры порфиринов находится порфин. Порфин представляет собой четыре пиррольных кольца, связанных между собой метеновыми мостиками (рис. 13-1). В зависимости от структуры заместителей в кольцах пирролов различают несколько типов порфиринов: протопорфирины, этиопорфирины, мезопорфирины и копропорфирины. Протопорфирины — предшественники всех других типов порфиринов.
Рис. 13-1. Строение порфина (А), протопорфирина IX (Б) и гема гемоглобина (В). Порфин — циклическая структура, состоящая из четырёх пиррольных колец, связанных между собой метеновыми мостиками. Протопорфирин IX имеет четыре метильных, два винильных радикала и два остатка пропионовой кислоты. В геме гемоглобина Fе2+ образует две ковалентные и две координационные связи с атомами азота пиррольных колец протопорфирина IX.

Гемы разных белков могут содержать разные типы порфиринов (см. раздел 6). В геме гемоглобина находится протопорфирин IX, который имеет 4 метальных, 2 винильных радикала и 2 остатка пропионовой кислоты. Железо в геме находится в восстановленном состоянии (Fе+2) и связано двумя ковалентными и двумя координационными связями с атомами азота пиррольных колец. При окислении железа гем превращается в гематин (Fе3+). Наибольшее количество гема содержат эритроциты, заполненные гемоглобином, мышечные клетки, имеющие миоглобин, и клетки печени из-за высокого содержания в них цитохрома Р450.
Б. Биосинтез гема
Гем синтезируется во всех тканях, но с наибольшей скоростью в костном мозге и печени (рис. 13-2). В костном мозге гем необходим для синтеза гемоглобина в ретикулоцитах, в гепатоцитах — для образования цитохрома Р450.
Рис. 13-2. Синтез гема. Цифрами на схеме указаны ферменты: 1 — аминолевулинатсинтаза; 2 — аминолевулинатдегидратаза; 3 — порфобилиногендезаминаза; 4 — уропорфириноген III косинтаза; 5 — уропорфириногендекарбоксилаза; 6 — копропорфириноген III оксидаза; 7 — протопорфириногеноксидаза; 8 — феррохелатаза. Буквами обозначены заместители в пиррольных кольцах: М — метил, В — винил, П — остатки пропионовой кислоты, А — ацетил, ПФ — пиридоксальфосфат. Донором железа служит депонирующий железо в клетках белок ферритин.
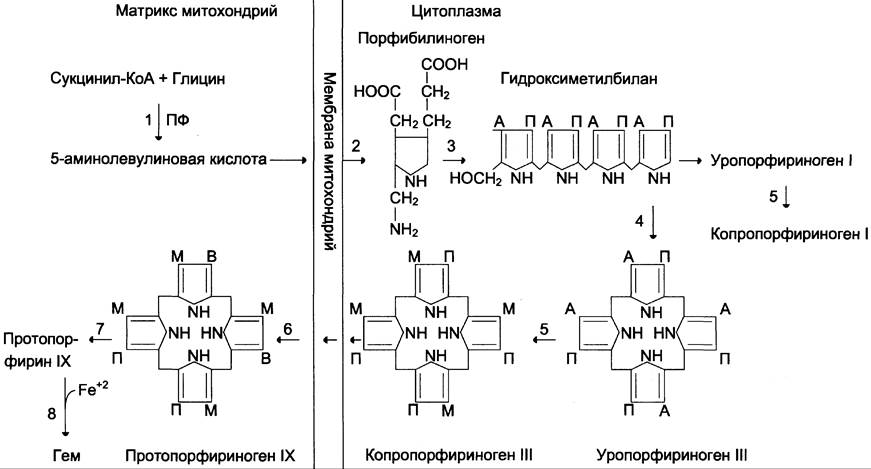
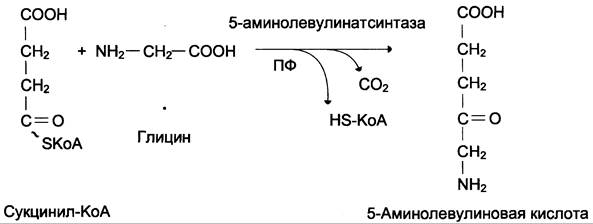
Первая реакция синтеза гема — образование 5-аминолевулиновой кислоты из глицина и сукцинил-КоА (рис. 13-3) идёт в матриксе митохондрий, где в ЦТК образуется один из субстратов этой реакции — сукцинил-КоА. Эту реакцию катализирует пиридоксальзависимый фермент аминолевулинатсинтаза.
Рис. 13-3. Реакция образования 5-аминолевулиновой кислоты.
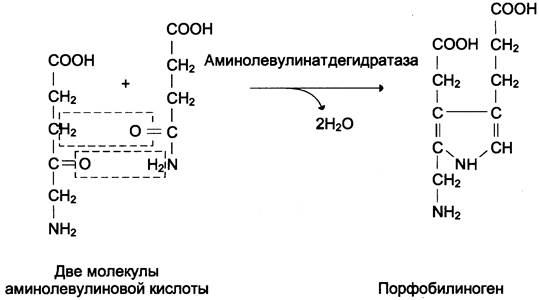
Из митохондрий 5-аминолевулиновая кислота поступает в цитоплазму. В цитоплазме проходят промежуточные этапы синтеза гема: соединение 2 молекул 5-аминолевулиновой кислоты в молекулу порфобилиногена (рис. 13-4), дезаминирование порфобилиногена с образованием гидроксиметилбилана, ферментативное превращение гидроксиметилбилана в молекулу уропор- фобилиногена III, декарбоксилирование последнего с образованием копропорфириногена III. Гидроксиметилбилан может также неферментативно превращаться в уропорфириноген I, который декарбоксилируется в копропорфириноген I. Из цитоплазмы копропорфириноген III опять поступает в митохондрии, где проходят заключительные реакции синтеза гема. В результате двух последовательных окислительных реакций копропорфириноген III превращается в протопорфириноген IX, а протопорфириноген IX — в протопорфирин IX. Фермент феррохелатаза, присоединяя к протопорфирину IX двухвалентное железо, превращает его в гем (рис. 13-2). Источником железа для синтеза гема служит депонирующий железо белок ферритин. Синтезированный гем, соединяясь с α- и β-полипепептидными цепями глобина, образует гемоглобин. Гем регулирует синтез глобина: при снижении скорости синтеза гема синтез глобина в ретикулоцитах тормозится.
Рис. 13-4. Реакция образования порфобилиногена.
В. Регуляция биосинтеза гема
Регуляторную реакцию синтеза гема катализирует пиридоксальзависимый фермент аминолевулинатсинтаза. Скорость реакции регулируется аллостерически и на уровне трансляции фермента.
Аллостерическим ингибитором и корепрессором синтеза аминолевулинатсинтазы является гем (рис. 13-5).
Рис. 13-5. Регуляция синтеза гема и гемоглобина. Гем по принципу отрицательной обратной связи ингибирует аминолевулинатсинтазу и аминолевулинатдегидратазу и является индуктором трансляции α- и β-цепей гемоглобина.

В ретикулоцитах синтез этого фермента на этапе трансляции регулирует железо. На участке инициации мРНК, кодирующей фермент, имеется последовательность нуклеотидов, образующая шпилечную петлю, которая называется железочувствительным элементом (от англ. iron- responsive element, IRE) (рис. 13-6).
Рис. 13-6. Регуляция синтеза аминолевулинатсинтазы. А — при высокой концентрации железа в ретикулоцитах оно присоединяется к железосвязывающему белку и снижает сродство этого белка к железочувствительному элементу (IRE) матричной РНК, кодирующей аминолевулинатсинтазу. Белковые факторы инициации трансляции связываются с мРНК и инициируют трансляцию аминолевулинатсинтазы. Б — при низком содержании железа в ретикулоцитах железосвязывающий белок обладает высоким сродством к IRE и взаимодействует с ним. Белковые факторы инициации трансляции не могут присоединиться к мРНК, и трансляция прекращается.
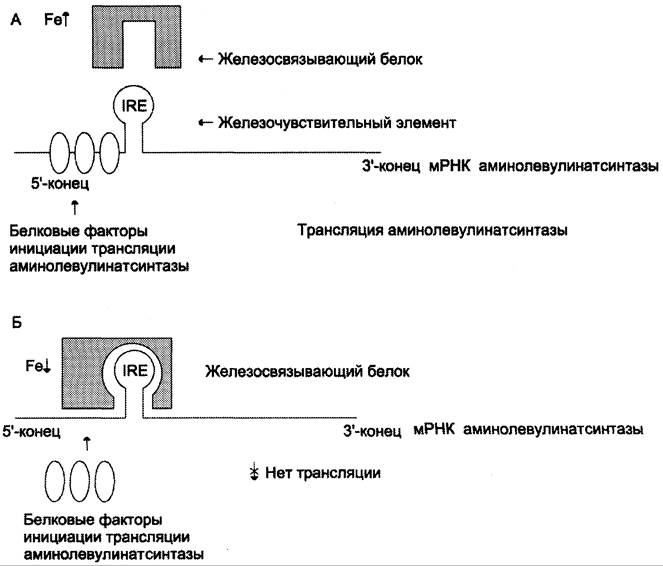
При высоких концентрациях железа в клетках оно образует комплекс с остатками цистеина регуляторного железосвязывающего белка. Взаимодействие железа с регуляторным железосвязывающим белком вызывает снижение сродства этого белка к IRE-элементу мРНК, кодирующей аминолевулинатсинтазу, и продолжение трансляции (рис. 13-6, А). При низких концентрациях железа железосвязывающий белок присоединяется к железочувствительному элементу, находящемуся на 5'-нетранслируемом конце мРНК, и трансляция аминолевулинатсинтазы тормозится (рис. 13-6, Б).
Аминолевулинатдегидратаза также аллостерически ингибируется гемом, но так как активность этого фермента почти в 80 раз превышает активность аминолевулинатсинтазы, то это не имеет большого физиологического значения.
Дефицит пиридоксальфосфата и лекарственные препараты, которые являются его структурными аналогами, снижают активность аминолевулинатсинтазы.
Г. Нарушения биосинтеза гема. Порфирии
Наследственные и приобретённые нарушения синтеза гема, сопровождающиеся повышением содержания порфириногенов, а также продуктов их окисления в тканях и крови и появлением их в моче, называют порфириями («порфирин» в переводе с греч. означает пурпурный).
Наследственные порфирии обусловлены генетическими дефектами ферментов, участвующих в синтезе гема, за исключением аминолевулинатсинтазы. При этих заболеваниях отмечают снижение образования гема. Поскольку гем — аллостерический ингибитор аминолевулинатсинтазы, то активность этого фермента повышается, и это приводит к накоплению промежуточных продуктов синтеза гема — аминолевулиновой кислоты и порфириногенов.
В зависимости от основной локализации патологического процесса различают печёночные и эрйтропоэтические наследственные порфирии. Эритропоэтические порфирии сопровождаются накоплением порфиринов в нормобластах и эритроцитах, а печёночные — в гепатоцитах.
При тяжёлых формах порфирий наблюдают нейропсихические расстройства, нарушения функций РЭС, повреждения кожи. Порфириногены не окрашены и не флуоресцируют, но на свету они легко превращаются в порфири- ны. Последние проявляют интенсивную красную флуоресценцию в ультрафиолетовых лучах. В коже на солнце в результате взаимодействия с порфиринами кислород переходит в синглетное состояние. Синглетный кислород вызывает ускорение ПОЛ клеточных мембран и разрушение клеток, поэтому порфирии часто сопровождаются фотосенсибилизацией и изъязвлением открытых участков кожи. Нейропсихические расстройства при порфириях связаны с тем, что аминолевулинат и порфириногены являются нейротоксинами.
Иногда при лёгких формах наследственных порфирий заболевание может протекать бессимптомно, но приём лекарств, являющихся индукторами синтеза аминолевулинатсинтазы, может вызвать обострение болезни. Индукторами синтеза аминолевулинатсинтазы являются такие известные лекарства, как сульфаниламиды, барбитураты, диклофенак, вольтарен, стероиды, гестагены. В некоторых случаях симптомы болезни не проявляются до периода полового созревания, когда повышение образования β-стероидов вызывает индукцию синтеза аминолевулинатсинтазы. Порфирии наблюдают и при отравлениях солями свинца, так как свинец ингибирует аминолевулинатдегидратазу и феррохелатазу. Некоторые галогенсодержащие гербициды и инсектициды являются индукторами синтеза аминолевулинатсинтазы, поэтому попадание их в организм сопровождается симптомами порфирии.