Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ III. МЕТАБОЛІЗМ ОСНОВНИХ КЛАСІВ БІОМОЛЕКУЛ
ГЛАВА 12. МЕТАБОЛІЗМ ВУГЛЕВОДІВ. II. АЛЬТЕРНАТИВНІ ШЛЯХИ ОБМІНУ МОНОСАХАРИДІВ. РЕГУЛЯЦІЯ ОБМІНУ ГЛЮКОЗИ
12.3. БІОСИНТЕЗ ГЛЮКОЗИ ТА ЙОГО РЕГУЛЯЦІЯ
Головном джерелом глюкози як метаболічного палива для організму людини є її надходження з харчовими продуктами у вигляді полісахариду крохмалю та сахарози. Надлишок глюкози, шо не використовується в окислювальних реакціях аеробного та анаеробного гліколізу, відкладається у вигляді енергетичних депо — глікогену та триацилгліцеролів. Втім, існують метаболічні шляхи, що забезпечують організм глюкозою за рахунок її синтезу з невуглеводних біомолекул.
Глюконеогенез (гліконеогенез) — синтез глюкози з невуглеводних метаболічних попередників, до яких належать: піруват (та лактат); деякі амінокислоти (глюкогенні амінокислоти); певна кількість глюкози може утворюватися з гліцеролу та продуктів катаболізму жирних кислот з непарною кількістю вуглецевих атомів у вуглеводневому ланцюзі.
Фізіологічне значення глюконеогенезу
Реакції глюконеогенезу відбуваються переважно в печінці та, в деякій мірі, в кірковому шарі нирок, оскільки в клітинах саме цих органів присутній повний набір необхідних ферментів.
За добу в організмі дорослої людини синтезується до 80 г глюкози. Біосинтез глюкози забезпечує її нормальну концентрацію в умовах зменшеного надходження моносахариду із зовнішнього середовища та вичерпання головного акумульованого джерела глюкози — глікогену печінки та м’язів. Така фізіологічна ситуація спостерігається через декілька годин після прийому їжі (постабсорбтивний стан, що відбувається зранку, натщесерце), в умовах тривалого голодування, після виснажливої фізичної роботи. Особливо чутливий до зменшення внутрішньоклітинної концентрації глюкози головний мозок людини, для якого глюкоза є основним субстратом енергетичного обміну, що споживається в кількості близько 120 г за добу.
Метаболічний шлях глюконеогенезу
Метаболічний шлях глюконеогенезу є значною мірою оберненням гліколізу (що утворює з глюкози піруват та лактат) за виключенням трьох гліколітичних «кіназних» реакцій, які є термодинамічно незворотними і потребують обхідних (шунтових) механізмів.
Незворотними реакціями гліколізу є:
1) гексокіназна (або глюкокіназна) реакція:
![]()
2) фосфофруктокіназна реакція:
![]()
3) піруваткіназна реакція:
![]()
Виходячи з незворотності зазначених реакцій, для перетворення пірувату (або лактату) в глюкозу необхідні додаткові, специфічні для глюконеогенезу ферментативні реакції. Це реакції:
- перетворення глюкозо-6-фосфату в глюкозу;
- перетворення фруктозо-1,6-дифосфату в фруктозо-6-фосфат;
- перетворення пірувату в фосфоенолпіруват.
Реакції та ферменти глюконеогенезу
1. Перетворення пірувату в фосфоенолпіруват.
Реакція відбувається в дві послідовні стадії:
1). Перетворення пірувату в оксалоацетат (щавлевооцтову кислоту) за участю ферменту піруваткарбоксилази:
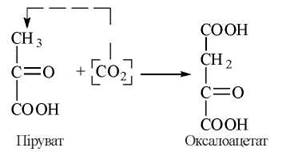
![]()
Піруваткарбоксилаза локалізована всередині мітохондрій. Простетичною групою ферменту є карбоксибіотин — коферментна форма СО2-транспортуючого вітаміну Н. Макроергічний зв’язок АТФ витрачається на карбоксилювання зв’язаного з ферментом біотину (див. главу 15, п. 15.1).
2). Перетворення оксалоацетату в фосфоенолпіруват (ФЕП) за участю ферменту фосфоенолпіруваткарбоксикінази (ФЕП-кінази):
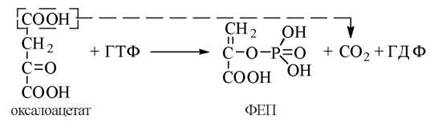
![]()
У клітинах більшості тваринних організмів ФЕП-кіназа локалізована в цитозолі, у людини — в цитозолі, частково — в мітохондріях.
Компартменталізація перетворення пірувату в ФЕП
Піруваткарбоксилазна реакція є однією з анаплеротичних реакцій циклу трикарбонових кислот, що забезпечують підтримання високої концентрації певних метаболітів ЦТК — в даному випадку — оксалоацетату (див. главу 10, п.10.4). Реакція відбувається всередині мітохондрій, і для включення оксалоацетату в реакції глюконеогенезу (за рахунок дії цитозольної ФЕП-кінази та інших ферментів глюконеогенезу) необхідно транспортувати оксалоацетат через мембрани мітохондрій у цитозоль.
Транспортування оксалоацетату в цитозоль забезпечується за допомогою однієї з човникових систем (шунтів — shuttles, англ.), принцип дії яких полягає в перетворенні мітохондріального оксалоацетату, для якого внутрішні мембрани мітохондрій є непроникними, в сполуку, що може дифундувати в цитозоль і там розщеплюватися з утворенням знову оксалоацетату. Човникові механізми використовуються для виходу з мітохондрій у цитозольний простір оксалоацетату, ацетил-КоА, надходження з цитозолю в мітохондрії гліколітичного НАДН. Човникові системи транспорту оксалоацетату:
1) малатна човникова система — включає в себе: відновлення оксалоацетату до малату за участю мітохондріального ізоферменту малатдегідрогенази:
![]()
вихід малату через мембрани мітохондрій у цитозоль і подальше окислення малату до оксалоацетату цитозольним ізоферментом малатдегідрогенази:
![]()
2) аспартатна човникова система — функціонує шляхом внутрішньомітохондріального перетворення оксалоацетату в аспартат:
![]()
з подальшим виходом аспартату в цитозоль і зворотним його перетворенням знову в оксалоацетат; механізм забезпечується послідовною дією мітохондріального та цитозольного ізоферментів аспартатамінотрансферази.
3) цитратна човникова система — функціонує шляхом внутрішньомітохондріального утворення з оксалоацетату цитрату (за рахунок дії цитратсинтази):
![]()
подальшого виходу цитрату в цитозоль і його розщеплення з вивільненням знову оксалоацетату за дії цитратліази:
![]()
Основним механізмом виходу оксалоацетату в цитозоль, що постачає цитозольний ФЕП, який далі використовується в реакціях глюконеогенезу, є малатний шунт, принципи функціонування якого подано на схемі (рис. 12.5):
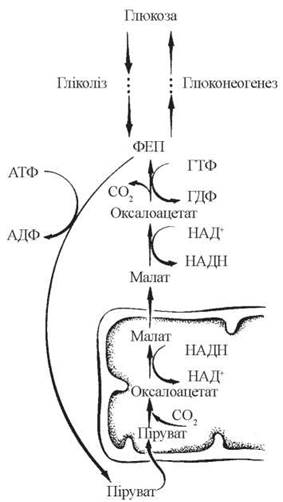
Рис. 12.5. Схема малатного шунта.
2. Перетворення фруктозо-1,6-дифосфату в фруктозо-6-фосфат:
Реакція каталізується регуляторним ферментом фруктозо-1,6-дифосфатазою (Фр-1,6-дифосфатазою), що міститься в печінці (головним чином), а також у нирках і епітеліоцитах кишечника.Фруктозо-1,6-дифосфатазна реакція забезпечує шунтування незворотної фосфофруктокіназної реакції гліколізу.
3. Перетворення глюкозо-6-фосфату в глюкозу:
![]()
Реакція забезпечує шунтування незворотної гексокіназної (глюкокіназної) реакції гліколізу; каталізується ферментом глюкозо-6-фосфатазою (Г-6-Ф-азою), найбільш високий вміст якого — в мембранах ендоплазматичного ретикулуму гепатоцитів. Завдяки наявності в печінці високої концентрації глюкозо-6-фосфатази, саме цей орган забезпечує вихід у кров вільної глюкози за рахунок гідролізу глюкозо-6-фоcфату, що утворюється при глюконеогенезі або фосфоролітичному розщепленні глікогену. Цей механізм є основним у підтриманні нормальної глюкоземії, особливо в умовах голодування.
Сумарна реакція та енергетика глюконеогенезу
Решта реакцій, що необхідні для перетворення невуглеводних субстратів у глюкозу, є реакціями гліколізу, які можуть перебігати у фізіологічних умовах як у прямому, так і в зворотному напрямках. Сумарна реакція глюконеогенезу (враховуючи витрати 2 молекул АТФ та 2 молекул НАДН для зворотного перетворення 2 молекул 3-фосфогліцеринової кислоти на 2 молекули 3-фосфогліцеринового альдегіду) має вигляд:
![]()
Наведене рівняння доводить, що глюконеогенез є суттєво ендергонічним метаболічним шляхом: синтез однієї молекули глюкози з двох молекул пірувату потребує витрат шести макроергічних зв’язків; тому глюконеогенез, як і гліколіз, є незворотним біохімічним процесом.
Загальну схему глюконеогенезу подано на рис. 12.6. Суцільними стрілками позначені реакції глюконеогенезу, перервними — реакції гліколізу та ЦТК. На схемі зазначені також місця входження в глюконеогенез основних глюкогенних амінокислот (див. нижче).
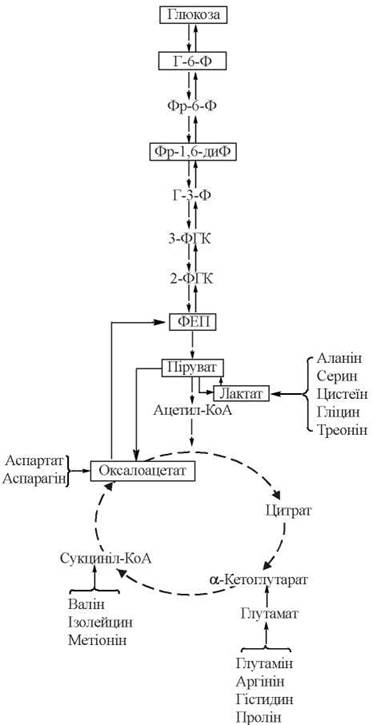
Рис. 12.6. Метаболічна карта глюконеогенезу.
Позначення: Г-6-Ф — глюкозо-6-фосфат; Фр-6-Ф — фруктозо-6-фосфат; Фр-1,6-диФ — фруктозо-1,6-дифосфат; Г-3-Ф — гліцеральдегід-3-фосфат; 3-ФГК — 3-фосфогліцеринова кислота; 2-ФГК — 2-фосфогліцеринова кислота; ФЕП — фосфоенолпіруват.
Субстрати глюконеогенезу
Основними попередниками (субстратами) глюконеогенезу є піруват (лактат) та амінокислоти (переважно аланін), що утворюються, головним чином, у функціонуючих скелетних м’язах, еритроцитах та клітинах деяких інших тканин.
1. Утворення пірувату з лактату в печінці
Лактат, утворенний з пірувату в анаеробному гліколізі, є кінцевим продуктом метаболізму; його включення в обмін речовин (окислення або використання в синтезі глюкози — глюконеогенезі) можливе лише через реокислення до пірувату в лактатдегідрогеназній реакції:
![]()
Реакція каталізується розглянутою вище (глава 11) лактатдегідрогеназою і є протилежною за напрямком відносно лактатдегідрогеназної реакції, яка утворює лактат із пірувату в умовах анаеробного гліколізу.
Напрямок ЛДГ-азної реакції в бік утворення пірувату наявний саме в глюконеогенних тканинах (печінка, нирки), де його спрямованість визначається відповідними відношеннями НАД+/НАДН, піруват/лактат, присутністю певного ізоферменту ЛДГ. При цьому джерелом лактату для печінкового глюконеогенезу є лактат, який надходить через плазму крові з місць його утворення — переважно скелетних м’язів.
Глюкозо-лактатний цикл
Таким чином, формується циклічний процес (глюкозо-лактатний цикл, або цикл Корі), що пов’язує процеси утворення лактату в клітинах м’язової тканини в ході анаеробного гліколізу, його вихід у кров через плазматичні мембрани м’язових клітин і використання лактату (після окислення в піруват) в гепатоцитах для глюконеогенезу (рис. 12.7). Частина пірувату (не зазначена на схемі) окислюється в піруватдегідрогеназній реакції до ацетил-КоА.
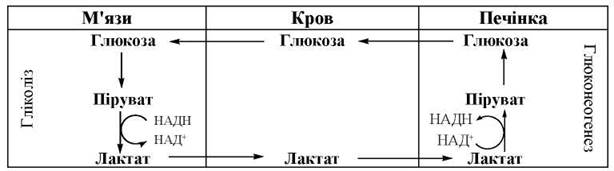
Рис. 12.7. Глюкозо-лактатний цикл (цикл Корі).
У скелетних м’язах ЛДГ-азна реакція перебігає переважно в бік утворення з пірувату лактату (глава 11). За рахунок відновлення пірувату в лактат та подальшого його використання для глюконеогенезу в печінці (цикл Корі), скелетні м’язи не тільки втрачають «зайву» молочну кислоту, що утворюється в особливо значних кількостях при інтенсивній фізичній праці, а й підтримують високе співвідношення НАД+/НАДН, необхідне для активного функціонування гліколізу (використання НАД+ у процесі гліколітичної оксидоредукції).
2. Глюкогенні амінокислоти
Безпосередніми попередниками глюкози при її синтезі (та, власне, метаболітами глюконеогенезу) є піруват, оксалоацетат та фосфоенолпіруват. Амінокислоти, які в результаті втрати аміногрупи (в реакціях дезамінування або трансамінування) перетворюються в зазначені безазотисті сполуки, можуть, таким чином, розглядатися як субстрати глюконеогенезу; такі амінокислоти отримали назву глюкогенних амінокислот (амінокислоти, вуглеводнева частина яких перетворюється в ацетоацетат або ацетил-КоА, з яких синтез глюкози за рахунок глюконеогенезу неможливий — кетогенні амінокислоти).
Окремі глюкогенні амінокислоти та ділянки їх включення в метаболічний шлях глюконеогенезу зазначені на рис. 12.6.
Глюконеогенез за участю амінокислот найбільш активний за умов повного голодування, коли підтримання рівня енергетичних процесів в організмі, зокрема нормальної концентрації глюкози крові та головного мозку, здійснюється за рахунок катаболізму власних тканинних білків.
Глюкозо-аланіновий цикл
Важливим субстратом глюконеогенезу в печінці є аланін, який може утворюватися в скелетних м’язах у зворотній реакції трансамінування пірувату з глутаматом:
![]()
Вивільняючись із працюючих м’язів у кров, аланін поглинається гепатоцитами і (після перетворення в піруват) використовується в глюконеогенезі (глюкозо-аланіновий цикл):
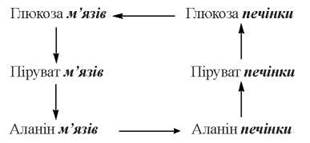
Регуляція глюконеогенезу
Контроль швидкості процесів глюконеогенезу забезпечується за рахунок метаболітної (алостеричної) регуляції, гормональної регуляції активності та синтезу певних глюконеогенних ферментів.
1. Метаболітна регуляція глюконеогенезу — реалізується на рівні таких регуляторних ферментів:
піруваткарбоксилази — ферменту, позитивним модулятором якого є ацетил-КоА; за відсутності ацетил-КоА піруваткарбоксилаза є практично неактивною;
фруктозо-1,6-дифосфатази — ферменту, активність якого залежить від співвідношення між концентраціями позитивного модулятора АТФ та негативного модулятора АМФ, який є інгібітором активності фруктозо-1,6-дифосфатази.
Таким чином, через регуляцію рівнів каталітичної активності зазначених алостеричних ферментів контролюється швидкість усього синтезу глюкози, залежно від загальної метаболічної ситуації в клітині:
-глюконеогенез активується в умовах зменшення внутрішньоклітинної концентрації глюкози, про що свідчить накопичення ацетил-КоА (продукту аеробного гліколізу), та за умов достатнього забезпечення джерелом хімічної енергії (у формі АТФ);
- глюконеогенез гальмується при зменшенні концентрації ацетил-КоА (що відображує зменшення швидкості розщеплення глюкози) та за умов недостатнього енергетичного забезпечення процесу (збільшення співвідношення АМФ/АТФ).
2. Гормональна регуляція глюконеогенезу — здійснюється за участю глюкагону, адреналіну (епінефрину), глюкокортикоїдних гормонів кори надниркових залоз та інсуліну.
2.1. Глюкагон, адреналін та глюкокортикоїди підвищують швидкості синтезу в гепатоцитах шунтових ферментів глюконеогенезу — ФЕП-кінази, Фр-1,6-дифосфатази, Г-6-Ф-ази.
2.1. Інсулін пригнічує синтез зазначених глюконеогенних ферментів, що гальмує активність процесу глюконеогенезу.