Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ V. ГОРМОНИ В СИСТЕМІ МІЖКЛІТИННОЇ ІНТЕГРАЦІЇ ФУНКЦІЙ ОРГАНІЗМУ
ГЛАВА 24. ГОРМОНАЛЬНА РЕГУЛЯЦІЯ МЕТАБОЛІЗМУ ТА БІОЛОГІЧНИХ ФУНКЦІЙ КЛІТИНИ. II. ГОРМОНИ - ПОХІДНІ ПЕПТИДІВ ТА АМІНОКИСЛОТ
24.4. КАТЕХОЛАМІНИ ТА ІНШІ БІОГЕННІ АМІНИ
На відміну від тиреоїдних гормонів, значна група похідних амінокислот — біорегуляторів із властивостями гормонів та нейромедіаторів — реалізують свою регуляторну дію на клітини через мембранні рецептори, спряжені з внутрішньоклітинними сигнальними системами. До цього класу біорегуляторів належать біогенні аміни:
- похідні L-тирозину катехоламіни: адреналін, норадреналін, дофамін;
- похідні L-триптофану індоламіни: серотонін та мелатонін;
- похідне L-гістидину (імідазоламін) гістамін.
1. Катехоламіни
Катехоламіни адреналін (епінефрин) та норадреналін (норепінефрин) синтезуються в хромафінних клітинах мозкового шару наднирникових залоз, гангліях симпатичної нервової системи та адренергічних структурах центральної нервової системи.
Обидва катехоламіни мають властивості як гормонів, так і нейромедіаторів, проте в адреналіну переважає «гормональна» дія, а в норадреналіну — «медіаторна». Згідно з такими функціональними відмінностями, основним місцем синтезу та локалізації в організмі адреналіну є мозковий шар наднирникових залоз (на його частку припадає близько 80 % усіх кaтехоламінів цієї структури), тоді як норадреналін міститься переважно в нейронах, його концентрація в головному мозку людини перевищує відповідний рівень адреналіну в десятки разів.
Попередниками в біосинтезі катехоламінів є циклічні амінокиcлоти фенілаланін та тирозин; ферментативні реакції синтезу включають процеси гідроксилювання в ядрі та бічному ланцюзі, декарбоксилювання з утворенням аміну та метилювання норадреналіну до адреналіну (рис. 24.6).
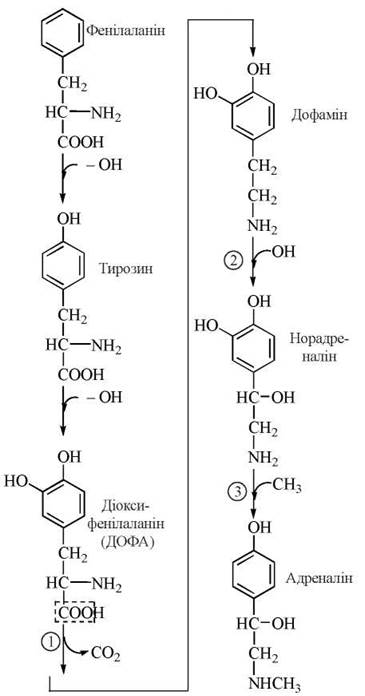
Рис. 24.6. Схема біосинтезу катехоламінів.
Адреналін
Ефекти адреналіну пов’язані з його взаємодією з різними класами адренорецепторів (α, β), що локалізовані як в центральній нервовій системі (глава 33), так і в численних ефекторних системах організму.
Фізіологічні прояви дії адреналіну характеризуються тонізуючим впливом на міокард (збільшення сили та частоти серцевих скорочень), загальне судинне русло (гіпертензивна дія), гладенькі м’язи судин різних внутрішніх органів, зокрема шлунково-кишкового тракту, нирок, бронхів, матки, ока тощо.
Біохімічні ефекти адреналіну проявляються, в основному, в катаболічній дії гормону на вуглеводний та ліпідний (жировий) обмін, опосередкований мембранними рецепторами, сполученими з аденілатциклазними ферментними каскадами.
1. Вплив адреналіну на обмін вуглеводів (глава 13) проявляється активацією глікогенфосфорилази, тобто глікогенолітичною дією (переважно в м’язах і частково — в печінці та інших органах), що призводить до активації глікогенолізу в м’язах і забезпеченні енергією м’язового скорочення; гіперглюкоземія, шо розвивається в умовах збільшеного виділення адреналіну (звичайно, разом із стимуляцією секреції глюкагону), має значення для забезпечення метаболічною енергією інших тканин (особливо головного мозку).
2. Вплив адреналіну на обмін ліпідів (глава 14) характеризується ліполітичним ефектом, спричиненим стимулювальною дією гормону на активність ТГ-ліпази адипоцитів жирової тканини. Вихід у кров’яне русло вільних жирних кислот (мобілізація НЕЖК, в якій бере участь також глюкагон) є також біохімічним механізмом забезпечення інших тканин (зокрема, міокарда) додатковими енергетичними субстратами.
Таким чином, сумарний підсумок фізіологічних та біохімічних ефектів катехоламінів (адреналіну та норадреналіну) має на меті підготовку організму до максимального використання енергетичних ресурсів та їх реалізацію в умовах стресових реакцій — ситуаціях типу «боротьба або втікання», спрямованих на фізичне виживання особини. Вивільнення адреналіну з хромафінних клітин та норадреналіну із закінчень симпатичних нейронів є біохімічним уособленням термінової активації симпатикоадреналової системи (У. Кеннон) у відповідь на вплив стресових факторів. Процеси довгострокової адаптації організму до дії пошкоджувальних агентів реалізуються глюкокортикоїдами кори наднирникових залоз (глава 25).
Розщеплення адреналіну та норадреналіну каталізується моноамінооксидазами мітохондрій з утворенням гормонально неактивних альдегідів та ванілілмигдальної кислоти.
Дофамін — біогенний амін, що є інтермедіатом у синтезі катехоламінів адреналіну та норадреналіну. Синтез цього аміну та чутливі до нього рецепторні структури локалізуються переважно в гіпоталамусі, мезокортикальній, лімбічній, екстрапірамідній системах головного мозку. Окрім нейромедіаторних властивостей у центральній нервовій системі, дофамін має близькі до інших катехоламінів симпатоміметичні властивості. Разом з тим, дофамін здійснює специфічний саме для нього вплив на функцію серцево-судинної системи, спричиняє дилатацію судин нирок, збільшує діурез та натрійурез, стимулює екзокринну функцію підшлункової залози.
2. Індоламіни
Серотонін (5-гідрокситриптамін) — біогенний амін, попередником якого є гідроксильований триптофан (5-гідрокси- триптофан), що підлягає декарбоксилюванню за участю ПАЛФ-залежної декарбоксилази з утворенням біологічно активного аміну:
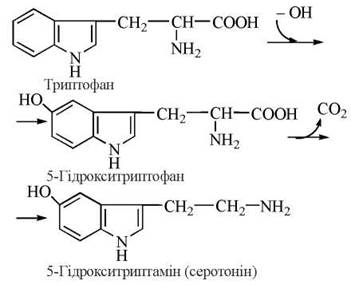
Біологічні функції серотоніну в організмі людини різноманітні. Крім нейромедіаторної дії в спеціальних (серотонінергічних) ділянках центральної нервової системи та участі в реалізації складних інтегративних психічних функцій, серотонін здійснює регуляторні ефекти щодо діяльності гладеньких м’язів та, відповідно, функцій серцево-судинної системи, шлунково-кишкового тракту, бронхів, модулює розвиток запальних та алергічних реакцій, процесів згортання крові. Характеристику серотонінергічних метаботропних рецепторів нервової системи та молекулярних механізмів дії серотоніну подано в главі 33.
Найвищий вміст серотоніну знайдено в ентерохромафінних клітинах дванадцятипалої кишки, тромбоцитах, тучних клітинах сполучної тканини, центральній нервовій системі. В головному мозку людини серотонін розподілений нерівномірно: найбільша його кількість міститься в гіпоталамічній ділянці та середньому мозку.
Катаболізм серотоніну в організмі, як і інших фізіологічно активних амінів, відбувається за участю мітохондріальної моноамінооксидази; в результаті реакції утворюється 5-оксііндолацетальдегід, який окислюється до кінцевого катаболіту — 5-оксііндолоцтової кислоти, що виділяється із сечею.
Мелатонін
Похідним триптофану є також мелатонін (N-ацетил-5-метокситриптамін) — біогенний амін, що утворюється в результаті N-ацетилювання та О-метилювання серотоніну.
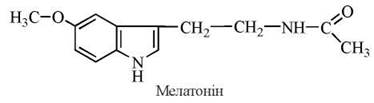
Біосинтез мелатоніну відбувається в пінеалоцитах епіфіза та деяких периферійних тканинах: шлунково-кишковому тракті, сітківці, ціліарному тілі ока тощо. Продукція мелатоніну в епіфізі має циклічний циркадний характер, вона збільшується у темряві і гальмується яскравим світлом.
Біологічні ефекти мелатоніну охоплюють широкий спектр фізіологічних функцій: він є універсальним синхронізатором ендогенних біоритмів в організмі людини, одним із регуляторів циклу «сон-неспання» (прискорює процес засинання, модулює структуру сну), гальмує секрецію гонадотропних гормонів гіпофіза, соматотропіну, тиреоїдних гормонів та кортикостероїдів, стимулює деякі імунні реакції тощо.
Вважають, що синтез мелатоніну в епіфізі є важливим компонентом системи регуляції статевої функції у людини: так, зокрема, значне падіння рівня мелатоніну в крові у хлопчиків в період статевого дозрівання може бути регуляторним сигналом, що запускає початок пубертатного періоду.
Мелатонін має високі антиоксидантні властивості як інгібітор реакцій вільнорадикального окислення, що за деякими параметрами перевищують відповідні характеристики вітаміну Е (α-токоферолу). У нижчих тварин мелатонін є регулятором пігментації покривних тканин.
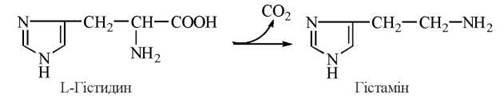
3. Гістамін — похідне L-гістидину, що утворюється в реакції декарбоксилювання амінокислоти.
Найбільша кількість гістаміну міститься в центральній нервовій системі та тканинних базофілах сполучної тканини. Фізіологічні ефекти гістаміну пов’язані з його дією на гладенькі м’язи периферійних судин (дилатаційні ефекти), регуляцією функцій жовчного та сечового міхурів, стимулювальним впливом на секрецію соляної кислоти в шлунку, звуженням бронхів, нейротрансмітерною функцією, участю в імунологічних реакціях. Надлишкове накопичення гістаміну в зонах запалення та ділянках взаємодії антиген-антитіло є одним із патогенетичних механізмів розвитку алергічних та анафілактичних реакцій.
Молекулярні механізми дії гістаміну на чутливі клітини реалізуються через мембранні Н1- та Н2-рецептори:
Н1-рецептори спряжені із функціонуванням фосфоінозитидного циклу, вивільненням цитозольного Са2+, активацією гуанілатциклази та накопиченням цГМФ;
Н2-рецептори спряжені з активацією аденілатциклази та накопиченням цАМФ.
Фармакологічні препарати, що є антагоністами гістамінових рецепторів:
антагоністи Н1-рецепторів — застосовуються при алергічних станах різного генезу, бронхіальній астмі (Димедрол, Тавегіл, Кларитин, Кетотифен);
антагоністи Н2-рецепторів — застосовуються для зменшення секреції соляної кислоти при виразковій хворобі (Ранітидин, Фамотидин).