Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ V. ГОРМОНИ В СИСТЕМІ МІЖКЛІТИННОЇ ІНТЕГРАЦІЇ ФУНКЦІЙ ОРГАНІЗМУ
ГЛАВА 25. ГОРМОНАЛЬНА РЕГУЛЯЦІЯ МЕТАБОЛІЗМУ ТА БІОЛОГІЧНИХ ФУНКЦІЙ КЛІТИНИ. III. ГОРМОНИ ТА ІНШІ БІОРЕГУЛЯТОРИ ЛІПІДНОГО ПОХОДЖЕННЯ
25.2. СТЕРОЇДНІ ГОРМОНИ КОРИ НАДНИРНИКОВИХ ЗАЛОЗ
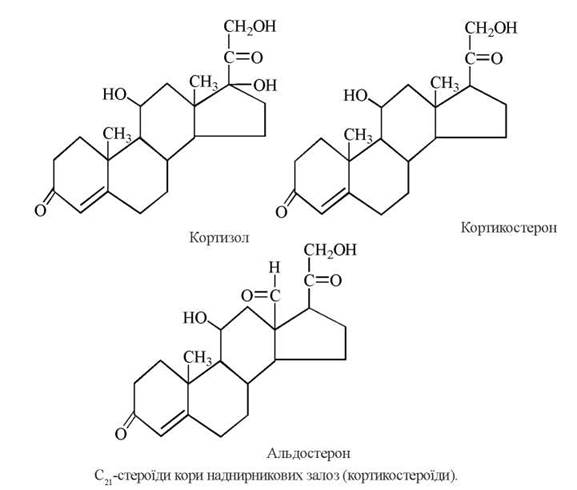
Стероїдні гормони кори наднирникових залоз — кортикостероїди — належать до С21-стероїдів.
У корі наднирникових залоз людини синтезується близько 30 стероїдів із різними рівнями фізіологічної активності. «Справжніми» стероїдними гормонами кори наднирникових залоз (тобто такими, що синтезуються в кров та впливають на чутливі периферійні тканини) є кортизол (гідрокортизон), кортикостерон та альдостерон.
Усі три гормони мають як глюкокортикоїдну, так і мінералокортикоїдну активність, проте виражену в різній мірі: кортизол є переважно глюкокортикоїдом, альдостерон — переважно мінералокортикоїдом, кортикостерону властиві обидва типи активності, але в меншому ступені, ніж у кортизолу та альдостерону, відповідно.
Біосинтез кортикостероїдів відбувається в клітинах надниркових залоз із загального для всіх стероїдних гормонів попередника — С27-Δ5-стероїду холестерину, який надходить в стероїдогенні клітини з кров’ю з печінки або синтезується in situ з ацетил-КоА.
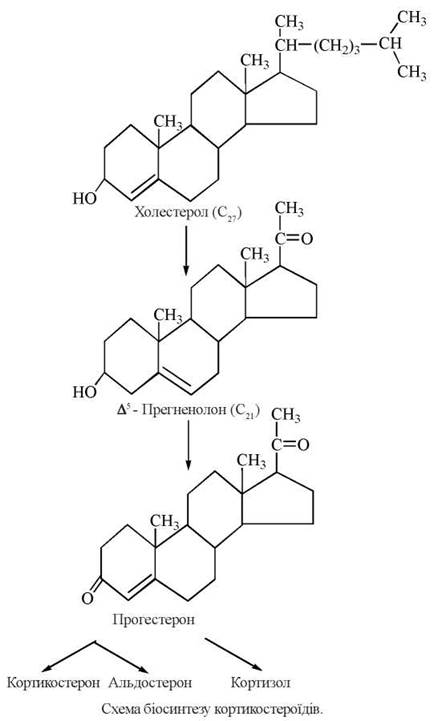
Ключовими етапами в синтезі кортикостероїдів, як і інших біологічно активних стероїдів, що проходять стадії утворення прегненолону та прогестагенів, є:
- вивільнення холестеролу з цитозольних ліпідних крапель та надходження в мітохондрії, де відбувається його біотрансформація;
- скорочення бічного ланцюга холестеролу на шість вуглецевих атомів (перетворення С27 —► С21) з утворенням С21-Δ5-стероїду прегненолону;
- перетворення прегненолону (шляхом реакцій окислення та ізомеризації) на Δ4-3-кетостероїд прогестерон;
- перетворення прогестерону на глюкокортикоїди та мінералокортикоїди (за рахунок реакцій гідроксилювання стероїдів цитохром-Р-450-залежними оксигеназами мішаної функції).
Біосинтез певних представників стероїдних гормонів відбувається в різних зонах кори наднирникових залоз: в зовнішній, клубочковій зоні синтезуються альдостерон та кортикостерон; в середній, пучковій зоні — кортизол та кортикостерон; у внутрішній, сітчастій — андрогени та частково кортизол.
Біологічні властивості кортикостероїдів
Фізіологічна функція кортикостероїдних гормонів полягає в регулюванні процесів адаптації цілісного організму до змін умов навколишнього середовища та підтриманні внутрішнього гомеостазу, особливо в умовах дії стресорних факторів.
Глюкокортикоїди — кортикостероїди, основним біологічним ефектом дії яких є регуляція вуглеводного обміну, спрямована на стимуляцію синтезу глюкози в печінці, тобто глюконеогенезу. До глюкокортикоїдів належать: кортизол (гідрокортизон), кортизон (11-дегідрокортизол), кортикостерон, 11-дегідрокортикостерон. Головним (таким, що секретується в кров та найбільш активним) представником глюкокортикоїдів є кортизол.
Активація синтезу глюкози при дії кортизолу досягається за рахунок координованої дії таких біохімічних механізмів:
у печінці — активації експресії генів, які відповідають за синтез ферментів глюконеогенезу (ФЕП-карбоксикінази, амінотрансфераз — зокрема, тирозин- амінотрансферази, триптофанпіролази), що постачають субстрати — попередники в синтезі глюкози;
у м’язах — пригнічення біосинтезу білка, що призводить до збільшення концентрації вільних амінокислот, які надходять в гепатоцити, де виступають в якості субстратів глюконеогенезу; подібний катаболічний ефект кортизолу спостерігається також у лімфоїдній тканині.
Вплив кортизолу на ліпідний обмін проявляється, переважно, в контраінсулярній дії, тобто стимуляції процесів ліполізу в жировій тканині із збільшенням вмісту жирних кислот (НЕЖК) в плазмі крові; в основі такого впливу глюкокортикоїдів на обмін триацилгліцеролів лежить їх здатність збільшувати ліполітичну дію катехоламінів та соматотропіну — «пермісивний ефект глюкокортикоїдів».
Крім контролю зазначених метаболічних шляхів, кортизол та інші глюко- кортикоїди регулюють течію багатьох фізіологічних процесів в організмі, змінюючи реактивність клітин відносно інших гормонів та нейромедіаторів. Особливо важливими є ефекти глюкокортикоїдів (разом з ефектами катехоламінів), спрямовані на мобілізацію захисних реакцій організму в умовах стресу, зокрема при хірургічних втручаннях, травмах, інфекціях. У високих фармакологічних дозах глюкокортикоїди та їх синтетичні похідні мають виражені протизапальні властивості, пов’язані з гальмуванням фосфоліпази А2, необхідної для вивільнення арахідонової кислоти — попередника в синтезі простагландинів (див. нижче); цей протизапальний ефект сполук із властивостями глюкокортикоїдів знайшов широке застосування в клінічній практиці (препарати Преднізолон, Дексаметазон, Тріамсинолон тощо).
Регуляція синтезу та секреції кортизону нг/мл
Біохімічним сигналом, що стимулює синтез та надходження в кров кортизолу, є зменшення концентрації в крові глюкози. Гіпоглікемія спричиняє включення процесів кортизолзалежного глюконеогенезу через чутливі структури гіпоталамуса, що секретують кортиколіберин (кортикотропін-рилізинг-гормон), який, у свою чергу, активує виділення кортикотропіну (АКТГ) і, відповідно, утворення в корі наднирникових залоз кортизолу.
Добова секреція в організмі людини кортизолу та гіпофізарного кортикотропіну має ритмічний характер із максимумом у ранкові години, тобто в постабсорбтивний період вичерпання внутрішніх резервів глюкози: найбільше зростання рівня АКТГ у сироватці крові спостерігається о 6-й-8-й годині ранку, дещо передуючи росту кортизолу (рис. 25.2)
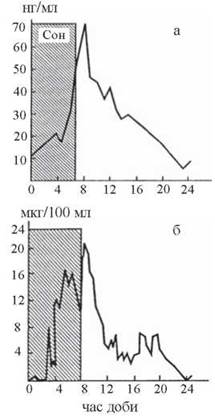
Рис. 25.2. Добовий ритм секреції АКТГ (а) та кортизолу (б) (за М.І. Балаболкіним, 1998).
Хвороба Іценко-Кушинга — патологічний стан, який характеризується аномальним збільшенням продукції в організмі людини глюкортикоїдів, зокрема кортизолу. Ця патологія виникає внаслідок наявності гормонопродукуючої пухлини наднирникових залоз або гіпофіза (із відповідним збільшенням секреції кортикотропіну). Головними проявами захворювання є зменшення толерантності до глюкози, наявність стійкої гіперглікемії та глюкозурії, навіть у постабсорбтивному стані, тобто через декілька годин після останнього прийому їжі, порушення жирового обміну; оскільки для природних глюкокортикоїдів властиві також мінералокортикоїдні ефекти (див. нижче), при хворобі Іценко-Кушинга розвиваються затримка в організмі Na+ і важка гіпертензія.
Мінералокортикоїди — кортикостероїди, біологічна дія яких полягає в регуляції водно-сольового обміну в тканинах: мінералокортикоїди спричиняють затримку в організмі іонів Na+ та виведення К+ і Н+. Мінералокортикоїдну активність мають такі стероїди, що синтезуються в наднирникових залозах: альдостерон, 18-оксикортикостерон, 11-дезоксикортикостерон (ДОК) та деякі інші сполуки. Серед них найбільш активний альдостерон (єдиний мінералокортикоїд, що секретується в кров), мінералокортикоїдний ефект якого перевищує дію інших стероїдів приблизно в 100 разів.
Альдостерон — основний мінералокортикоїд, який синтезується в клітинах клубочкової зони кори наднирникових залоз; головний біохімічний ефект дії альдостерону полягає в стимуляції реабсорбції Na+ (а разом з ним і Cl-) в дистальній частині канальців нефронів.
Молекулярні механізми дії альдостерону, як і інших стероїдних гормонів, полягають у взаємодії в цитозолі клітин-мішеней із специфічним рецептором, що в комплексі з мінералокортикоїдом переноситься в ядро клітини; активований альдостероном рецептор спричиняє активацію генів, що необхідні для синтезу білків, які реалізують транспорт Na+ через апікальну та базальну мембрани чутливих клітин нефронів.
Альдостеронізм
У нормі клубочкова зона кори наднирникових залоз продукує 60-90 мкг альдостерону на добу. Стан збільшення концентрації гормону внаслідок підвищеного його утворення в корі наднирникових залоз або зменшення швидкості катаболізму гормону в печінці при порушенні функції гепатоцитів (наприклад, при цирозі печінки) отримав назву синдрому альдостеронізму; патологія проявляється гіпертензією та розвитком набряків внаслідок збільшеної затримки в організмі іонів натрію та води. Первинний альдостеронізм (синдром Кона) — захворювання, спричинене аденомою кори наднирникових залоз, що секретується в системі ренін-ангіотензин.
Система ренін-ангіотензин — система вазоактивних пептидів, яка є регулятором артеріального тиску та водно-електролітного обміну в організмі людини. Основним компонентом системи є октапептид ангіотензин II, що утворюється шляхом ступеневого обмеженого протеолізу з білка α2-глобулінової фракції сироватки крові — ангіотензиногену:
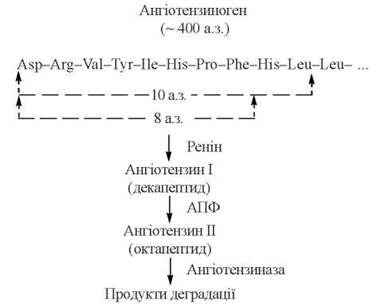
При дії протеолітичного ферменту реніну, який синтезується в юкстагломерулярних клітинах аферентних артеріол нефронів, відбувається відщеплення від ангіотензиногену декапептиду ангіотензину I, який, e свою чергу (за дії протеїнази ангіотензинперетворюючого ферменту, АПФ), перетворюється на судинозвужувальний пептид ангіотензин II. Фізіологічним стимулом для продукування реніну і запуску протеолітичного каскаду утворення ангіотензину II є зниження артеріального тиску.
Ангіотензин II є найбільш потужним судинозвужувальним фактором; його біологічні ефекти реалізуються також за рахунок стимуляції секреції альдостерону та вазопресину (антидіуретичного гормону), що в цілому призводить до затримки в організмі іонів Na+ та води. Інгібітори ангіотензинперетворюючого ферменту спричиняють зниження артеріального тиску і мають діуретичну (і натрійуретичну) фармакологічну дію; ці сполуки — інгібітори АПФ — застосовують як ефективні засоби для терапії гіпертонічної хвороби (препарати Каптоприл, Еналаприл тощо).
Натрійуретична система
Фізіологічним антагоністом альдостерону та ангіотензину II є натрійуретична система, що складається з пептидів, які синтезуються, переважно, в міокарді (міоцитах передсердя) та головному мозку. Натрійуретичний фактор (гормон), що продукується в передсерді, — це пептид (126 амінокислотних залишків), який має натрійуретичні, діуретичні та калійуретичні властивості; при дії протеаз крові та тканин вихідний пептид (прогормон) розщеплюється на окремі пептиди із зазначеними активностями. Натрійуретичні пептиди виявлені (хоча і в значно менших концентраціях) також у наднирникових залозах, нирках, матці.