Биотехнология - Ю.О. Сазыкин 2006
Общая биотехнология
Молекулярные механизмы внутриклеточной регуляции и их использование в биотехнологическом производстве
Индукция и репрессия синтеза ферментов
В соответствии со своей специализацией любая клетка (микробная, растительная, животная) поддерживает гомеостаз и совершает свой цикл развития, обслуживая те или иные потребности многоклеточного организма. Биотехнолог, преследуя задачу максимальной наработки целевого продукта, воздействует на эти процессы в соответствии с интересами производства. Современное биотехнологическое производство лекарственных средств наряду с совершенствованием продуцента требует и постоянной оптимизации условий самого процесса ферментации.
Известно, что микробная клетка как продуцент лекарственных веществ содержит несколько тысяч ферментов и часто используется как основа создания продуцентов-рекомбинантов.
Значительную часть ферментов микробной клетки составляют конститутивные ферменты, которые всегда присутствуют в ней в строго определенной концентрации, характерной для каждого отдельного фермента, например фермента гликолиза. Однако эволюция жизни на Земле и необходимость приспособления организмов (микроорганизмов) к разнообразным и часто меняющимся условиям внешней среды привели к возникновению так называемых адаптивных или индуцибельных ферментов. Гены, кодирующие такого рода ферментные белки, экспрессируются лишь когда в среде появляется относительно редкий субстрат, который может быть использован как источник энергии. Индуцибельные ферменты довольно часто образуются в клетке при появлении в среде антимикробных веществ, структура которых может подвергаться ферментативной инактивации.
Индукция фермента — резкое увеличение скорости его синтеза (в миллионы раз за несколько секунд) в ответ на появление индуктора.
Схематически механизм индукции может быть представлен, исходя из предложенной в 1960-х гг. Ф, Жакобом и Ж. Моно концепции регуляции индукции и репрессии синтеза ферментов (рис. 7). Одновременно авторами концепции была разработана и «модель оперона», в соответствии с которой в систему регуляции синтеза ферментов на генетическом уровне входит несколько компонентов. Первым следует назвать структурный ген, кодирующий структуру ферментного белка; иногда это могут быть несколько последовательно расположенных структурных генов, которые кодируют участвующие в общем метаболическом процессе ферменты.
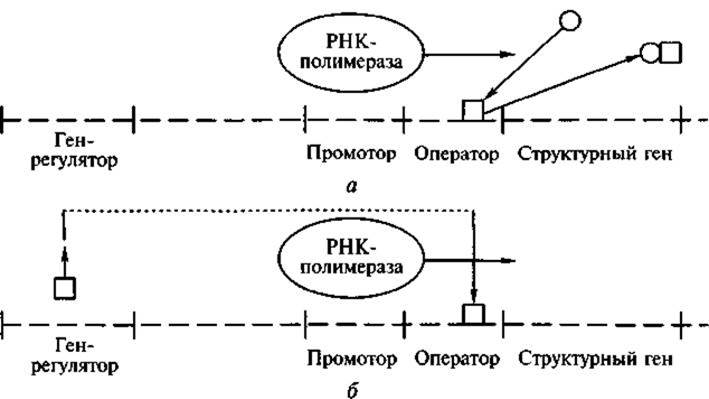
Рис. 7. Схема индукции (а) и репрессии (б) фермента:
![]()
В опероне структурному гену предшествует участок ДНК, именуемый оператором, который контролирует работу структурных генов. Именно с этим участком связывается белок-репрессор, структуру которого определяет ген-регулятор, который локализован вне оперона и может находиться даже в другой хромосоме, например, если это — клетка эукариота. Принципиально важно, что оператор располагается между участком, именуемым промотором и структурным геном. Молекула РНК-полимеразы «садится» на промогорный участок, чтобы затем двигаться по структурному гену, транскрибируя его последовательность в информационную РНК. Последняя служит в рибосомной системе матрицей для конкретного белка.
Если на операторном участке находится белок-репрессор, движение РНК-полимеразы тормозится и структурный ген (или последовательно расположенные структурные гены) не считывается. Возникает явление репрессии.
Для того чтобы репрессия сменилась индукцией, белок-репрессор должен быть убран с операторного участка. Тогда РНК- полимераза получает возможность двигаться с промотора через этот участок, а затем — по структурному гену (или нескольким структурным генам).
Удаление репрессора осуществляется инактивацией репрессора индуктором. Вместе с тем индукцию можно рассматривать и как предотвращение связывания репрессора с оператором.
В целом механизмы индукции и репрессии синтеза ферментов сложны и разнообразны. Важно, что использование механизмов индукции и репрессии синтеза ферментов помогает биотехнологам в решении самых разных задач, например, позволяет поддерживать оптимальный уровень ферментных систем клетки, включенных в биосинтез целевого продукта и корректировать его в течение всего цикла ферментации.
Представляет интерес конструирование продуцентов-рекомбинантов, активность которых повышается за счет использования явления индукции. Например, в геноме микроорганизма — кишечной палочки создается оперон с общим промотором и операторным участком для двух структурных генов: гена индуцибельной бетагалактозидазы и расположенного за ним гена цепи А или цепи В человеческого инсулина. Продуцент-рекомбинант культивируется на ферментационной среде с лактозой, утилизация которой требует быстрого синтеза бетагалактозидазы. Образующаяся (быстро и в большом количестве) аминокислотная последовательность вначале соответствует бетагалактозидазе, а затем цепи А (или В) инсулина. После выделения этого гибридного белка фрагмент инсулина отделяют от фермента и используют для построения полной молекулы гормона.