Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Состав живой материи: биомолекулы
Биомолекулы имеют специфическую форму и определенные размеры
Четыре ковалентные одинарные связи, образуемые атомом углерода, располагаются в пространстве в виде тетраэдра, причем угол между любыми двумя из этих связей составляет около 109,5° (рис. 3-4). В молекулах различных органических соединений этот угол у разных атомов углерода несколько изменяется. Благодаря такому свойству углеродсодержащие соединения образуют разнообразные трехмерные структуры. Никакой другой химический элемент не может образовывать молекулы, столь различные по размерам и форме, а также по строению боковых цепей и функциональных групп. Необычайная сложность внутриклеточных структур в значительной мере отражает разнообразие размеров и форм органических молекул, из которых они построены.
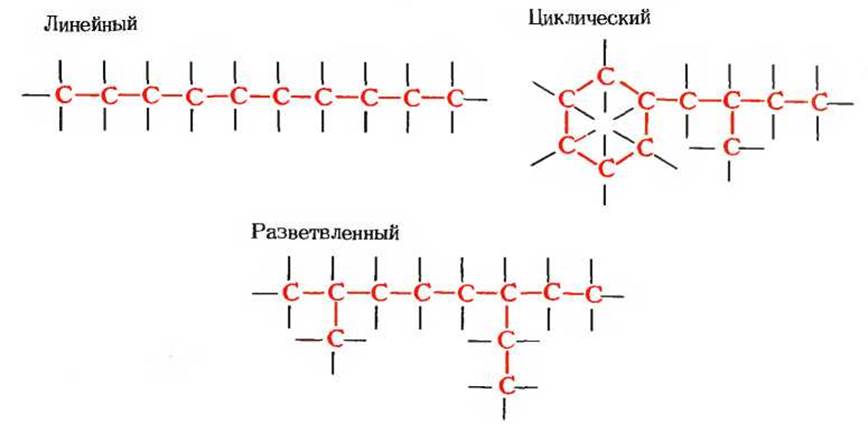
Рис. 3-3. Углерод-углеродные связи образуют каркас молекул многих органических веществ.

Рис. 3-4. А. Четыре одинарные связи, образуемые атомом углерода, расположены в пространстве в виде характерного тетраэдра; длина связей составляет приблизительно 0,154 нм, а угол между ними - 109,5° Б. Вокруг одинарных углерод-углеродных связей возможна полная свобода вращения: это отчетливо видно на примере молекулы этана (Н3С—СН3), структуру которого можно изобразить разными схемами. В. Двойные углерод-углеродные связи короче, чем одинарные, и свободное вращение вокруг них не возможно. Угол между одинарными связями, образуемыми каждым из атомов углерода, соединенных между собой двойной связью, составляет 120°. Оба атома углерода, образующие двойную связь, и атомы, обозначенные А, В, X и Y, лежат в одной плоскости.
Второе важное свойство органических соединений заключается в том, что составные части их молекул могут абсолютно свободно вращаться вокруг одинарных углерод-углеродных связей, если только к атомам углерода, участвующим в образовании таких связей, не присоединены очень большие или сильно заряженные группы; в этом случае вращение может быть ограничено. Благодаря такому свойству органические молекулы с большим числом одинарных связей могут принимать различные формы, называемые конформациями (рис. 3-4), в зависимости от угла поворота этих связей.
Третье важное свойство ковалентных связей, образуемых углеродом, заключается в том, что они характеризуются определенной длиной. В среднем длина одинарных углерод-углеродных связей равна 0,154 нм (или 1,54 А, если использовать более старую единицу длины, применявшуюся ранее в структурной химии); двойные связи короче, их длина составляет примерно 0,134 нм. В отличие от одинарных двойные углерод-углеродные связи обладают большей жесткостью и не допускают свободного вращения. При наличии в молекуле двойной связи углы между одинарными связями увеличиваются (рис. 3-4). Углы между связями и длины связей (от центра одного атома до центра другого) лучше всего можно показать с помощью моделей из шариков и стержней, тогда как внешние контуры органических молекул хорошо видны на пространственных моделях (рис. 3-5), составные части которых пропорциональны по размерам радиусам атомов (табл. 3-3). Из рассмотренных здесь данных следует, что органические биомолекулы имеют характерные размеры и трехмерную структуру, определяемые строением их скелета и расположением боковых групп.
Таблица 3-3. Радиусы некоторых атомов
Приведенные данные относятся к вандерваальсовым радиусам, характеризующим истинные размеры атомов в пpостранстве; однако, когда атомы соединяются между собой ковалентными связями, их радиусы в точке взаимодействия с другими атомами уменьшаются из-за притяжения атомов друг к другу за счет образования обобщенной пары (молекулярной орбитали)

Трехмерная структура (конформация) органических биомолекул играет исключительно важную роль во многих биохимических процессах, в частности при взаимодействии каталитических центров ферментов с субстратами (рис. 3-6). Для обеспечения нормальных биологических функций молекулы фермента и субстрата должны быть комплементарными, т.е. их структуры должны стерически точно соответствовать друг другу. Такая же строгая комплементарность необходима для связывания молекулы гормона с его рецептором на поверхности клетки, для репликации ДНК и многих других протекающих в клетке процессов. Поэтому изучение трехмерной структуры биомолекул при помощи точных физических методов составляет важную часть современных исследований, направленных на выяснение связи между структурой клеток и их биохимическими функциями.
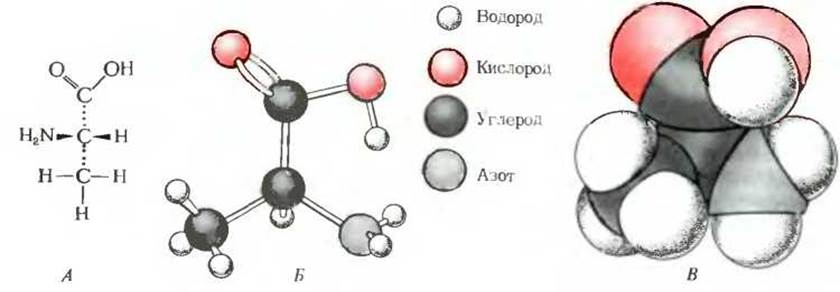
Рис. 3-5. Модели, показывающие строение аминокислоты аланина. А. Перспективное изображение структурной формулы. Б. Модель из шариков и стержней, на которой хорошо видны относительные длины связей и углы между ними. Шарики показывают приблизительные размеры атомных ядер. В. Пространственная модель. Здесь относительные размеры всех атомов точно соответствуют их вандерваальсовым радиусам (см. также табл. 3-3).

Рис. 3-6. Комплементарное соответствие молекулы субстрата активному, или каталитическому, центру молекулы фермента. Каталитический центр распознает лишь те молекулы, пространственные характеристики и размеры которых в точности соответствуют его строению.