Основы биохимии Том 2 - А. Ленинджер 1985
Биоэнергетика и метаболизм
Перенос электронов, окислительное фосфорилирование и регуляция синтеза АТР
NАDH-дегидрогеназа принимает электроны от NADH
На следующей стадии переноса электронов (рис. 17-5) пара восстановительных эквивалентов переносится от NADH к NADH-дегидрогеназе, находящейся во внутренней митохондриальной мембране. В этой реакции прочно связанная простетическая группа NADH-дегидрогеназы восстанавливается (рис. 17-8). Роль простетической группы NADH-дегидрогеназы играет фливинмононуклеотид (FMN), в состав которого входит молекула витамина В2, или рибофлавина (разд. 10.5). NADH-дегидрогеназа принадлежит к классу флавинзависимых дегидрогеназ, или флавопротеинов. В результате переноса двух восстановительных эквивалентов от NADH на NADH-дегидрогеназу (обозначена здесь E-FMN) простетическая группа фермента FMN восстанавливается в FMNH2:
![]()
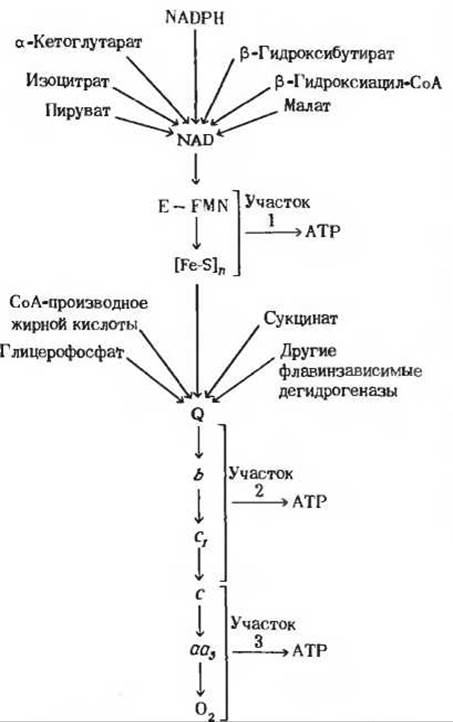
Рис. 17-7. Коллекторная функция NAD и убихинона (Q). NAD собирает восстановительные эквиваленты от многих NAD-зависимых субстратов, а также от NADPH. Убихинон собирает восстановительные эквиваленты от NADH-дегидрогеназы и от различных субстратов, на которые действуют другие флавинзависимые дегидрогеназы. Пары восстановительных эквивалентов, поставляемые большинством флавин-зависимых дегидрогеназ, не проходят через первый пункт фосфорилирования, и поэтому за счет их энергии образуются только две молекулы АТР.
В молекуле NADH-дегидрогеназы присутствует помимо флавиннуклеотидной простетической группы еще несколько атомов негемового железа. Эти атомы собраны в несколько групп, в которых они объединены с равным числом атомов кислотолабильной серы. Такие группы носят название железо-серных центров (рис. 17-9). Напомним, что железо-серные центры имеются также и в молекуле сукцинитдегидрогеназы (разд. 16.5,е). В [Fe(II)-Fe(III)]-циклax, связанных с изменением валентности, атомы железа железо-серных центров передают восстановительные эквиваленты от восстановленной простетической группы NADH-дегидрогеназы (FMNH2) на следующий переносчик в дыхательной цепи, убихинон. Таким образом, этот комплекс, состоящий из NADH-дегидрогеназы и белков, содержащих железо и серу (его называют NADH: убихинон - оксидоредуктазой), включает электронпереносящие структуры двух типов: FMN и несколько железо-серных центров, которые действуют, очевидно, последовательно.
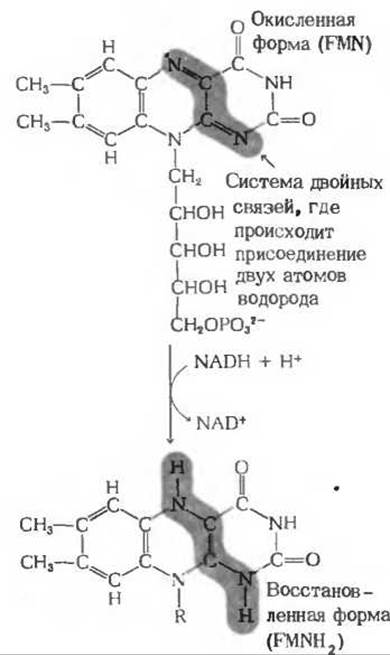
Рис. 17-8. Перенос восстановительных эквивалентов от NADH на флавинмононуклеотид (FMN)-простетическую группу NADH-дегидрогеназы. R означает здесь пятиуглеродную фосфорилированную боковую цепь.
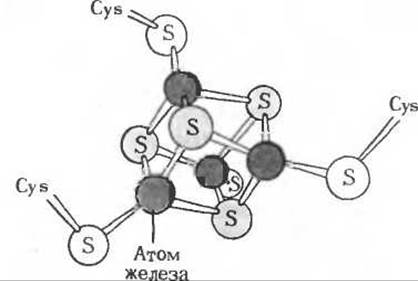
Рис. 17-9. Постулированное расположение атомов железа (красные кружки) и атомов серы (серые кружки) в железо-серных центрах. Число атомов железа и атомов кислотолабильной серы в этих центрах всегда одинаково, но есть центры, в которых содержатся только два атома железа, и есть такие, где их четыре.
Здесь представлен железо-серный центр, содержащий четыре атома железа. Атомы серы на периферии принадлежат четырем остаткам цистеина в полипептидной цепи фермента.