Биохимия аминокислот - А. Майстер 1961
Общая биохимия и физиология аминокислотного обмена
Окислительное дезаминирование
Введение
Дезаминирование аминокислот с образованием соответствующих а-кетокислот было впервые обнаружено Нейбауером [110] и Кноопом [111]. Оно осуществляется посредством двух основных общих механизмов — переаминирования (стр. 208) и окислительного дезаминирования. Окислительное дезаминирование аминокислот было впервые обстоятельно изучено Кребсом [112—114]. Он установил, что препараты печени и почек катализируют окисление как D-, так и L-изомеров аминокислот.
Фермент, катализирующий окисление D-аминокислот, был отделен от ферментной системы, осуществляющей окисление L-аминокислот. В ряде более поздних исследований присутствие в почках и печени оксидазы D-аминокислот было подтверждено. Окислительное дезаминирование L-аминокислот, о котором сообщал Кребс, объясняется, вероятно, сочетанным действием транс-аминаз и дегидрогеназы глутаминовой кислоты (стр. 234). Получен, однако, ряд препаратов оксидаз L-аминокислот, и в существовании подобных ферментов едва ли можно сомневаться.
Реакцию окисления L- и D-изомеров аминокислот соответствующими оксидазами можно выразить следующим образом:
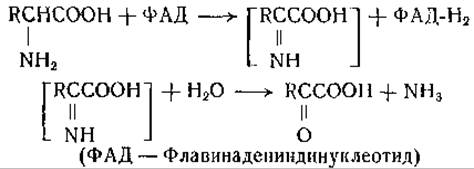
Основные изученные до сих пор D- и L-аминокислотные оксидазы общего действия оказались флавопротеинами [115—119]. При действии этих оксидаз от молекулы аминокислоты отнимается два атома водорода и образуется перекись водорода, как показано ниже:
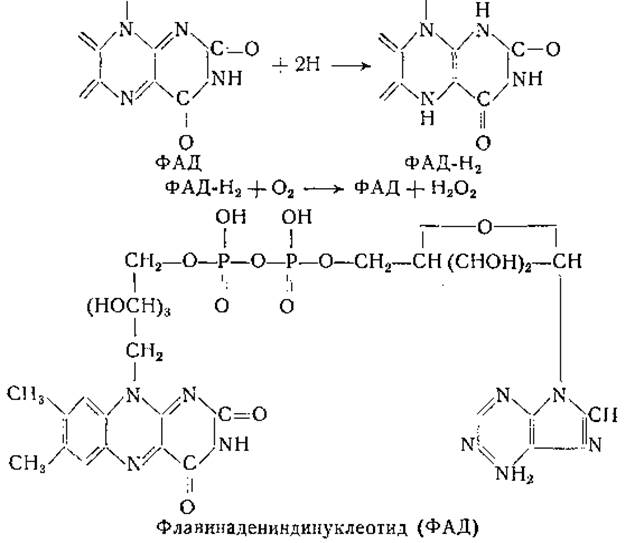
Образование иминокислоты, взятой в квадратные скобки в приведенном выше уравнении, до сих пор не установлено. Принято считать, что гидролиз гипотетической иминокислоты происходит самопроизвольно. В отсутствие каталазы при ферментативном окислении аминокислоты наблюдается образование гомологичной ей низшей карбоновой кислоты и углекислоты:
![]()
Как известно, перекись водорода вступает с а-кетокислотами в следующую неферментативную реакцию:
![]()
В присутствии каталазы перекись водорода разрушается; в этом случае реакция окислительного дезаминирования аминокислоты протекает по суммарному уравнению
![]()
При наличии в системе каталазы перекись водорода, возникающая при окислении аминокислот, может также окислять этиловый спирт [120]:
![]()
Эта реакция может служить типичным примером разнообразных пероксидазных реакций, катализируемых каталазой.