Биохимия - Химические реакции в живой клетке Том 3 - Д. Мецлер 1980
Свет в биологии
Фотосинтез
Специфическая адаптация
Первым продуктом включения СО2 в цикле Кальвина является 3-фосфоглицериновая кислота (гл. 11, разд. Г, 2). Именно быстрый переход радиоактивной метки из 14СО2 в фосфоглицерат и другие С3-соединеиия позволил Кальвину и его коллегам построить схему этого сложного цикла в том виде, в каком она представлена на рис. 11-4, Зеленые водоросли (с которыми работал Кяльвин), шпинат и другие культурные растения часто называют С3-растениями. Другая группа растений, большей частью тропические виды, способные к исключительно быстрому росту (в частности, сахарный тростник, кукуруза и ползучие сорняки), ведет себя иначе [123—127]. Радиоактивный СО2 включается сначала в С4-соединения — оксалоацетат, малат и аспартат. С4-растения характеризуются высокой эффективностью фотосинтеза, чем и объясняются быстрый рост ползучего сорняка и высокие урожаи кукурузы. Максимальная скорость включения СО2 у этих растений может достигать 40—60 мг СO2 на квадратный дециметр поверхности листа в час (~0,3 ммоль СО2 на м-2∙с-1, или ~0,10 моль СО2 на 1 моль суммарного хлорофилла в 1 с), что вдвое выше, чем для большей части сельскохозяйственных растений.
а. Низкая скорость фотодыхания С4-растений
Как и все другие организмы, растения дышат, причем при освещении С3-растений скорость потребления ими кислорода сильно возрастает. Она может составлять на свету (фотодыхание) 50% от скорости фотосинтеза и не позволяет растениям достичь максимальной эффективности фотосинтеза. Понимание этих процессов и контроль над ними составляют одну из важнейших сельскохозяйственных проблем. В частности, обсуждались такие возможности, как выведение сортов растений с низкой скоростью фотодыхания или подавленным синтезом гликолата [126, 127].
Скорость фотодыхания довольно трудно измерить. Поэтому в литературе часто оперируют другой величиной — точкой СО2-компенсации1), понимая под этим такую концентрацию СО2 (при заданной постоянной интенсивности света), при которой ассимиляция СО2 в ходе фотосинтеза уравновешивается дыханием. Воздух содержит ~0,03% (или 300 млн-1) СО2. Для обычных сельскохозяйственных С3-растений точка СО2-компенсации составляет ~40—60 млн-1 при 25 °С. Для С4-растений эта точка намного ниже, иногда менее 10 млн-1. Роль данного различия особенно велика при сильном освещении, поскольку при этом содержание СО2 в воздухе над полем растущих растений заметно падает. Точка СО2-компенсации в жаркие дни повышается, в результате у С3-растений в отличие от С4-растений сильно понижается эффективность фотосинтеза.
б. Связь фотодыхания с метаболизмом гликолевой кислоты
Двухуглеродная гликолевая кислота образуется в больших количествах в хлоропластах С3-растений и далее поступает в цитозоль [128]. Одним из источников гликолата, вероятно, служит фосфогликолат, образование которого катализируется рибулозодифосфат-карбоксилазой хлоропластов [уравнение (7-28)]. Гликолевая кислота образуется в результате конкуренции О2 за центр связывания СО2 на ферменте (отсюда легко понять, почему повышение содержания О2 в воздухе повышает точку СО2-компенсации растения). Вторым источником гликолата служит реакция с участием транскетолазы, в результате которой в качестве побочного продукта образуется гликольальдегид [уравнение (8-15)]. Гликольальдегид далее легко окисляется в гликолат. Могут существовать и другие источники гликолата.
1) Точка световой компенсация определяется как интенсивность света, при которой скорость дыхания и скорость потребления СО2 в процессе фотосинтеза равны.
Метаболизм гликолата характеризуется высокой скоростью, но протекает он не в хлоропластах, а в пероксисомах (микротельцах; гл. 1, разд. Б, 6). Здесь имеется флавинсодержащая оксидаза, превращающая гликолат в глиоксилат с образованием Н2О2 (рис. 13-25) [129].

РИС. 13-25. Образование гликолата в хлоропластах и некоторые пути его метаболизма в пероксисомах и митохондриях [120].
Часть образовавшейся перекиси водорода неферментативным путем декарбоксилирует глиоксилат (при этом образуются формиат и СО2), но основная ее часть, вероятно, разрушается в пероксисомах под действием пероксидаз или каталазы (последний фермент, как это ни странно, отсутствует в хлоропластах — видимо, в этом состоит одна из причин, почему окисление гликолата происходит именно в микротельцах). Из глиоксилата в результате переаминирования образуется глицин, который может подвергаться декарбоксилированию в митохондриях (рис. 14-32). Он может также превращаться в серин, часть которого снова попадает в пероксисомы и окисляется в оксипировиноградную и далее в глицериновую кислоту (рис. 13-25). Последняя может быть далее использована для синтеза глюкозы. В итоге происходит интенсивная стимуляция метаболизма, приводящего к освобождению СО2; по-видимому, именно к этим процессам сводится индуцированное светом дыхание растений (хотя до конца этот вопрос далеко не ясен).
в. С4-цикл, приводящий к повышению концентрации двуокиси углерода
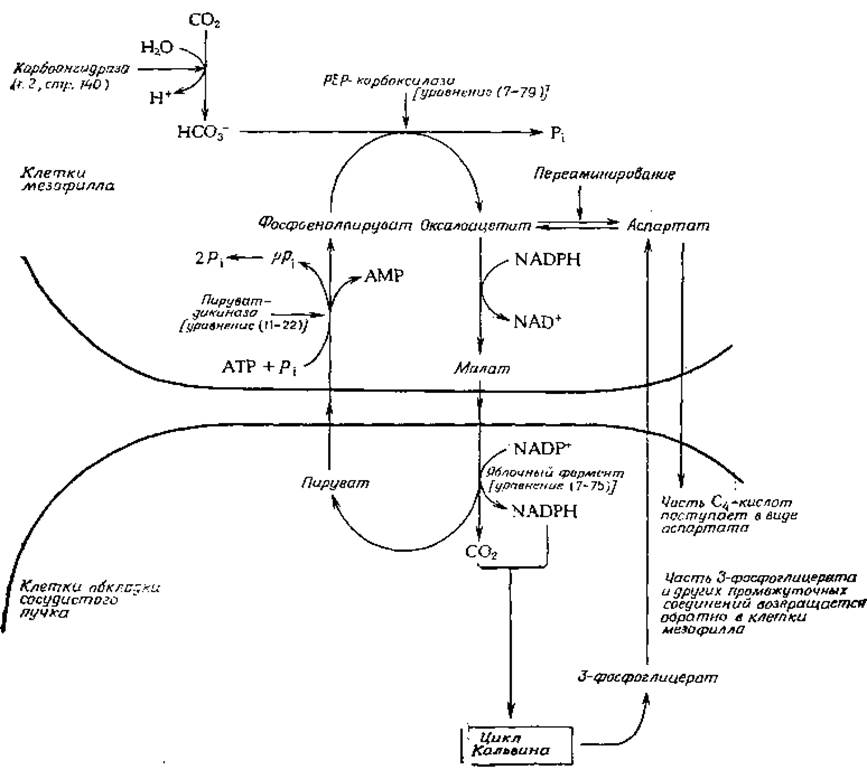
РИС. 13-26. С4-цикл повышения концентрации СО2 в С4-растениях.
Каким образом снижается интенсивность фотодыхания С4-растений? Данные о включении СО2 в оксалоадетат привели вначале к предположению о существовании альтернативного циклу Кальвина процесса восстановления СО2, однако дальнейшие исследования показали, что «секрет» С4-растений лежит в наличии у них механизма повышения концентрации СО2, ослабляющем конкуренцию со стороны О2. Все виды С4-растений имеют характерную внутреннюю анатомию листа: сосудистые пучки охватывает одиночный плотный слой темно-зеленых клеток, а вокруг этой обкладки располагается рыхлый слой клеток мезофилла (так называемая анатомия «krаnz»-типа). Для С4-растений характерно пространственное разделение химических реакций между мезофиллом и клетками обкладки. Включение СО2 (точнее, бикарбонат-иона) в оксалоацетат происходит в мезофилле и осуществляется в основном с помощью РЕР-карбоксилазы (рис. 13-26). Оксалоацетат восстанавливается в малат при участии NADPH, образующегося под действием света. Другой путь основан на переаминировании оксало-ацетата с образованием аспартата. Далее и малат, и аспартат диффундируют, перемещаясь из клеток мезофилла в клетки обкладки. Здесь малат подвергается окислительному декарбоксилированию [под действием яблочного фермента; уравнение (7-37)] в пируват (рис. 13- 26). Аспартат тоже может превращаться в тех же клетках в оксалоацетат, малат и пируват. Отметим, что результатом всех этих превращений является транспортировка СO2 из клеток мезофилла в клетки обкладки, а также перенос двух восстанавливающих эквивалентов в форме NADPH (после действия яблочного фермента). СO2, NADPH (и еще некоторое количество NADPH, который образуется в хлоропластах клеток обкладки) используются затем в реакциях цикла Кальвина для синтеза 3-фосфоглицерата и других соединений. По имеющимся оценкам, из всех молекул СO2, используемых в клетках обкладки, 85% поступает через С4-цикл и лишь 15% — за счет прямой диффузии. Это дает клетке ряд преимуществ: создается более высокое давление СO2, уменьшается конкуренция со стороны O2 и существенно ослабляется фотодыхание.
Пируват, образующийся в клетках обкладки, в основном возвращается в клетки мезофилла и фосфорилируется при участии пируват, фосфат—дикиназы. Этот необычный фермент [уравнение (11-22)] расщепляет АТР на АМР и РРi, который в свою очередь расщепляется до Рi. В результате на возвращение каждой молекулы пирувата в цикл приходится затрачивать энергию двух высокоэнергетических связей. По этой причине считают, что циклическое фотофосфорилирование играет более важную роль в хлоропластах клеток мезофилла, чем в клетках обкладки.
г. Метаболизм у растений семейства Crassulaceae
К семейству Crassulaceae принадлежит большая группа растений, в том числе многие декоративные суккуленты, например заячья капуста (Sedum). Метаболизм у этих растений примечателен тем, что в ночное время в них синтезируется большое количество яблочной и изолимонной кислот. В течение дня, когда идут процессы фотосинтеза, эти кислоты исчезают. Еще один интересный факт: устьица листьев (гл. 1, разд. Д, 4) днем остаются закрытыми и открываются только ночью — таким путем растения приспособились обходиться малым количеством воды. Задача, стоящая перед указанными растениями, заключается в том, чтобы ночью накопить двуокись углерода, а днем включить ее в состав органических соединений путем фотосинтеза. Возможный механизм этого процесса схематически представлен на рис. 13-27. В левой части рисунка изображены реакции, идущие ночью, в ходе которых крахмал расщепляется с образованием фосфоенолпировиноградной кислоты (РЕР). Хотя это соединение можно было бы получить путем гликолиза, эксперименты с введением метки указывают, что в рассматриваемом нами случае более важную роль играют реакции пентозофосфатного пути [96]. РЕР выступает в роли акцептора СO2 и превращается э оксалоацетат, который далее восстанавливается в яблочную кислоту. Эти процессы можно изобразить в виде схемы сбалансированного брожения [рис. 13-27; уравнение (13-32)], где используется NADPH, образующийся в ходе превращения глюкозо-6-фосфата в рибулозо-5-фосфат. Днем, когда АТР и NADPH имеются в избытке в результате фотосинтеза, происходят превращения, изображенные в правой части рисунка. Первая стадия — высвобождение СO2 из яблочной кислоты под действием яблочного фермента — протекает так же, как и в С4-растениях. В данном случае она используется для высвобождения запасенного ночью СO2, который далее включается в органические соединения в цикле Кальвина. Остающийся пируват снова превращается в крахмал.
![]()
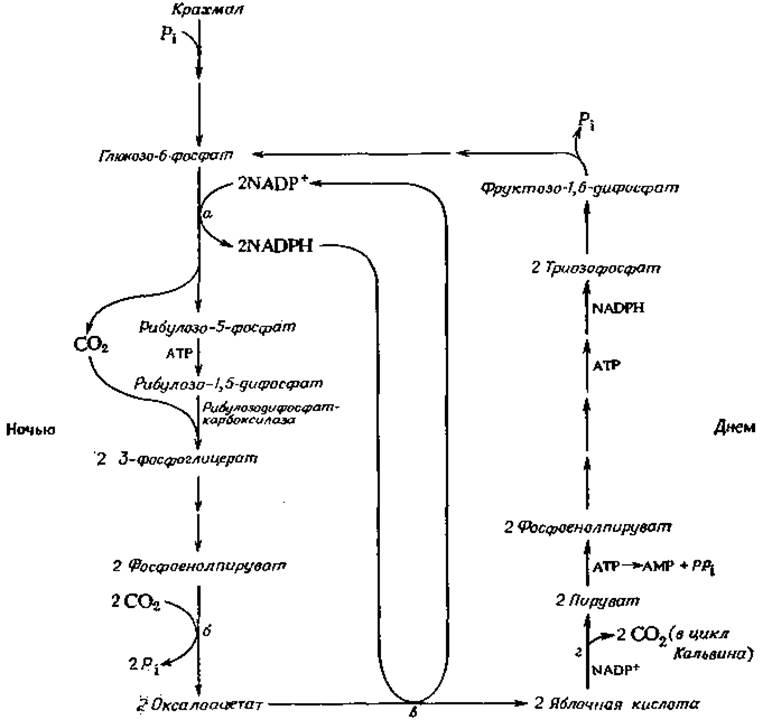
РИС. 13-27. Предполагаемая схема метаболизма органических кислот в дневное и ночное время у растений семейства Crassulaceae.
Интересно, что многие растения накапливают значительные количества малата в цитоплазме и в вакуолях. Очевидно, он служит резервным материалом, использующимся при синтезе углеводов.
д. Прямое восстановление в формиат
В конских бобах (Vicia faba) наблюдается специфическое включение метки из 14СO2 в глутамат, в положение C5, что может быть объяснено прямым восстановлением СО2 в формиат восстановленным ферредоксином [130]:
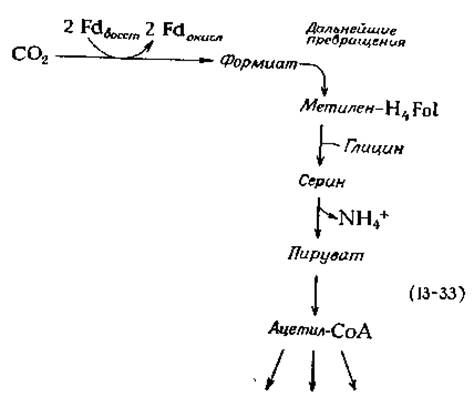
Как указано на схеме, включение метки может осуществляться с помощью глицина, образующегося из гликолата. Интересно сравнить эти реакции с циклическим процессом включения формиата, изображенным на рис. 11-5.