Химия белка. Структура, свойства, методы исследования - Шендрик А.Н. 2022
Методы экспериментального исследования структуры белков
Методы определения молекулярной массы белков
Определение молекулярной массы по давлению насыщенных паров
Из термодинамики известно, что давление насыщенных паров раствора равно сумме парциальных давлений всех компонентов раствора:
![]()
где РΣ, и рі- суммарное давление насыщенных паров и парциальные давления паров каждого из компонентов раствора.
В идеальных (предельно разбавленных растворах) величины парциальных давлений компонентов пропорциональны мольным долям каждого из них. Давление насыщенных паров полимеров (в частности, белков) при комнатных температурах крайне мало и его вкладом в РΣ можно пренебречь. Тогда, для идеального двухкомпонентного раствора белка в растворителе будем иметь:
![]()
Увеличение концентрации белка в растворе будет понижать мольную долю растворителя, и как следствие, его парциальное давление. Иными словами величина насыщенных паров над раствором будет в этом случае уменьшаться. Что и позволяет определить молекулярную массу растворенного полимера.
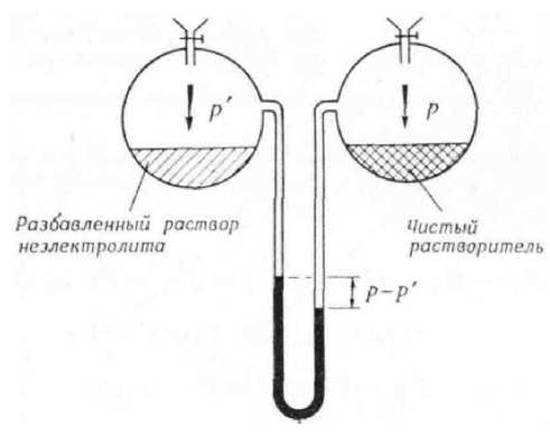
Упругость паров над поверхностью разбавленных растворов неэлектролитов и чистым растворителем можно сопоставить по величине с помощью тензиметра (см рис.). Для простоты предполагается, что давление создают лишь пары растворителя, т. е. давление паров растворенных веществ равно нулю. Установлено, что упругость паров раствора падает по мере того, как возрастает его титр (s), рассчитанный по формуле:
![]()
где m' и m— масса растворенного вещества и растворителя соответственно.
Приведенная величина понижения давления над раствором ((P - P')/P) связана с его титром и молекулярными массами растворенного вещества (М') и растворителя (М) следующим простым соотношением:
![]()
Это основное уравнение тонометрии, которое позволяет рассчитать молекулярную массу растворенного вещества. Молекулярная масса растворителя является тономентрической постоянной.
Метод тонометрии не всегда дает надежные результаты. Во-первых потому, что с увеличением концентрации растворы белков быстро отклоняются от идеальных. Во вторых, при очень больших разбавлениях трудно зафиксировать вызванные небольшими добавками белка уменьшения давления насыщенных паров над раствором.