БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ II ГЕНЕРИРОВАНИЕ И ХРАНЕНИЕ МЕТАБОЛИЧЕСКОЙ ЭНЕРГИИ
ГЛАВА 15. ПЕНТОЗОФОСФАТНЫЙ ПУТЬ И ГЛЮКОНЕОГЕНЕЗ
15.5. Скорость функционирования пентозофосфатного пути регулируется концентрацией NАDР+
Первая реакция окислительной ветви пен- тозофосфатнош пути, дегидрирование глюкозо-6-фосфата, по существу необратИма. Действительно, при физиологических условиях эта реакция лимитирует скорость процесса и выполняет функцию «контрольного пункта». Наиболее важным регуляторным фактором является концентрация NADP+, акцептора электронов при окислении глюкозо-6-фосфата в 6-фосфоглюконо- лактон. Кроме того, NADPH конкурирует с NADP+ за связывание с ферментом, и АТР конкурирует с глюкозо-6-фосфатом. Отношение концентрации NADP+ к концентрации NADPH в цитозоле печени крыс, содержащихся на полноценном рационе, составляет примерно 0,014, что на несколько порядков ниже отношения [NAD+]/[NADH], которое при этих же условиях равно 700. Выраженное действие концентрации NADP+ на скорость превращений по окислительной ветви пентозофосфатного пути подтверждает, что генерирование NADPH тесно сопряжено с его использованием в восстановительных биосинтезах. Вопрос о регуляции неокислительной ветви пентозофосфатного пути до сих пор остается открытым.
15.6. Судьба глюкозо-6-фосфата зависит от потребности в NADPH, рибозо-5-фосфате и АТР
Проследим судьбу глюкозо-6-фосфата в четырех различных ситуациях.
1. Потребность в рибозо-5-фосфате значительно превышает потребность в NADPH. Ббльшая часть глюкозо-6-фосфата превращается во фруктозо-6-фостфат и глицеральдегид-3-фосфат по гликолитическому пути. Затем две молекулы фру кто- зо-6-фосфата и одна молекула глицеральдегид-3-фосфата превращаются под действием трансальдолазы и транскетолазы в три молекулы рибозо-5-фосфата путем обращения реакции, описанной ранее. Стехиометрия этого превращения (рис. 15.2, А) следующая:
5Глюкозо-6-фосфат + 5АТР → 6Рибозо-5-фосфат + 5ADP + Н+.
Рис. 15.2. Четыре механизма пентозофосфатного пути. Названия основных продуктов закрашены
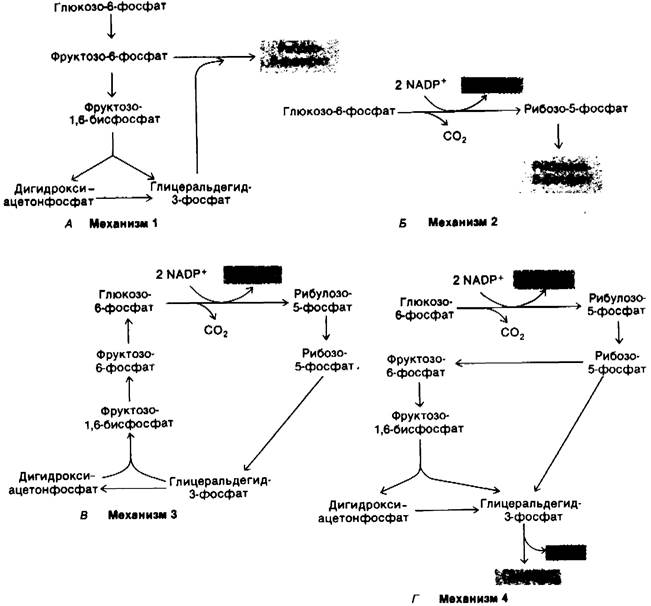
2. Потребность в NADPH и рибозо-5- фосфате сбалансирована. При таких условиях преобладающей реакцией является образование двух молекул NADРН и одной молекулы рибозо-5-фосфата из одной молекулы глюкозо-6-фосфата по окислительной ветви пентозофосфатного пути. Стехиометрия этого превращения (рис. 15.2. Б) описывается уравнением
Глюкозо-6-фосфат + 2NADP+ + Н2O → Рибозо-5-фосфат + 2NАDРН + 2Н+ + СO2. '
3. Потребность в NАDРН значительно превышает потребность в рибозо-5-фосфате; глюкозо-6-фосфат полностью окисляется в СO2. В этой ситуации активно протекают три группы реакций. Во-первых, по окислительной ветви пентозофосфатного пути образуются два NADPH и один рибозо-5-фосфат. Далее рибозо-5-фосфат превращается во фруктозо-6-фосфат и гли- церальдегид-3-фосфат под действием транскетолазы и трансальдолазы. Наконец, происходит ресинтез глюкозо-6-фосфата из фруктозо-6-фосфата и глицеральдегид-3- фосфата по пути глюконеогенеза (рассматривается ниже в этой главе). Стехиометрия указанных реакций (рис. 15.2, В) описывается следующими уравнениями:
6Глюкозо-6-фосфат + 12NADP+ + 6Н2О → 6Рибозо-5-фосфат + 12NADPH + 12Н+ + 6СО2,
6Рибозо-5-фосфат → 4Фруктозо-6-фосфат + 2Глицеральдегид-3-фосфат,
4Фруктозо-6-фосфат + 2Глицеральдегид- 3-фосфат + Н2O → 5Глюкозо-6-фосфат + Рi.
Суммируя эти реакции, получаем
Глюкозо-6-фосфат + 12NADP+ + 7Н2O → 6СO2 + 12NADPH + 12Н+ + Рi.
Таким образом, эквивалент глюкозо-6-фосфата может быть полностью окислен до СO2 с одновременным генерированием NADPH. Смысл указанных реакций состоит в том, что рибозо-5-фосфат, образовавшийся по пентозофосфатному пути, вновь превращается в глюкозо-6-фосфат под действием транскетолазы, трансальдолазы и некоторых ферментов глюконеогенеза.
4. Потребность в NADPH значительно превышает потребность в рибозо-5-фосфате: глюкозо-6-фосфат превращается в пируват. Возможен и другой путь: рибозо-5- фосфат, образовавшийся по окислительной ветви пентозофосфатного пути, превращается в пиру ват (рис. 15.2,0-Фруктозо-6-фосфат и глицеральдегид-3-фосфат, происходящие из рибозо-5-фосфата, вступают на гликолитический путь обмена, а не подвергаются обратному превращению в глюкозо-6-фосфат. Согласно изложенному механизму, происходит одновременное генерирование АТР и NADPH и пять из шести атомов углерода глюкозо-6-фосфата появляются в пирувате:
ЗГлюкозо-6-фосфат + 6NADP+ + 5NAD+ + 5Рi + 8ADP → 5Пируват + ЗСO2 + 6NADPH + 5NADH + 8АТР + 2Н2O + 8Н+.
Образовавшийся в этих реакциях пируват может окисляться с образованием дополнительного количества АТР или может быть использован в качестве строительного блока в различных биосинтетических процессах.
15.7. Активность пентозофосфатного пути в жировой ткани значительно выше, чем в мышцах
Опыты с радиоактивной меткой дают возможность измерить, сколько глюкозо-6- фосфата метаболизируется по пентозофосфатному пути и сколько по гликолитическому пути в сочетании с циклом трикарбоновых кислот. Для этого одну пробу тканевого гомогената инкубируют с глюкозой, меченной 14С при С-1, другую-с глюкозой, меченной 14С при С-6, и сравнивают радиоактивность СO2, образовавшегося в обеих пробах. Смысл эксперимента состоит в том, что по пентозофосфатному пути происходит декарбоксилиро- вание только при С-1, тогда как в ходе превращений глюкозы под действием пируват-дегидрогеназного комплекса по гликолитическому пути и далее в цикле трикарбоновых кислот декарбоксилирование при С-1 и при С-6 идет с одинаковой интенсивностью. Одинаковая степень декарбоксилирования при С-1 и С-6 в этой последней группе реакций объясняется быстрым взаимопревращением глицеральдегид- 3-фосфата и дигидроксиацетонфосфата под действием триозофосфат-изомеразы.
При таком экспериментальном подходе оказалось, что активность пентозофосфатного пути находится на чрезвычайно низком уровне в скелетной мышце, но на очень высоком в жировой ткани. Эти данные подтверждают предположение, что главная роль пентозофосфатного пути состоит в генерировании NADPH для восстановительных биосинтезов. Жировая ткань потребляет большие количества NADPH для восстановительного синтеза жирных кислот из ацетил-СоА (гл. 17).