БИОЛОГИЯ Том 3 - руководство по общей биологии - 2004
21. РАЗМНОЖЕНИЕ
21.7. Репродуктивные системы человека
21.7.4. Сперматогенез - развитие спермиев
Спермин продуцируются со скоростью примерно 120 млн. в сутки. Образование одного спермия занимает примерно 70 дней. Наружный слой стенки семенных канальцев состоит из клеток зачаткового (герминативного) эпителия, которые путем многократных делений образуют остальные шесть слоев клеток (рис. 21.36 и 21.37, А и Б). Эти слои соответствуют последовательным стадиям развития спермиев. В результате первых делений клеток зачаткового эпителия возникает множество сперматогониев, которые, увеличиваясь в размерах, образуют сперматоциты первого порядка. Эти сперматоциты, после первого мейотического деления превращаются в гаплоидные сперматоциты второго порядка, а после второго мейотического деления — в сперматиды. Между этими рядами развивающихся клеток расположены крупные клетки Сертоли, тянущиеся от наружного слоя канальца до его просвета.
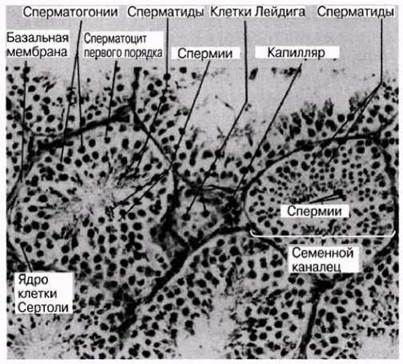
Рис. 21.36. Микрофотография среза семенника. Видны семенные канальцы и интерстициальные клетки (клетки Лейдига).
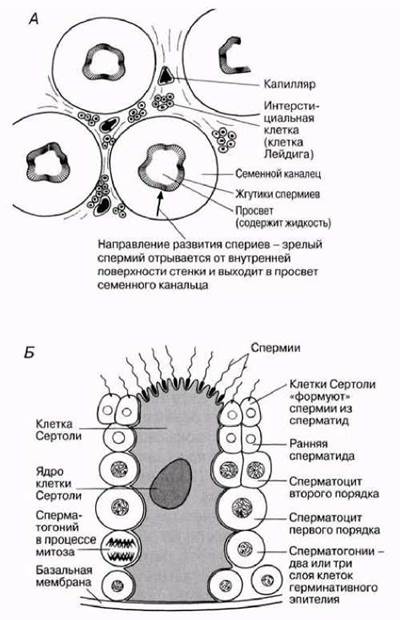
Рис. 21.37, А. Группа семенных канальцев в поперечном разрезе. Б. Схема строения участка стенки семенного канальца. Показаны клетки на разных стадиях сперматогенеза.
21.6. Клетки Сертоли богаты элементами агранулярного эндоплазматического ретикулума, содержат обширный аппарат Гольджи, а также много митохондрий и лизосом. Что можно сказать о функциях этих клеток на основании такой их структуры?
Сперматоциты располагаются в многочисленных впячиваниях на боковых поверхностях клеток Сертоли; здесь они превращаются в сперматиды, после чего переходят на верхушки клеток Сертоли, обращенные к просвету семенного канальца, где и превращаются в зрелые спермин. Превращение сперматид в спермии обеспечивают клетки Сертоли. Вся поставка питательных веществ и кислорода, развивающимся спермиям, а также удаление из них конечных продуктов метаболизма происходит через клетки Сертоли. Они же секретируют жидкость, в которой спермин проходят по канальцам. Весь процесс развития от сперматогония до спермия занимает около двух месяцев.
Спермии
Спермии — это очень мелкие клетки, всего 2,5 мкм в диаметре (при средних размерах для животных клеток 20 мкм) и примерно 50 мкм в длину. Строение спермия показано на рис. 21.38. В его головке находится ядро, содержащее гаплоидное число хромосом (23 у человека). В ядре имеется также акросома — большая лизосома, содержащая гидролитические ферменты, которые в дальнейшем участвуют в проникновении спермия сквозь слои клеток, окружающих яйцеклетку непосредственно перед оплодотворением.
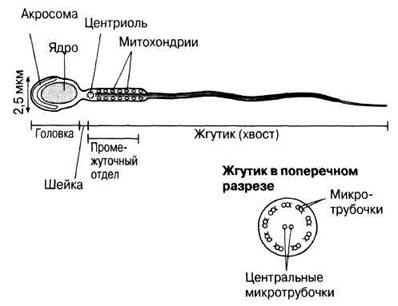
Рис. 21.38. Схема строения зрелого спермия человека.
Короткая шейка спермия содержит пару центриолей, расположенных под прямым углом друг к другу. Микротрубочки одной из центриолей в процессе созревания спермия удлиняются, образуя аксиальную нить жгутика, или хвоста, проходящую вдоль всей остальной части спермия.
Средняя часть спермия — это начало жгутика; она увеличена за счет множества митохондрий, расположенных по спирали вокруг аксиальной нити. Митохондрии обеспечивают аэробное дыхание и продуцируют АТФ, служащую источником энергии. Эта энергия расходуется на движения жгутика, благодаря которым спермий плывет со скоростью примерно 1—4 мм/мин. На поперечном срезе жгутика можно видеть характерное для всех жгутиков расположение девяти пар периферических микротрубочек, окружающих центральную пару микротрубочек.
Активизация жгутика происходит после того, как он попадает во влагалище. Движений жгутика недостаточно, чтобы преодолеть расстояние от влагалища до того места, где происходит оплодотворение. Главная локомоторная задача спермиев состоит в том, чтобы скопиться вокруг ооцита, и ориентироваться соответствующим образом прежде чем проникнуть сквозь мембраны ооцита.
Гормональная регуляция сперматогенеза
Сперматогенез регулируется гормонами гипоталамуса и передней доли гипофиза, действующими совместно. Гипоталамус — один из отделов головного мозга (рис. 17.24), а гипофиз расположен прямо под ним. Гипоталамус секретирует гонадотропин-рилизинг гормон (ГнРГ), который попадает из гипоталамуса в гипофиз по небольшой вене. В свою очередь ГнРГ стимулирует переднюю долю гипофиза к секреции двух гормонов, известных под названием гонадотропинов. (Гонадотропин — это гормон, стимулирующий активность гонады, в данном случае семенника.) Два гонадотропина представляют собой фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ) (рис. 21.39). Такие же два гормона секретируются в организме женщины (см. разд. 21.7.6). По своей химической природе это гликопротеины. ФСГ стимулирует сперматогенез, побуждая клетки Сертоли способствовать завершению развития спермиев из сперматид. ЛГ стимулирует клетки Лейдига (интерстициальные клетки) семенника синтезировать гормон тестостерон. Он известен также как гормон, стимулирующий интерстициальные клетки мужчины. Тестостерон представляет собой стероидный гормон, образующийся из холестерола. Он стимулирует рост и развитие спермиев из клеток зачаткового эпителия; кроме того, вместе с ФСГ он оказывает стимулирующее действие ан клетки Сертоли. Механизм, действующий по принципу отрицательной обратной связи, повышает уровень тестостерона, что ведет к уменьшению секреции ГнРГ гипоталамусом, как это показано на рис. 21.39. Это в свою очередь ведет к понижению уровней ЛГ и ФСГ. Не исключено также, что тестостерон непосредственно воздействует на переднюю долго гипофиза, понижая секрецию Л Г, однако это его действие выражено слабее.
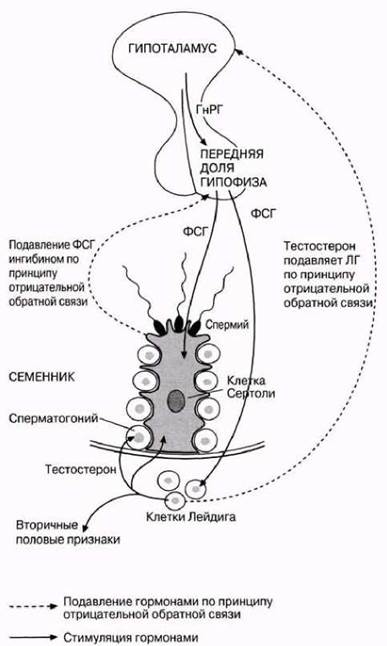
Рис. 21.39. Гормональная регуляция сперматогенеза. ГнРГ, продуцируемый гипоталамусом, стимулирует гипофиз к секреции ФСГ и ЛГ. Л Г стимулирует секрецию тестостерона, который в свою очередь стимулирует образование спермиев, но действует также как ингибитор гипоталамуса по принципу отрицательной обратной связи. ФСГ стимулирует клетки Сертоли, которые вырабатывают ингибин. Ингибин образует вторую ингибирующую систему, действующую по принципу обратной связи, которая регулирует продукцию ФСГ передней долей гипофиза.
Роль ингибина
Клетки Сертоли вырабатывают еще один гликопротеиновый гормон — ингибин, регулирующий образование спермиев по принципу отрицательной обратной связи. Если сперматогенез происходит слишком быстро, то начинает синтезироваться ингибин, который, воздействуя на переднюю долю гипофиза, снижает секрецию ФСГ (рис. 21.39). Ингибин воздействует на гипоталамус, уменьшая секрецию ГнРГ. При низкой скорости сперматогенеза секреция ингибина прекращается, и ФСГ стимулирует сперматогенез.
Роль циклического АТФ
Как ФСГ, так и ЛГ вызывают в клетках, которые они стимулируют, высвобождение циклического АМФ (циклического аденозинмонофосфата, цАМФ); цАМФ является «вторым посредником», рассмотренным в разд. 17.6.1. Он высвобождается в цитоплазму, а затем поступает в ядро, где стимулирует синтез ферментов. В случае ЛГ, например, это ферменты, участвующие в синтезе тестостерона из холестерола.
Вторичные половые признаки
Тестостерон — это главный мужской половой гормон, влияющий на развитие как первичных, так и вторичных половых признаков. Первичными называют признаки, имеющиеся у человека с самого рождения, а вторичными — признаки, развивающиеся к достижению половой зрелости. Для успешного образования спермиев необходимы тестостерон и ФСГ, тогда как развитие вторичных половых признаков и поддержание их на протяжении всей взрослой жизни контролируется только одним тестостероном. К вторичным половым признакам относятся:
1) развитие и увеличение размеров семенников, полового члена и желез репродуктивных путей;
2) увеличение гортани и соответственно более низкий голос;
3) усиленное развитие мускулатуры;
4) рост волос на лобке и усиление их роста в подмышечных впадинах и на груди;
5) особенности поведения, связанные с ухаживанием, брачными отношениями, половой жизнью и родительскими заботами.