Фізіологія людини - Вільям Ф. Ґанонґ 2002
Ендокринна система, метаболізм і репродуктивна функція
Мозкова речовина і кора надниркових залоз
Кора надниркових залоз - Структура і біосинтез адренокортикоїдних гормонів
Класифікація і структура
Гормони кори надниркових залоз є похідними холестеролу. Подібно до холестеролу, жовчних кислот, вітаміну D і тестикулярних стероїдів, вони містять циклопентанпер- гідрофенантренове ядро (рис. 20-7). Гонадні та адренокортикальні стероїди є трьох типів: С21-стероїди, які мають двокарбоновий боковий ланцюг у положенні 17; С19, які мають кето- або гідроксигрупу в положенні 17; С18-стероїди, які мають 17-кето- або гідроксигрупу, однак не мають метильної групи в положенні 10. Кора надниркових залоз виділяє передусім С21- і С19-стероїди. Більшість С19-стероїдів має кетогрупу в положенні 17, тому їх називають 17- кетостероїдами. Стероїди С21, які містять гідроксильну групу в положенні 17 і додатковий боковий ланцюг, часто називають 17-гідроксикортикоїдами, або 17-кортикостероїдами.
Крім того, С19-стероїди мають андрогенну активність; а С21-стероїди поділяють за термінологією Сельє на мінерал окортикоїди і глюкокортикоїди. Всі С21 -стероїди, що виділяються, мають як глюко-, так і мінералокортикоїдну активність. Домінуючим впливом мінералокортикощів є виділення Na+ і К+, а і люкокортикоїдів - обмін глюкози та білків.
Детальна номенклатура стероїдів та їхня ізомерія описані в літературі з номенклатури стероїдів, однак зазначимо, що грецька літера А означає подвійний зв’язок, а групи, що розміщені вище від площини ядра, позначають грецькою літерою ß і простою лінією (-ОН), на відміну від груп, що є під стероїдним кільцем і які позначають літерою а і штриховою лінією (- - - ОН). Отже, С21-стероїди, що їх виділяють надниркові залози, мають ∆4-3-кетокон-фігурацію в А-кільці.
Найчастіше природні надниркові стероїди мають 17- гідроксигрупи в a-конфігурації, а 3-, 11- і 21-гідроксигрупи в ß-конфігурації; 18-альдегідконфігурація в природному альдостероні - D-форма; L-альдостерон є фізіологічно неактивним.
Стероїди, що виділяються
Велика кількість стероїдів була виділена з тканин надниркових залоз, однак єдиними стероїдами, що виділяються у фізіологічно суттєвих кількостях, є мінералокортикоїд альдостерон, глюкокортикоїди кортизол і кортикостерон, андрогени дегідроепіандростерон (ДГЕА) і андростендіон. Структури цих стероїдів показані на рис. 20-8, 20-9. Дезоксикортикостерон є мінералокортикоїдом, який звичайно виділяється в таких же кількостях, як і альдостерон (табл. 20-1), Однак має тільки 3% мінералокортикоїдної активності альдостерону. Його вплив на мінеральний обмін звичайно незначний, проте у випадку захворювань, що супроводжуються збільшенням його секреції, може бути помітним. Більшість естрогенів, які не утворюються в яєчниках, надходять до кровообігу з надниркового андростендіону. Майже весь дегідроепіандростерон виділяється у вигляді сульфату, хоча більшість, якщо не всі стероїди, - у вільній некон’югованій формі.
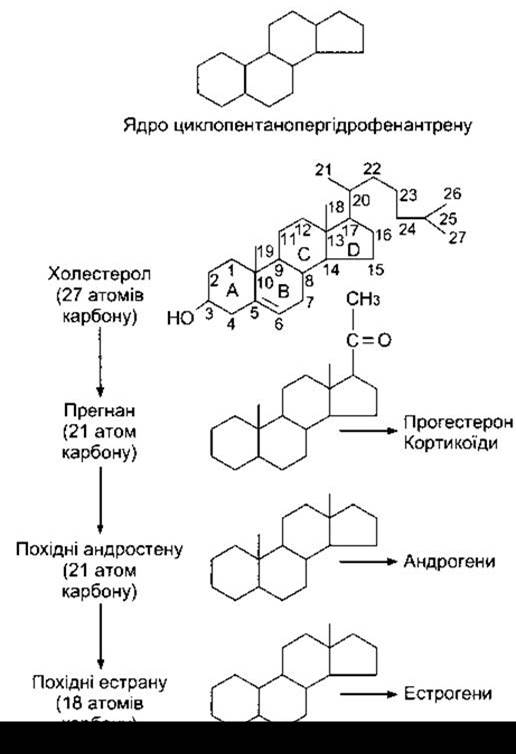
Рис. 20-7. Головні структури адренокортикальних і гонадних стероїдів. Літери у формулі холестеролу відображають чотири головні цикли, а цифри - нумерацію положення замісників у молекулі. Ангулярні метильні групи (положення 18 і 19) звичайно позначають рисками.
Ступінь секреції для окремих стероїдів можна визначити за допомогою введення дуже малих доз позначених ізотопами стероїдів і з’ясування ступеня розведення його непозначеними гормонами у сечі, що виділяється. Цю методику використовують для вимірювання виділень багатьох гормонів.
Видова диференціація
У всіх видів (від амфібій до людей) головними С21-стероїдними гормонами, що їх виділяє адренокортикальна тканина, є альдостерон, кортизол і кортикостерон, хоча співвідношення кортизолу і кортикостерону змінюється. Птахи, миші та щурі виділяють практично тільки кортикостерон; собаки - приблизно однакові кількості цих двох глюкокортикоїдів; у котів, овець, мавп і людей переважає кортизол. У людей співвідношення кортизолу і кортикостерону приблизно 7:1.
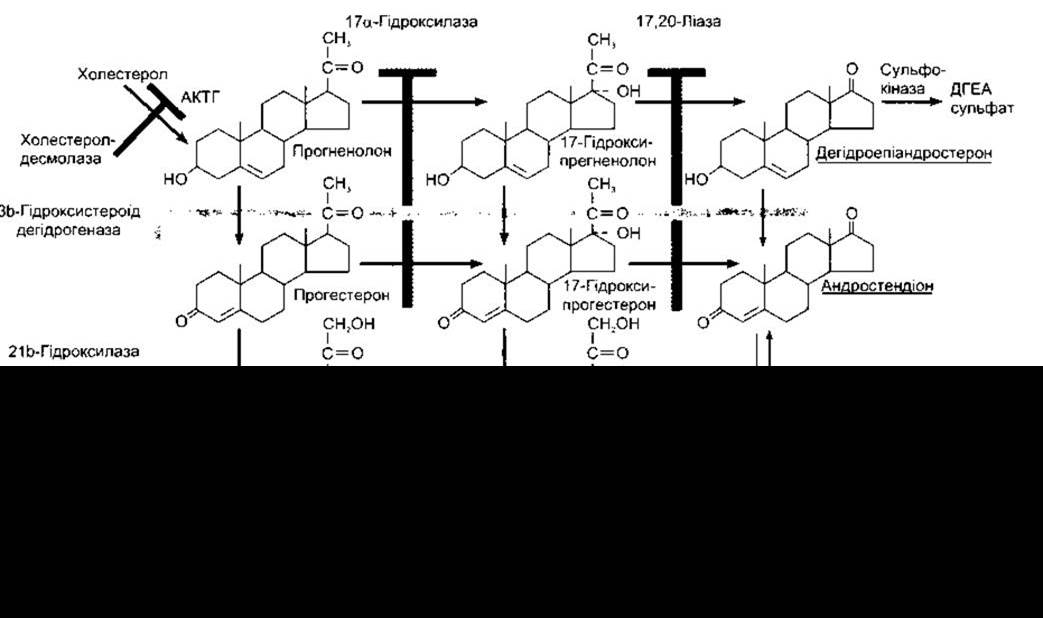
Рис. 20-8. Схема біосинтезу гормонів у пучковій і сітчастій зонах кори надниркових залоз. Головні продукти секреції підкреслені. Ензими відповідних реакцій показані ліворуч і зверху схеми. Якщо відповідного ензиму нема, то утворення гормону блоковано у точках, позначених штриховою лінією.
Синтетичні стероїди
Як і багатьох природних речовин, активність адренокортикальних стероїдів можна збільшити у разі зміни їхньої структури. Сьогодні відомо багато синтетичних стероїдів, що в декілька разів активніші від кортизолу. У табл. 20-2 наведені відносна глюко- і мінералокортикоїдна активність природних та синтетичних стероїдів — 9a-флюорокортизону, преднізолону і дексаметазону. Активність дексаметазону є найбільшою, що пояснюють його високою спорідненістю до глюкокортикоїдних рецепторів і великим періодом напіврозпаду (див. нижче). Преднізолон також має великий період напіврозпаду.
Біосинтез стероїдів
Головні шляхи синтезу природних гормонів кори надниркових залоз, що синтезуються в організмі, показані на рис. 20-8 і 20-9. Попередником усіх стероїдів є холестерол. Частина холестеролу синтезується з ацетату, однак більшість утворюється з ЛПНЩ у кровотоку (див. Розділ 17). Найбільша кількість ЛПНЩ-рецепторів є в адренокортикальних клітинах. Холестерол естерифікується і відкладається у крапельках жиру. Холестиролгідролаза каталізує утворення вільного холестеролу в крапельках жиру (рис. 20-10). Холестерол потрапляє до мітохондрій за допомогою білка, носія стеролів. У мітохондрії він перетворюється в прегненолон під час реакції, яку каталізує холестеролдесмолаза. Цей ензим з надродини мітохондріальних цитохромів Р450, відомий також як ензим відщеплення бокового ланцюга, P450scc або CYP11A. Основи нової CYP-термінології цитохромів P450s описані у Розділі 17. У табл. 20-3 наведені різні назви ензимів, що беруть участь у біосинтезі адренокортикальних стероїдів.
Таблиця 20-1. Головні гормони кори надниркових залоз у дорослих людей1
Назва |
Синонім |
Середня концентрація у плазмі (вільний і зв’язаний)1, мкг/дл |
Середня кількість секреції, мг/доба |
Кортизол |
Сполука F, гідрокортизон |
13,9 |
10 |
Кортикостерон |
Сполука В |
0,4 |
3 |
Альдостерон |
0,006 |
0,15 |
|
Дезоксикортикостерон |
ДОК |
0,006 |
0,20 |
Дегідроепіандростерон моносульфат |
ДГЕАС |
175,0 |
20 |
1 Усі концентрації у плазмі виміряні після стану спокою, крім ДГЕАС, для якого наведена ранкова концентрація.
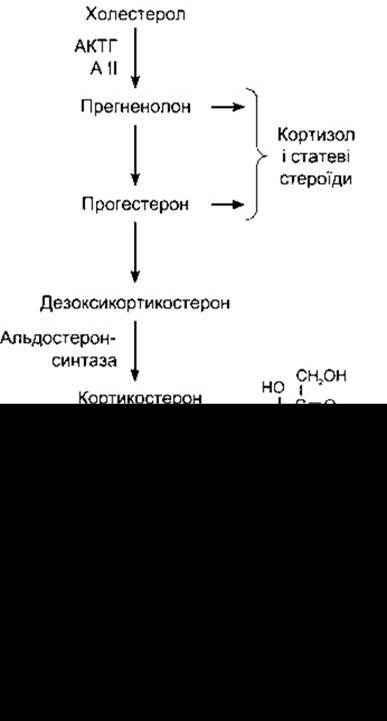
Рис. 20-9. Гормональний синтез у клубочковій зоні. Ця зона потребує 17а-гідроксилазу і тільки у ній може відбуватись перетворення кортикостерону в альдостерон, тому що тільки тут у нормі є альдостеронсинтаза, А II та ангіотензин II.
Прегненолон переходить у гладку ендоплазматичну сітку, де частина його дегідрогенізується з утворенням прогестерону в реакції, яку каталізує 3β-гідроксистероїдодегідрогеназа. Цей ензим має молекулярну масу 46 000 і не є Р450. У пучковій і сітчастій зонах частина прегненолону і прогестерону гідролізується в шорсткій ендоплазматичній сітці з утворенням 17а-гідроксипрегненолону та 17а-гідроксипрогестерону (див. рис. 20-8). Ензим, який каталізує ці реакції, - 17а-гідроксилаза - це є інший Р450 цитохром, який також відомий як Р450с17 (CYP17). Той же ензим є 17,20-ліазою і може каталізувати розрив 17,20-зв’язку з перетворенням 17а-прегненолону і 17а-прогестерону у С19-стероїди дегідроепіандростерон і андростендіон.
Гідроксилювання прогестерону до 11-дезоксикортикостеролу і 17а-гідроксипрогестерону до 11-дезоксикортизолу також відбувається в гладкій ендоплазматичній сітці, його каталізує цитохром 21β-гідроксилаза, яка також відома як Р450с17, або CYP21A2.
11-Дезоксикортикостерон і 11-дезоксикортизол транспортуються назад у мітохондрії, де вони гідроксилюються у положення 11 з утворенням кортикостерону і кортизолу, відповідно. Ця реакція відбувається у пучковій та сітчастій зонах, її каталізує 11ß-гідроксилаза, цитохром Р450, відомий як Р450сn, або CYP11B1.
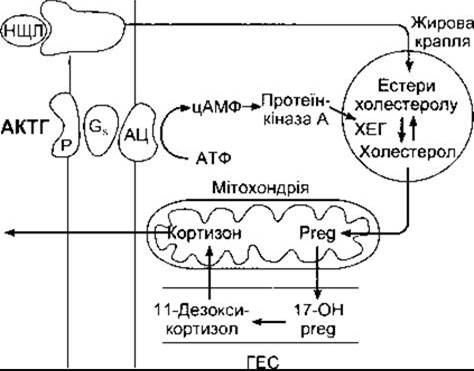
Рис. 20-10. Механізм дії АКТГ на кортизолопродукувальні клітини у двох внутрішніх зонах кори наднирників Коли АКТГ зв’язується зі своїм рецептором (Р) аденілатциклаза (АЦ) активується через Gs. Унаслідок цього збільшення цАМФ активує протеїнкіназу А, а кіназа фосфорилює холестерол-естергідролазу (ХЕГ), збільшуючи її активність. Отже, утворюється більша кількість вільного холестеролу, який перетворюється в прегненолон у мітохондрії Зверніть увагу, що у наступних стадіях біосинтезу стероїдів продукти курсують між мітохондрією й гладкою ендоплазматичною сіткою (ГЕС). Кортикостерон також синтезується і виділяється.
У клубочковій зоні ті ж самі ензими каталізують стероїдний біосинтез до 11-дезоксикортикостерону. Однак інший ензим - альдостеронсинтаза - каталізує утворення кортикостерону і його подальше гідроксилювання й окиснення з утворенням альдостерону. Альдостеронсинтаза, відома також як P450C11AS, або CYP11B2, на 95% подібна до СYP11В1, і гени для них обох містяться в тій же частині 8-ї хромосоми. Однак альдостеронсинтаза звичайно наявна тільки в клубочковій зоні. У цій зоні є недостатня кількість 17а-гідроксилази. Це пояснює те, чому клубочкова зона виробляє альдостерон, однак не здатна утворювати 17- гідроксистероїди або статеві гормони.
Таблиця 20-2. Відносна активність кортикостероїдів порівняно з кортизолом1
Глюкокортикоїдна активність |
Мінералокортикоїдна активність |
|
Стероїд |
||
Кортизол |
1,0 |
1,0 |
Кортикостерон |
0,3 |
15 |
Альдостерон |
0,3 |
3000 |
Дезоксикортикостерон |
0,2 |
100 |
Кортизон |
0,7 |
1,0 |
Преднізолон |
4 |
0,8 |
9а-Флюорокортизол |
10 |
125 |
Дексаметазон |
25 |
~0 |
1 Середні значення, що ґрунтуються на виділенні печінкового глікогену або протизапальних тестах для глюкокортикоїдної активності і впливу на вміст Na+/K+ у сечі або мінералокортикоїдної активності у тварин з адреналектомією. Останні три з наведених стероїдів є синтетичними і не утворюються в організмі (дані з різних джерел).
Таблиця 20-3. Номенклатура надниркових стероїдогенних ензимів та їхнє розміщення у клітинах надниркових залоз
Тривіальна назва |
Р450 |
CYP |
Місцезнаходження |
Холестеролдесмолаза, ензим розщеплення ланцюга |
P450scc |
CYP11A1 |
Мітохондрія |
3ß-Гідроксистероїдодегідрогеназа |
ГЕС |
||
17а-Гідроксилаза, 17,20-ліаза |
Р450С17 |
CYP17 |
ГЕС |
21β-Гідроксилаза |
Р450С21 |
CYP21A2 |
ГЕС |
11ß-Гідроксилаза |
Р450С11 |
CYP11B1 |
Мітохондрія |
Альдостеронсинтаза |
P450C11AS |
CYP11B2 |
Мітохондрія |
Примітка ГЕС - гладка ендоплазматична сітка.
Велика кількість дегідроепіандростерону, утвореного у двох внутрішніх зонах, перетворюється у дегідроепіандростеронсульфат під дією адреналсульфокінази. Андростерон перетворюється у тестостерон і етрадіол.
Дія АКТГ
АКТГ зв’язується з високоафінними рецепторами на плазматичній мембрані адренокортикальних клітин. Це активує аденілатциклазу (див. Розділ 1) через G-білок. Унаслідок збільшення внутрішньоклітинного цАМФ настає активування протеїнкінази А. Протеїнкіназа фосфорилює холестеролестергідролазу, збільшуючи її активність, і перетворення естерів холестеролу у вільний холестерол збільшується (див. рис. 20-10). Це, відповідно, призводить до пришвидшеного утворення прегненолону та його похідних. У довших циклах АКТГ також збільшує синтез Р450, що залучений у синтез глюкокортикоїдів.
Дія ангіотензину II
Ангіотензин II зв’язується з рецепторами клубочкової зони, які діють через G-білок, активуючи фосфоліпазу С (див. Розділ 1). Це сприяє збільшенню протеїнкінази С і перетворенню холестеролу у прегненолон (див. рис. 20-9) та полегшує утворення 18-гідроксикортикостерону, який, відповідно, полегшує утворення альдостерону.
Недостатність ензимів
Наслідки блокування будь-якої з ензимних систем, які беруть участь у біосинтезі стероїдів, можна передбачити з рис. 20-8 і 20-9. Вроджені дефекти ензимів призводять до недостатньої секреції кортизолу і синдрому вродженої надниркової гіперплазії. Гіперплазія є результатом збільшення секреції АКТГ. Недостатність холестеролдесмолази фатальна для внутрішньоутробного розвитку, тому що блокується синтез прогестерону у плаценті, необхідного для підтримання вагітності. Причина важкої вродженої ліпоїдної гіперплазії надниркових залоз у новонароджених - мутація з втратою функції гена білка негайного регулювання стероїдогенезу (StAR - від англ. steroidogenic acute regulatory). Цей білок потрібний у надниркових залозах і гонадах, однак не в плаценті, для нормального транспортування холестеролу у мітохондрію до холестеролдесмолази, яка розташована на матриксній поверхні внутрішньої мітохондріальної мембрани. Якщо його нема, то синтезуються невеликі кількості стероїдів. Ступінь АКТГ стимулювання значний, і як наслідок, простежується нагромадження великої кількості жирових вкраплень у надниркових залозах. Такий стан називають вродженою ліпоїдною гіперплазією надниркових залоз. Оскільки андрогени не сформовані, то жіночі геніталії розвиваються незалежно від генетичної статі (див. Розділ 23). У разі недостатності 3ß-гідроксистероїдодегідрогенази, що також зрідка трапляється, секреція ДГТ збільшена. Цей стероїд - слабкий андроген, який може спричиняти деяку маскулінізацію у хворих жінок, проте не здатний створити повну маскулінізацію геніталій у генетичних чоловіків. Поширена також гіпоспадія (вада розвитку), коли зовнішній отвір сечівника відкривається в калитці або в піхві. У разі повної відсутності 17а-гідроксилази виникає третя рідкісна патологія, зумовлена недостатністю ензиму, кодованого CYP17 геном на 10-й хромосомі, коли жодні статеві гормони не утворюються і формуються жіночі зовнішні статеві органи. Однак шляхи синтезу кортикостерону і альдостерону не ушкоджені і підвищення рівня 11-дезоксикортикостерону та інших мінералокортикоїдів спричинює гіпертонію і гіпокаліємію. Недостатність кортизолу частково компенсує глюкокортикоїдна активність кортикостерону. Різновиди цього синдрому можуть простежуватись у разі втрати активності 17,20-ліази, яка попереджує утворення нормальної кількості статевих гормонів, у випадку адекватної 17-гідроксилазної активності для утворення кортизолу.
На відміну від трьох патологій, описаних вище, недостатність 21ß-гідроксилази і 11ß-гідроксилази трапляється частіше і становить 90-95% від загальної кількості випадків вродженої надниркової гіперплазії. Однак останні підрахунки свідчать, що майже всі випадки спричинені цією патологією і лише 1 % - іншими. Недостатність обох ензимів супроводжується вірилізацією, тому що збільшення секреції АКТГ призводить до накопичення стероїдів і зміни шляху синтезу до утворення андрогенів. Характерним прикладом є андрогенітальний синдром, який виникає у жінок без лікування (рис. 20-11). Ген 21ß-гідроксилази міститься на короткому плечі 6-ї хромосоми; він тісно пов’язаний з HLA - головним комплексом тканинної сумісності (див. Розділ 19), і різноманітні дефекти можуть бути спричинені помірною або значною недостатністю 21 ß-гідроксилази. Для підтримки життєдіяльності звичайно синтезується достатня кількість глюко- і мінералокортикоїдів. У важких випадках геніталії генетичних жінок маскулізують (жіночий псевдогермафродизм; див. Розділ 23). Однак у помірних випадках маскулінізацію можна визначити тільки лабораторним дослідженням. Багато пацієнтів з недостатністю 21ß-гідроксилази втрачають значну частину натрію (вроджена вірилізована надниркова гіперплазія, що супроводжується втратою солей). Втрату Na4 може також зумовлювати недостатність мінералокортикоїдів і альдостеронантагоністичний ефект деяких стероїдів, що утворюються в надлишкових кількостях. За недостатності 11 ß-гідроксилази простежується вірилізація з надлишковою секрецією 11-дезоксикортизолу і 11-дезоксикортикостерону, оскільки 11-дезоксикортикостерон є активним мінералокортикоїдом, то у пацієнтів виникає затримка солей та води і другий-третій ступінь гіпертонії (гіпертонічна форма вродженої вірилізованої надниркової гіперплазії). Глюкокортикоїдна терапія рекомендована у всіх випадках вірилізованих форм вродженої надниркової гіперплазії, тому що відновлює нестачу глюкокортикоїдів і блокує секрецію АКТГ (див. нижче), зменшуючи патологічну секрецію андрогенів та інших стероїдів. Однак дози, які тільки відновлюють нормальну глюкокортикоїдну активність, не повністю усувають надлишкове утворення андрогенів, оскільки наявна патологія у стероїдному біосинтезі і деякий ендогенний субстрат відхилений у бік синтезу андрогену. Інколи на практиці цю проблему вирішують призначенням супернормальних доз глюкокортикоїдів, або комбінуючи глюкокортикоїдну терапію з ліками, що попереджують ефекти надлишку статевих гормонів.

Рис. 20-11. Типові ознаки адреногенітального синдрому у постпубертантної жінки (відтворено за дозволом з Forsham PH, Di Raimondo VC: Traumatic Medicine and Surgery for the Attorney. Butterworth, 1960).
Прояв активності ензимів цитохрому Р450, що відповідають за біосинтез стероїдних гормонів, залежить, відповідно, від стероїдного фактора-1 (SF-1), ядерного рецептора (орфану). У разі Ft2-F1, гена для SF-1, статеві органи, як і надниркові залози, не в стані розвиватися, що зумовлює додаткову аномалію на гіпофізарно-гіпоталамічному рівні.