Молекулярная биотехнология. Принципы и применение - Глик Б., Пастернак Дж. 2002
Молекулярная биотехнология микробиологических систем
Молекулярная диагностика
Методы иммунодиагностики
Многие иммунологические системы детекции обладают высокой чувствительностью и специфичностью, являясь в то же время достаточно простыми. Они широко используются для тестирования лекарственных препаратов, оценки и мониторинга различных онкологических заболеваний, определения специфических метаболитов, идентификации и контроля патогенных микроорганизмов, но имеют и свои ограничения. Если молекулой-мишенью является белок, то необходимо обеспечить экспрессию детерминирующих его генов и создать условия, в которых не происходит маскирование или блокирование сайта связывания с антителом.
Традиционные процедуры диагностики возбудителей инфекции опираются либо на набор характеристик патогенного микроорганизма, либо, что предпочтительнее, на одну уникальную, легко различимую его особенность. Клинические микробиологи пытаются найти тот минимальный набор биологических характеристик, при помощи которого можно будет гарантированно обнаруживать и идентифицировать патогенные микроорганизмы. Например, некоторые возбудители вырабатывают специфические биохимические соединения, которые и необходимо обнаружить в биологическом образце. Часто подобную маркерную молекулу можно выявить непосредственно, проведя высокоспецифичный биохимический анализ. Но такой подход неизбежно приведет к увеличению числа индивидуализированных систем детекции патогенных микроорганизмов. Более предпочтительным был бы универсальный метод, позволяющий выявлять любую маркерную молекулу независимо от ее химической природы. Именно таким является метод, основанный на идентификации комплексов антиген—антитело.
Ферментный иммуносорбентный анализ
Существует целый ряд подходов, позволяющих определить, произошло ли связывние антитела с антигеном-мишенью. Один из них — это ферментный иммуносорбентный анализ (ELISA), который часто используют для диагностики. Процедура включает следующие этапы (рис. 9.1).
1. Образец, в котором хотят обнаружить специфическую молекулу или микроорганизм, фиксируют на твердой подложке, например на пластиковой микротитровальной плашке, обычно имеющей 96 лунок (рис. 9.1, А).
2. К фиксированному образцу добавляют антитело, специфичное к маркерной молекуле (первое антитело), затем промывают лунку, чтобы удалить несвязавшиеся молекулы первого антитела (рис. 9.1, Б).
3. Добавляют второе антитело, которое специфически связывается с первым антителом и не взаимодействует с маркерной молекулой (рис. 9.1, В). К этому антителу присоединен фермент (например, щелочная фосфатаза, пероксидаза или уреаза), катализирующий превращение неокрашенного субстрата в окрашенный продукт. Промывают лунку, чтобы удалить несвязавшиеся молекулы конъюгата второе антитело—фермент.
4. Добавляют неокрашенный субстрат (рис. 9.1, І).
5. Проводят качественное или количественное определение окрашенного продукта.
Если первое антитело не связывается с мишенью образца, то оно удаляется при первом промывании. Поскольку при этом конъюгату второе антитело—фермент не с чем связываться, он удаляется при втором промывании, и образец остается неокрашенным. Если связывание с мишенью происходит, то второе антитело присоединяется к первому, и конъюгированный фермент катализирует образование легко регистрируемого окрашенного продукта.
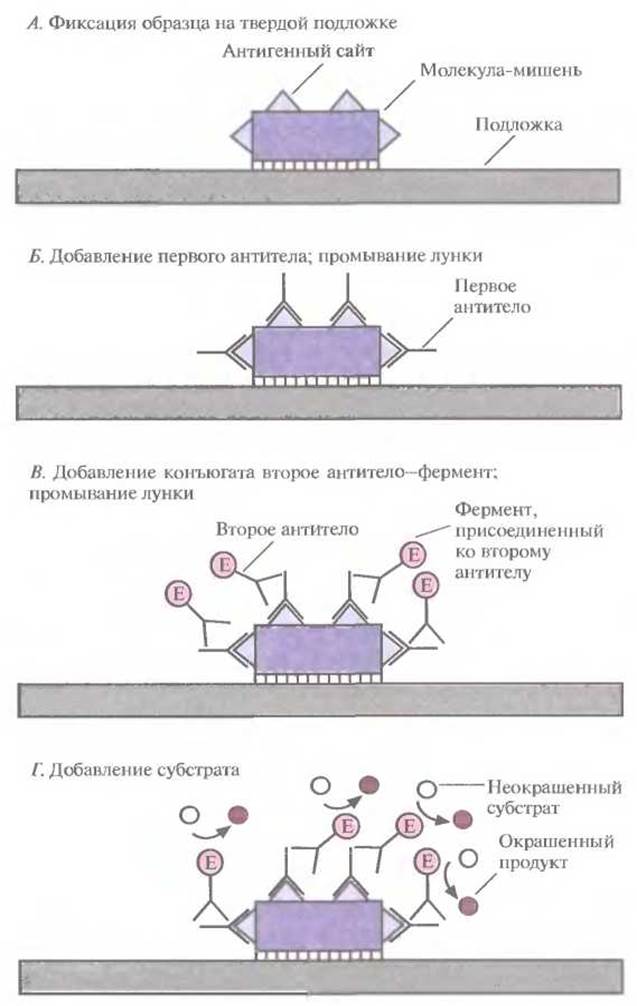
Рис. 9.1. Обнаружение антигена-мишени с помощью ELISA. Е—фермент, присоединенный ко второму антителу
Основной принцип ELISA — специфическое связывание первого антитела с мишенью. Если молекула-мишень представляет собой белок, то его очищенный препарат обычно используют для получения антител, при помощи которых затем и выявляют данную мишень. Антитела, которые образуются в сыворотке (антисыворотке) крови иммунизированного животного (обычно кролика), связываются с разными антигенными детерминантами (эпитопами) молекулы-мишени. Такую смесь антител называют поликлональным препаратом. Использование поликлональных антител имеет два недостатка, существенных для некоторых методов диагностики: 1) содержание отдельных антител в поликлональном препарате может варьировать от одной партии к другой; 2) поликлональные антитела нельзя применять, если необходимо различить две сходные мишени, т. е. когда патогенная (мишень) и непатогенная (не-мишень) формы различаются единственной детерминантой. Однако эти проблемы вполне разрешимы, поскольку сейчас научились получать препараты антител, выработанных к одной антигенной детерминанте, т. е. препараты моноклональных антител.
Моноклональные антитела
У млекопитающих в ходе эволюции выработался сложный набор клеточных систем, защищающих организм от токсичных веществ и инфекционных агентов. Составной частью защитной реакции является индуцированная выработка клетками лимфатической системы специфических белков (антител), которые соединяются с чужеродными веществами (антигенами) и при помощи других белков иммунной системы, включая системы комплемента, нейтрализуют их эффект. В ответ на иммунологический стимул каждая антителопродуцирующая клетка синтезирует и выделяет единственный вид антител, которые с высоким сродством распознают отдельный участок (эпитоп, антигенную детерминанту) молекулы антигена. Поскольку в молекуле антигена обычно присутствует несколько разных эпитопов, антитела против каждого из них вырабатываются отдельными клетками иммунной системы. Такие антитела, каждое из которых взаимодействует с данным антигеном, называют поликлональными.
Уже в начале нынешнего века, когда о поликлональности антител ничего не знали, было ясно, что их специфичность можно использовать для подавления инфекций. Позже антитела стали применять в качестве диагностического инструмента для выявления токсичных соединений в клинических образцах. К сожалению, эффективность препаратов поликлональных антител варьирует от одной партии к другой, поскольку в одних случаях при проведении иммунизации антителопродуцирующие клетки сильнее стимулируются одними детерминантами данного антигена, а в других иммунная система активнее отвечает на другие эпитопы того же антигена. Это может влиять на способность разных препаратов нейтрализовать антигены, поскольку отдельные эпитопы обладают разной эффективностью (стимулирующей способностью). Следовательно, в данной партии поликлональных антител может содержаться мало молекул, направленных против основного эпитопа, и в результате она будет менее эффективной, чем предыдущая.
Следовательно, для практического применения антител в качестве диагностического инструмента или компонентов терапевтических средств необходимо было создать такую линию клеток, которая росла бы в культуре и продуцировала антитела одного типа, обладающие высоким сродством к специфическому антигену-мишени, — моноклональные антитела. Подобная клеточная линия могла бы стать неиссякающим источником идентичных молекул антител. К сожалению, В-лимфоциты (В-клетки), синтезирующие антитела, не могут воспроизводиться в культуре. Решение данной проблемы виделось в создании гибридной клетки. Получив генетическую составляющую от В-клетки, она могла бы вырабатывать антитела, а приобретя способность к делению от клетки совместимого типа — расти в культуре. Было известно, что В-лимфоциты иногда перерождаются и становятся раковыми (миеломными) клетками, приобретая способность к росту в культуре и сохраняя в то же время многие свойства В-клеток. Так клетки миеломы, в первую очередь те, которые не вырабатывают антител, стали кандидатами на слияние с антителопродуцирующими В-клетками. В середине 70-х гг. эти идеи стали реальностью.
Образование и отбор гибридных клеток Первый шаг в процессе получения гибридной клеточной линии, продуцирующей антитела одного типа, состоит во введении мышам антигена. После ряда иммунизаций, проведенных в течение нескольких недель, проверяют, произошло ли развитие у животных иммунного ответа. Если ответ развился, то животных умерщвляют, извлекают селезенку, промывают ее, измельчают и несильно встряхивают для высвобождения единичных клеток, среди которых находятся и антителопродуцирующие В-клетки. Взвесь клеток селезенки смешивают со взвесью миеломных клеток, дефектных по гипоксантин-гуанин—фосфорибозилтрансферазе (HGPRT-). Комбинированную взвесь в течение нескольких минут инкубируют в 35%-ном полиэтиленгликоле, а затем переносят в среду, содержащую гипоксантин, аминоптерин и тимидин (среда ГАТ).
Обработка полиэтиленгликолем облегчает слияние клеток, тем не менее слияние происходит редко и является в достаточной степени случайным событием. В смеси присутствуют клетки миеломы, селезенки, а также слившиеся клетки миеломы—селезенки, миеломы—миеломы, селезенки—селезенки. Однако в среде ГАТ растут только гибридные клетки миеломы—селезенки, все остальные типы клеток не могут в ней пролиферировать. Клетки селезенки и слившиеся клетки селезенки—селезенки вообще не растут в культуре, а миеломные клетки HGPRT и слившиеся клетки миеломы—миеломы не могут использовать гипоксантин в качестве предшественника в процессе биосинтеза пуриновых оснований гуанина и аденина, без которых невозможен синтез нуклеиновых кислот. Но у них есть другой естественный путь синтеза пуринов — при участии дигидрофолатредуктазы, поэтому в состав среды и входит аминоптерин, ингибирующий активность этого фермента. Таким образом, миеломные клетки HGPRT- и слившиеся клетки миеломы—миеломы не могут синтезировать пурины в среде ГАТ и погибают.
Слившиеся клетки селезенки—миеломы растут в среде ГАТ, поскольку: 1) клетки селезенки поставляют функциональную HGPRT, которая может утилизировать экзогенный гипоксантин среды несмотря на блокирование синтеза пуринов с участием дигидрофолатредуктазы аминоптерином; 2) клетки миеломы способны активно делиться. Тимидин необходим для устранения блокирования в синтезе пиримидинов, обусловленного ингибированием дигидрофолатредуктазы. На 10—14-е сутки после слияния клеток в среде ГАТ остаются и растут только слившиеся клетки селезенки—миеломы. Их затем вносят в лунки пластиковых микротитровальных плашек и выращивают на полной культуральной среде без ГАТ.
Идентификация гибридных клеточных линий, секретирующих специфические антитела
Теперь необходимо идентифицировать гибридные клетки, вырабатывающие антитела к иммунизирующему антигену. Для этого обычно проводят скрининг культуральных сред, содержащих секретируемые антитела. Среду из тех лунок, в которых есть растущие клетки, отбирают и переносят в лунки другой микротитровальной плашки, предварительно покрытые слоем молекул антигена-мишени. Если в культуральной среде находится антитело (первое антитело), распознающее один из эпитопов данного антигена, то оно свяжется с антигеном и останется в лунках после их промывания. Затем в лунки добавляют второе антитело, специфичное к мышиным антителам. Оно будет присоединяться к любому первому антителу, связанному с антигеном.
К используемому в иммунном анализе второму антителу предварительно присоединяют фермент, который превращает неокрашенный субстрат в окрашенное соединение. Изменение цвета содержимого одной из лунок говорит о том, что исходная культуральная среда содержала антитело, специфичное к данному антигену (рис. 9.2). Если же такое антитело в среде отсутствовало, то второму антителу не с чем будет связываться и оно смоется при втором промывании. Субстрат в таких лунках останется неокрашенным.
Лунки исходной микротитровальной плашки, среда из которых дает положительный иммунный ответ (изменение цвета), могут содержать смесь слившихся клеток. Чтобы получить линии, происходящие от одной клетки (клоны), клеточную суспензию из таких лунок разводят культуральной средой и высевают в другие лунки. После культивирования полученных клонов среды вновь тестируют, определяя, какая из клеточных линий (гибридом) продуцирует моноклональные антитела, распознающие антиген-мишень. В том случае, когда получают более одной специфичной гибридомы, проводят дальнейшие исследования, позволяющие определить, направлены ли антитела, вырабатываемые разными клонами, против одной и той же антигенной детерминанты. Каждый клон, продуцирующий моноклональное антитело, можно поддерживать в культуре практически бесконечно. Кроме того, образцы можно заморозить в жидком азоте и использовать их в дальнейшем как источник клеток.

Рис. 9.2. Скрининг клеток, вырабатывающих моноклональные антитела. Выделяют клетки селезенки мыши, иммунизированной специфическим антигеном, и проводят их слияние с клетками миеломы, не вырабатывающими антитела. Слившиеся клетки отбирают по способности к росту на среде ГАТ (гипоксантин, аминоптерин, тимидин). Клетки, вырабатывающие специфические антитела к иммунизирующему антигену (клетки гибридомы), идентифицируют иммунологическими методами и субкультивируют, чтобы получить отдельные клоны. Из гибридомы, растущей в культуре и секретирующей единственный тип молекул антител, получают моноклональные антитела.

Рис. 9.3. Использование моноклональных антител для выявления различных соединений и диагностики инфекционных заболеваний.
Применение моноклональных антител позволяет существенно повысить специфичность метода ELISA, поскольку они связываются с одним, строго определенным антигенным сайтом. К настоящему времени получен целый ряд моноклональных антител, которые можно использовать для обнаружения различных соединений и патогенных микроорганизмов (рис. 9.3). Альтернативой получению моноклональных антител из культуры гибридомных клеток может быть отбор и производство моноклональных антител и их частей (Fv-фрагментов), направленных против антигена-мишени, с помощью Е. coli (см. гл. 10).