Молекулярная биотехнология. Принципы и применение - Глик Б., Пастернак Дж. 2002
Молекулярная биотехнология микробиологических систем
Молекулярная диагностика
Молекулярная диагностика генетических заболеваний
Диагностика специфических наследственных заболеваний человека на генетическом уровне дает ответ на вопрос, входят ли обследуемые индивидуумы или их потомки в группу повышенного генетического риска. ДНК-анализ можно использовать для выявления носителей генов наследственных заболеваний, а также для пренатальной и пресимптоматической диагностики серьезных генетических нарушений.
Тесты на уровне ДНК позволяют безошибочно выявлять специфические мутации. Раньше для этого применялись биохимические методы, основанные на выявлении продукта анализируемого гена. ДНК-тесты не требуют экспрессии мутантного гена для его выявления, что позволяет разработать системы скрининга для всех моногенных заболеваний.
Серповидноклеточная анемия Серповидноклеточная анемия — генетическое заболевание, обусловленное заменой одного нуклеотида в кодоне, который соответствует шестой аминокислоте в ß-цепи молекулы гемоглобина. У индивидов, гомозиготных по мутантному гену (S/S), эритроциты имеют необычную серповидную форму; это связано с искажением конформации молекулы гемоглобина вследствие замены в ней валина на глутаминовую кислоту. Мутантный гемоглобин не может с достаточной эффективностью переносить кислород, и у таких больных развивается тяжелая анемия с прогрессирующим поражением сердца, легких, мозга, суставов и других органов. У индивидов, гетерозиготных по данному гену (A/S) (носителей генетического заболевания), эритроциты имеют нормальную форму, и симптомы заболевания проявляются лишь в экстремальных условиях (на большой высоте над уровнем моря либо при слишком высоких или низких температурах, когда снижается снабжение организма кислородом). Если оба родителя гетерозиготны (имеют генотип A/S), то вероятность того, что их ребенок будет гомозиготным по мутантному гену (S/S) (т. е. будет болен серповидноклеточной анемией), составляет 25%. Ген серповидноклеточной анемии с высокой частотой встречается среди афроамериканцев и их потомков, а также среди латиноамериканцев. В США проводят скрининг для выявления носителей гена серповидноклеточной анемии, которые могут передать этот ген своим потомкам. Рассмотрим один из используемых для этого тестов.
Замена одного нуклеотида в ß-глобиновом гене, приводящая к серповидноклеточной анемии, сопровождается элиминацией сайта для рестрицирующей эндонуклеазы CvnІ. Этот фермент узнает последовательность CCTNAGG и расщепляет молекулу ДНК между основаниями С и Т (N — любой из четырех нуклеотидов). В нормальном гене эта последовательность имеет вид CCTGAGG, а в гене серповидноклеточной анемии — ССТGTGG. На этом различии основывается ДНК-диагностика данного заболевания (рис. 9.9).
Используя праймеры, фланкирующие сайт CvnІ, амплифицируют с помощью ПЦР небольшое количество тестируемой ДНК (рис. 9.9, А). Амплифицированный фрагмент обрабатывают CvnІ, продукты рестрикции разделяют с помощью гель-электрофореза и окрашивают их бромистым этидием. При наличии CvnІ-сайта на электрофореграмме появляется специфический набор полос (рис. 9.9, В), отличный от такового в отсутствие Civil-сайта. Описанным способом можно без труда и достаточно быстро установить генетический статус обследуемого, не проводя при этом процедуру гибридизации.
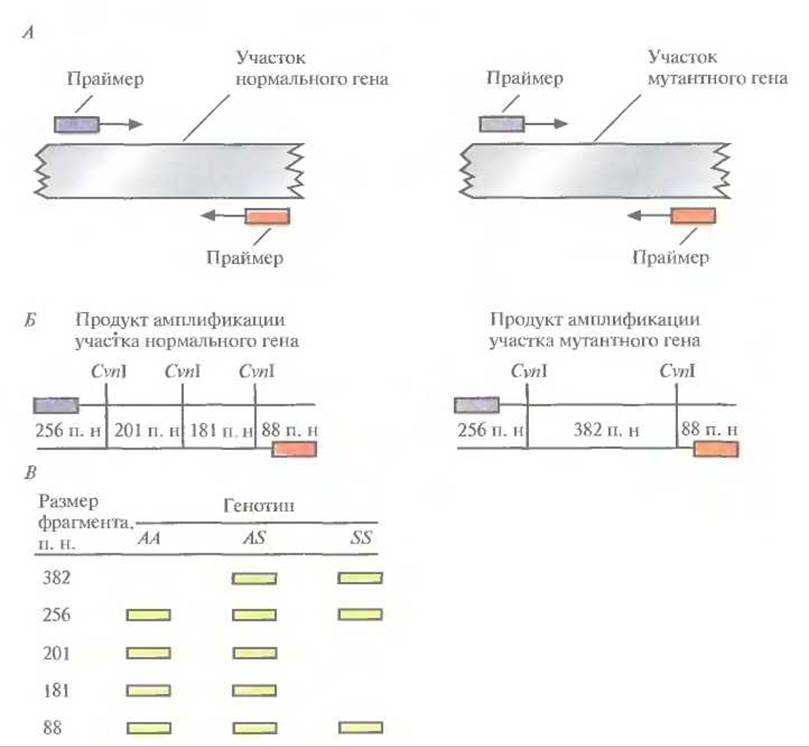
Рис, 9.9. Выявление мутантного гена, ответственного за развитие серповидноклеточной анемии. A. ПЦР-амплификация участка ß-глобинового гена, содержащего сайты для эндонуклеазы CvnІ, один из которых отсутствует в мутантном гене. Б. Рестрикция полученных ПЦР -продуктов с помощью CvnІ. Нормальный ген содержит три CvnI-сайта в сегменте ДНК, фланкируемом праймерами, а мутантный — два. B. Электрофоретическое разделение фрагментов, полученных при обработке ПЦР-амплифицированной ß-глобиновой ДНК с помощью CvnI. AA — гомозиготность по нормальному ß-глобиновому гену, AS — гетерозиготность, SS — гомозиготность по гену серповидноклеточной анемии.
Метод ПЦР/ЛO3
Не все генетические нарушения, приводящие к появлению дефектных генов, сопровождаются утратой или изменением сайтов рестрикции, поэтому для обнаружения однонуклеотидных замен применяют и другие подходы. В одном из них объединены ПЦР и метод, основанный на лигировании олигонуклеотидных зондов (ЛОЗ), ПЦР/ЛОЗ.
Предположим, что в определенном сайте нормального гена (скажем, в 106-м положении) находится пара А∙Т, а в том же сайте мутантного гена — G∙C. Зная нуклеотидные последовательности, фланкирующие 106-й нуклеотид, можно синтезировать два коротких (20-нуклеотидных) фрагмента, прилегающих к данному сайту и комплементарных противоположным цепям (рис. 9.10). Основная особенность этой пары олигонуклеотидов состоит в том, что 3'-концевой нуклеотид одного из них (зонд X) комплементарен основанию, находящемуся в 106-м положении нормальной последовательности, а 5'-концевой нуклеотид второго (зонд Y) комплементарен нуклеотиду, примыкающему к 106-му нуклеотиду. При отжиге этих зондов с содержащей нормальную последовательность ДНК-мишенью (амплифицированной методом ПЦР) происходит их полная гибридизация, и при добавлении в реакционную смесь ДНК-лигазы зонды X и Y ковалентно сшиваются. Если же эти зонды отжигаются с мутантной ДНК, в которой произошла замена 106-го нуклеотида, то некомплементарный ему 3'-концевой нуклеотид зонда X не может образовать с ним пару. И хотя зонд Y по-прежнему гибридизуется полностью, ДНК-лигаза не может сшить зонды X и Y.
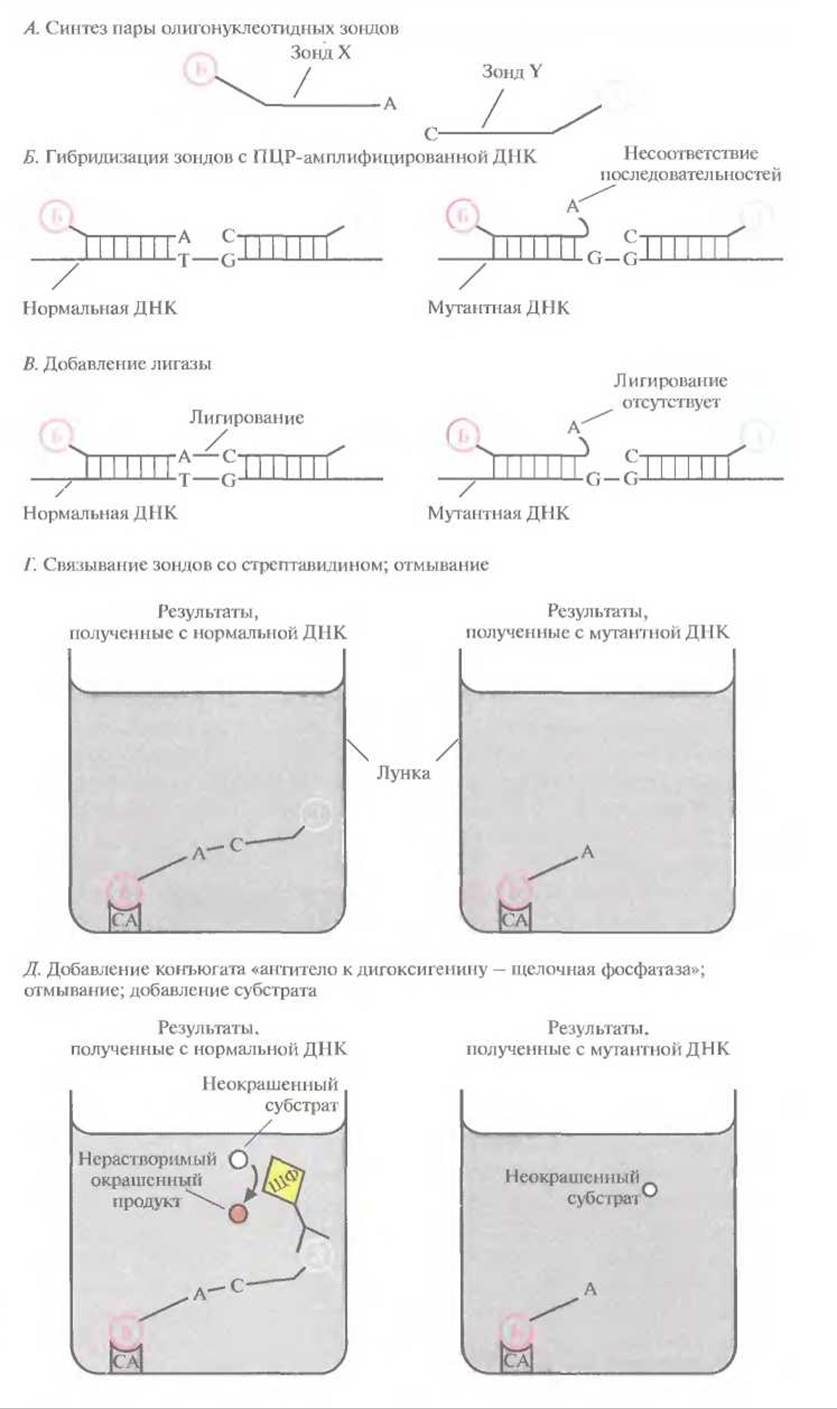
Рис. 9.10. Метод ПЦР/ЛОЗ. Б — биотин; Д — дигоксигенин; 1ДФ — щелочная фосфатаза; СА — стрептавидин.
Можно синтезировать и другие олигонуклеотидные зонды, полностью соответствующие последовательности с мутантным 106-м нуклеотидом. При таком наборе зондов лигирование будет происходить в случае их отжига с мутантной ДНК-мишенью и не будет в случае отжига с нормальной мишенью. Таким образом, метод ПЦР/ЛОЗ различает две ситуации: лигирование зондов и отсутствие лигирования.
Чтобы определить, произошло ли лигирование, 5'-конец зонда X метят биотином, а 3'-конец зонда Y — дигоксигенином, низкомолекулярным соединением, связывающимся с соответствующим антителом. После гибридизации и лигирования проводят денатурацию ДНК для высвобождения гибридизовавшегося зонда и переносят смесь в небольшую пластиковую лунку, покрытую стрептавидином. Лунку промывают, чтобы удалить весь материал, кроме связавшегося со стрептавидином биотинилированного зонда. Затем добавляют в лунку антитела к дигоксигенину, предварительно соединенные со щелочной фосфатазой. После промывания, в ходе которого происходит удаление несвязанного конъюгата, добавляют бесцветный хромогенный субстрат. Окрашивание раствора в лунке свидетельствует о связывании антитела к дигоксигенину с зондом, меченным дигоксигенином, т. е. о том, что этот зонд был лигирован с зондом, меченным биотином. Если же окрашивания не происходит, значит лигирования не было.
Располагая двумя парами зондов, можно установить генетический статус любого человека. Например, ДНК гетерозиготных носителей дает положительный ответ с обеими парами зондов, ДНК лиц, обладающих двумя копиями нормального гена, — только с тем набором зондов, который содержит нуклеотид, комплементарный нормальному сайту, и, наконец, ДНК индивидов с двумя измененными копиями гена — только с набором зондов, детектирующим мутантный сайт. Чтобы минимизировать необходимое для анализа количество исходной ДНК, перед гибридизацией участок ДНК-мишени, содержащий тестируемый сайт, амплифицируют с помощью ПЦР.
ПЦР/ЛОЗ является быстрым, чувствительным и высокоспецифичным методом. Все его стадии роботизированы, что позволяет проводить до 1200 тестов в день.
Более простым, хотя и менее чувствительным вариантом ПЦР/ЛОЗ является метод лигазной цепной реакции. Тестируемую ДНК смешивают с избытком двух индикаторных зондов, описанных выше, в присутствии термостабильной ДНК-лигазы. Проводят лигирование при 65 °С, затем повышают температуру до 94 °С, чтобы произошла денатурация образовавшихся гибридов зонд—ДНК-мишень, и вновь понижают температуру до 65 °С для гибридизации свободных нелигированных индикаторных ЛОЗ-зондов с ДНК-мишенью. Этот цикл повторяют 20 раз. Если индикаторные ЛОЗ-зонды полностью комплементарны ДНК-мишени, то лигирование будет происходить в каждом цикле, и после 20 циклов накопится достаточно продуктов лигирования («сшитых» зондов X и Y) для того, чтобы их можно было обнаружить с помощью электрофореза или ELІSA. Если комплементарностъ неполная, то лигирование не произойдет и никаких продуктов зарегистрировано не будет.
Генотипирование с использованием флуоресцентно меченных ПЦР-праймеров Колориметрическое генотипирование основано на применении ПЦР-праймеров, меченных различными флуоресцентными красителями. Чтобы различить мутантную ДНК и ДНК дикого типа, проводят ПЦР с двумя разными праймерами. Один из них (Р1) комплементарен ДНК дикого типа и на 5'-конце помечен родамином (красный цвет), другой (Р3) комплементарен мутантной ДНК и на 5'-конце помечен флуоресцеином (зеленый цвет) (рис. 9.11). В обоих случаях амплификацию проводят в присутствии третьего, немеченного праймера (Р2), комплементарного противоположной цепи. Поскольку ПЦР может идти только в том случае, когда праймер полностью комплементарен ДНК-мишени, в присутствии в реакционной смеси всех трех праймеров будет амплифицироваться либо ДНК дикого типа, либо мутантная ДНК, либо обе они, в зависимости от ДНК-мишени, играющей роль матрицы. Если индивид гомозиготен по Д НК дикого типа, то после проведения ПЦР и удаления лишних праймеров будет наблюдаться флуоресценция красного цвета, если он гомозиготен по мутантной ДНК — зеленого, а если присутствуют и мутантная ДНК, и ДНК дикого типа (т. е. индивид гетерозиготен) — желтого. Этот метод можно автоматизировать и адаптировать для любого однонуклеотидного сайта-мишени в любом гене с известной нуклеотидной последовательностью.
Мутации в разных сайтах одного гена
Далеко не все генетические заболевания обусловливаются одним специфическим изменением в гене. В большинстве случаев мутации происходят в разных сайтах в пределах одного гена, но приводят к одному генетическому заболеванию. В качестве примера можно привести ß-талассемию — наследственное заболевание, связанное с утратой активности ß-глобина. У гетерозиготных носителей при этом обычно наблюдается небольшая анемия. Индивиды же, гомозиготные по одному из как минимум восьми возможных мутантных сайтов, для поддержания жизни нуждаются в регулярном переливании крови и другом лечении. Поскольку мутация в любом из восьми специфических сайтов ß-глобинового гена может приводить к ß-талассемии, необходимо провести по крайней мере восемь разных тестов. Такая диагностика возможна, хотя и весьма дорогостояща.
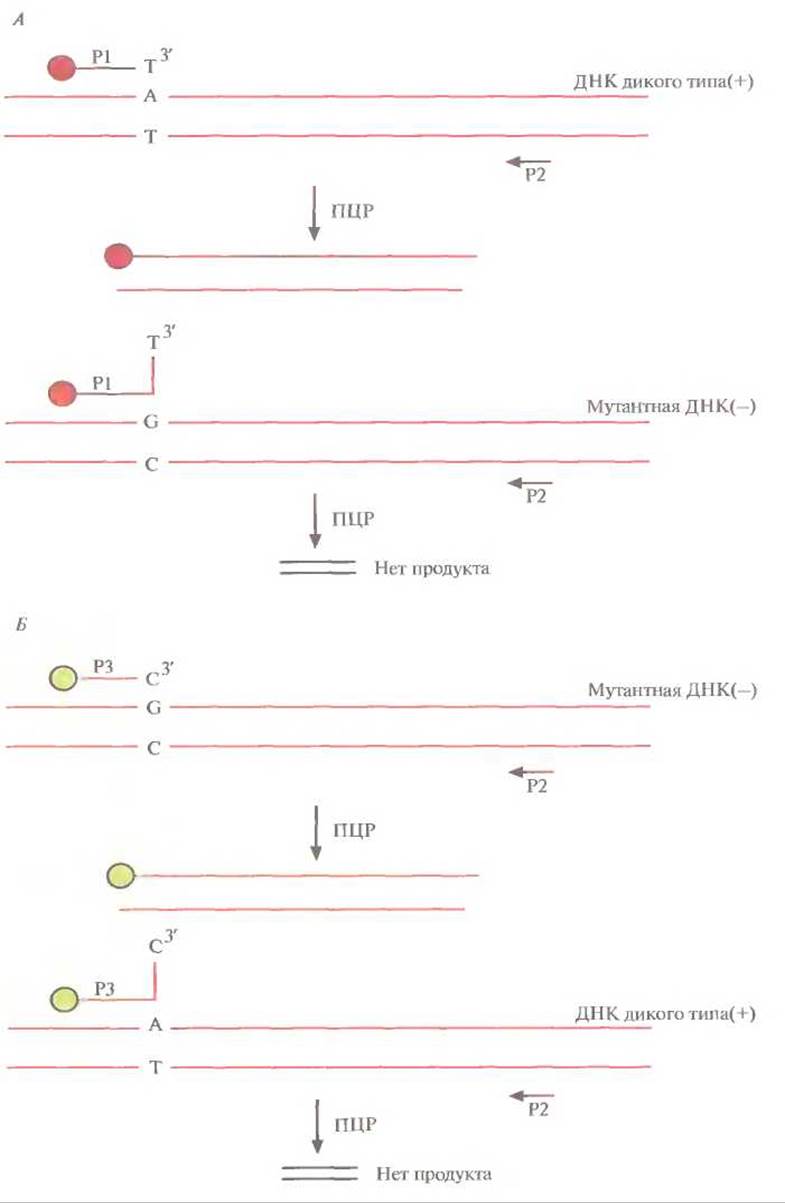
Рис. 9.11. Обнаружение толковой мутации с помощью флуоресцентно меченных ПЦР-праймеров. А. Используя праймеры Р1 и Р2, амплифицируют ДНК дикого типа. Мутантная ДНК при помощи данных праймеров не амплифицируется из-за несоответствия ей праймера Р1. 5'-конец праймера Р1 помечен родамином, праймер Р2 немеченый. Б. Используя праймеры Р3 и Р2, амплифицируют мутантную ДНК; ДНК дикого типа в этом случае не амплифицируется. S'- конец праймера Р3 помечен флуоресцеином, праймер Р2 немеченый. Знаки «+» и «—» соответствуют сайту дикого типа и мутантному сайту. В случае генотипов «+/+», «+/—» и «—/—» образуются ПЦР-продукты, содержащие только родамин, смесь родамина и флуоресцеина и только флуоресцеин, и соответственно наблюдается красная, желтая и зеленая флуоресценция.
Поэтому для скрининга мутаций, возникающих в разных сайтах одного гена, была разработана стратегия ПЦР/гибридизация, основанная на проведении одной реакции. Для этого синтезируют набор специфических 20-нуклеотидных зондов, каждый из которых полностью комплементарен фрагменту гена-мишени, несущему известную мутацию. К 3'-концу каждого зонда присоединен гомополимер poly(dT) длиной примерно 400 нуклеотидов, с помощью которого ДНК-зонд связывается с заранее отмеченной точкой на найлоновом фильтре, а остальная его часть остается свободной и может гибридизоваться (рис. 9.12). Сегменты тестируемой ДНК, каждый из которых включает по одному из возможных мутационных сайтов, одновременно амплифицируют с помощью ПЦР, причем один праймер из каждой пары на 5'-конце помечен биотином. Амплифицированные фрагменты ДНК-мишени гибридизуют с зондами, пришитыми к фильтру, в условиях, обеспечивающих гибридизацию только полностью комплементарных последовательностей. В гибридизационную смесь добавляют стрептавидин, связанный с щелочной фосфатазой (можно также использовать пероксидазу хрена или уреазу). После гибридизации промывают фильтр и добавляют неокрашенный субстрат. Если имеет место полное соответствие между амплифицированным сегментом ДНК-мишени и специфическим олигонуклеотидным зондом, то на фильтре появится цветная точка. На один и тот же фильтр можно нанести несколько точек, соответствующих целому ряду разных специфических олигонуклеотидных зондов. Проанализировав эту цветную мозаику, можно идентифицировать один из многих возможных сайтов мутации.
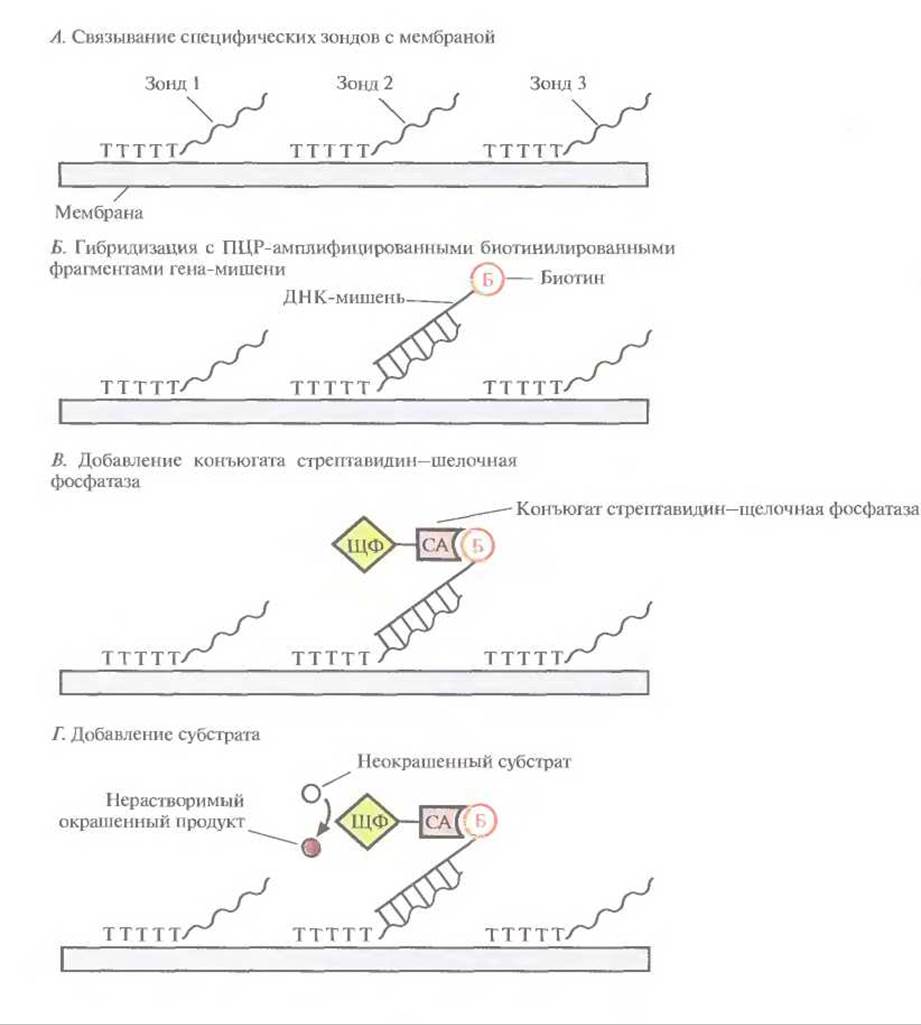
Рис. 9.12. Выявление мутаций в разных сайтах одного гена. Б — биотин; СА — стрептавидин; ЩФ — щелочная фосфатаза.