Молекулярная биология клетки - Том 2 - Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К., Уотсон Дж. 1993
Цитоскелет
Мышечное сокращение
Многие белки, входящие в состав свойственного всем клеткам актинового цитоскелета, впервые были открыты в мышцах, и из всех типов движения, наблюдаемых у животных, мышечное сокращение для нас наиболее знакомо и лучше всего изучено. Бег, ходьба, плавание, полет - все эти виды локомоции у позвоночных основаны на способности скелетных мышц быстро сокращаться, приводя в движение соединенные с ними кости скелета; а такие виды непроизвольных движений, как работа сердца и перистальтика кишечника, обусловлены сокращением сердечной и гладких мышц соответственно.
Мышечное сокращение-результат работы весьма сложного и мощного белкового аппарата, который в зачаточной форме присутствует почти во всех эукариотических клетках. В процессе эволюции мышечных клеток элементы цитоскелета подверглись сильной гипертрофии и специализации, что сделало сократительный механизм мышц чрезвычайно стабильным и эффективным. В поперечнополосатой мускулатуре, к которой относятся скелетные и сердечная мышцы, а также сходные ткани беспозвоночных (например, летательные мышцы насекомых), структурная организация сократительного аппарата достигает такой степени, что можно непосредственно наблюдать его работу, и при этом сразу выявляется ряд важных свойств составляющих его молекул.
11.1.1. Сократительными элементами клеток скелетной мышцы служат миофибриллы
Длинные, тонкие мышечные волокна, из которых построена скелетная мышца, - это гигантские клетки, образующиеся в ходе онтогенеза при слиянии множества отдельных клеток (разд. 17.6.1). Они получаются многоядерными, причем ядра располагаются прямо под плазматической мембраной. Основная же часть цитоплазмы (около двух третей сухого веса) состоит из миофибрилл - цилиндрических элементов толщиной 1-2 мкм, которые часто тянутся от одного конца клетки до другого (рис. 11-1). На изолированных миофибриллах отчетливо видны поперечные полоски, от которых и зависит характерная поперечная исчерченность клеток скелетных мышц. Если к изолированным миофибриллам добавить АТР и Са2+, они тотчас же сократятся - значит, именно они служат генераторами силы при сокращении мышечных клеток. Каждая миофибрилла представляет собой цепь миниатюрных сократимых единиц, состоящих из регулярным образом расположенных систем толстых и тонких нитей (филаментов).
11.1.2. Миофибриллы построены из повторяющихся ансамблей толстых и тонких филаментов
Регулярно повторяющиеся единицы, образующие миофибриллы и придающие им характерную исчерченостъ, - саркомеры - имеют длину около 2,5 мкм. При большом увеличении в миофибрилле можно видеть широкие темные и светлые полосы, а посередине каждой светлой полосы-плотную линию, которая отделяет один саркомер от другого и называется Z-линией (на срезе) или Z-диском (рис. 11-2).
Молекулярная основа поперечной исчерченности (послужившая ключом к пониманию функционального значения этой особенности) была выявлена в 1953 г. в одной из первых работ по электронной микроскопии биологического материала. Оказалось, что в состав каждого саркомера входят два набора параллельных, частично перекрывающихся филаментов: толстых, которые образуют темную полосу и тянутся от одного ее края до другого, и тонких, лежащих в области светлой полосы и частично проникающих в соседние темные полосы (рис. 11-2, В). Когда рассматривали поперечный срез миофибриллы в области, где толстые и тонкие филаменты перекрываются, можно было видеть, что толстые филаменты организованы в виде правильной гексагональной решетки, причем каждый толстый филамент окружен тонкими, тоже расположенными регулярно (рис. 11-3).

Рис. 11-1. Схематическое изображение небольшого отрезка клетки скелетной мышцы (называемой также мышечным волокном). У взрослого человека эти гигантские многоядерные клетки обычно имеют толщину около 50 мкм, а в длину могут достигать 500 000 мкм (50 мм).
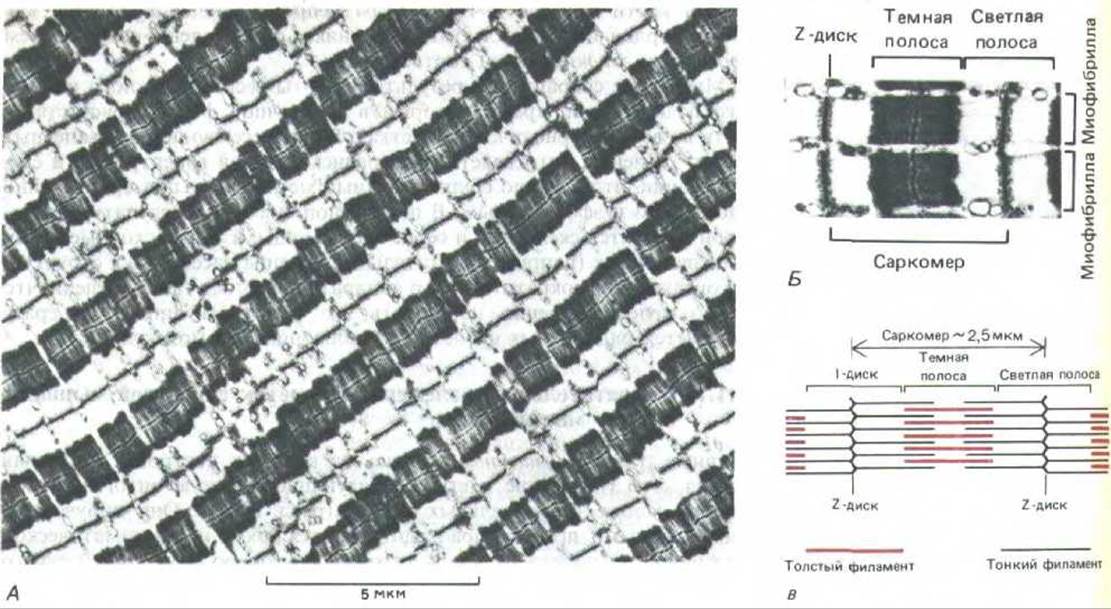
Рис. 11-2. А. Электронная микрофотография продольного среза через клетку скелетной мышцы кролика (при малом увеличении). Видна регулярная поперечная исчерченность. Клетка содержит множество параллельных миофибрилл (см. рис. 11-1). Б. Небольшой участок того же фото: показаны отрезки двух смежных миофибрилл и детали саркомера. В. Схема строения отдельного саркомера, объясняющая происхождение темных и светлых полос, которые видны на электронной микрофотографии. Темные полосы иногда называют полосами А, так как они выглядят анизотропными в поляризованном свете (т. е. их показатель преломления меняется с изменением плоскости поляризации). Светлые полосы относительно изотропны в поляризованном свете, и их иногда называют полосами I. (А и Б с любезного разрешения Roger Craig.)

Рис. 11-3. Электронные микрофотографии поперечного среза летательной мышцы насекомого. Видна кристаллоподобная упаковка толстых и тонких филаментов. У насекомых в отличие от позвоночных толстые филаменты имеют продольную центральную полость, что можно видеть при более сильном увеличении (справа). Сама геометрия гексагональной решетки в мышцах позвоночных тоже несколько иная. (J. Auber, J. de Microsc., 8: 197-232, 1969.)
11-3
11.1.3. Сокращение - результат скольжения тонких и толстых филаментов друг относительно друга [2]
Если через живую мышечную клетку пропустить пучок монохроматического света, возникнет интерференционная картина, позволяющая с большой точностью регистрировать изменения в длине саркомеров. Такие измерения показали, что при сокращении мышцы пропорционально укорачивается и каждый саркомер; если миофибрилла, состоящая из 20000 саркомеров, укорачивается с 5 см до 4 см (т.е. на 20%), длина каждого саркомера соответственно уменьшится с 2,5 до 2 мкм.
При укорочении саркомера сжимаются только светлые полосы - темная полоса своих размеров не меняет. Это можно легко объяснить, предположив, что сокращение вызывается скольжением тонких филаментов относительно толстых без изменения длины тех и других (рис. 11-4). Эта «модель скользящих нитей», впервые предложенная в 1954 г., сыграла решающую роль в понимании механизма мышечного сокращения. Она, в частности, привлекла внимание к молекулярным взаимодействиям, лежащим в основе взаимного скольжения соприкасающихся толстых и тонких филаментов.
Модель скользящих нитей базируется на нескольких группах экспериментальных данных. Электронномикроскопические исследования показали, что длина как толстых, так и тонких филаментов при укорочении мышцы не изменяется. Судя по данным рентгеноструктурного анализа, характер упаковки субъединиц, образующих филаменты, тоже остается неизменным. По мере укорочения мышцы развиваемое механическое усилие растет пропорционально степени перекрывания толстых и тонких филаментов; этого и следует ожидать, если усиление - результат взаимодействия нитей во всей области их соприкосновения.
Ультраструктурную основу этого взаимодействия удается выявить с помощью электронной микроскопии высокого разрешения. Оказалось, что от толстых филаментов отходят многочисленные боковые отростки, или поперечные мостики, соприкасающиеся с тонкими нитями, которые лежат на расстоянии около 13 нм от толстых (рис. 11-5). При сокращении мышцы толстые и тонкие филаменты подтягивают друг друга с помощью этих мостиков, работающих циклично, как миниатюрные весла.
Взаимодействующие белки тонких и толстых филаментов были идентифицированы как актин и миозин соответственно. Актин, которого в цитоскелете больше, чем какого-либо другого белка, часто образует вместе с миозином структуры, способные к сокращению. Хотя эти белки имеются почти во всех эукариотических клетках, большая часть наших знаний об их свойствах первоначально была получена в биохимических экспериментах с актином и миозином, выделенными из мышцы.
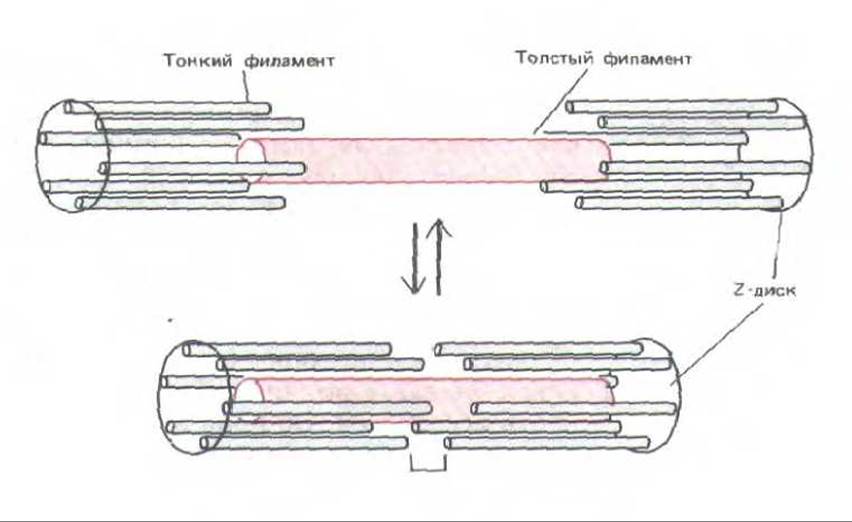
Рис. 11-4. Схема, иллюстрирующая процесе мышечного сокращения по принципу скользящих нитей; толстые и тонкие филаменты скользят друг по другу, не изменяя собственной длины.

Рис. 11-5. Продольный срез летательной мышцы насекомого (электронная микрофотография; препарат получен методом быстрого замораживания, скалывания и глубокого травления). Обратите внимание на почти кристаллическую укладку толстых миозиновых и тонких актиновых филаментов. Поперечные мостики, соединяющие нити двух типов, - головки миозина. (С любезного разрешения John Heuser и Roger Cooke.)
11.1.4. Тонкие филаменты состоят в основном из актина [2]
Актин имеется у всех эукариот, включая одноклеточных (например, у дрожжей). Гены актина эволюционно крайне консервативны, так что актины весьма далеких друг от друга организмов в опытах in vitro функционально взаимозаменяемы. Главные свойства актина, выделенного, например, из скелетных мышц позвоночных, являются общими| для актинов из любых других источников.
Обычно актин выделяют, обрабатывая порошок высушенной мышечной ткани сильно разбавленным солевым раствором, который вызывает диссоциацию актиновых филаментов на их глобулярные субъединицы. Каждая субъединица представляет собой одну полипептидную цепь длиной в 375 аминокислотных остатков, с которой нековалентно связана одна молекула АТР. Такой актин называют глобулярным, или G-актином. При полимеризации актина связанный АТР гидролизуется, отщепляя концевой фосфат, а актин образует филаменты, называемые фибриллярным актином (F-актином). Полимеризацию можно вызвать, просто повысив концентрацию соли до уровня, близкого к физиологическому; при этом раствор актина, лишь ненамного более вязкий, чем вода, быстро «густеет» по мере образования филаментов.
Хотя в процессе полимеризации и происходит гидролиз связанного АТР, сама полимеризация энергии не требует; она идет, даже если. с актином связан ADP или негидролизуемый аналог АТР. Однако гидролиз АТР оказывает существенное влияние на динамическое поведение актиновых филаментов; это мы увидим позже, когда будем рассматривать те виды клеточной активности, которые (в отличие от мышечного сокращения) зависят от контролируемой полимеризации и деполимеризации актина.
На электронных микрофотографиях актиновые филаменты выглядят как однородные нити толщиной около 8 нм (рис. 11-6). Эти нити составляют основу тонких филаментов скелетных мышц, что подтверждается данными электронной микроскопии, рентгеноструктурного анализа и окраски антителами к актину. Однако актин - не единственный компонент тонких филаментов, о чем будет сказано позже (разд. 11.1.12).
Актиновые филаменты представляют собой плотную спираль, собранную из однотипно ориентированных мономеров актина (рис. 11-7). Они обладают полярностью, т. е. два их конца различны. Эта полярность играет важную роль в осуществлении подвижности клеток и легче всего обнаруживается в ориентированных комплексах, которые каждый актиновый мономер образует с миозином. Но прежде чем обсуждать это ключевое взаимодействие, мы должны рассмотреть некоторые особенности молекул миозина.

Рис. 11-6. Электронные микрофотографии актиновых филаментов (негативное контрастирование). (С любезного разрешения Roger Craig.)
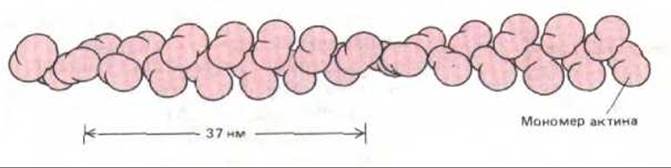
Рис 11-7. Организация глобулярных молекул актина в актиновом филаменте. Молекулы упакованы в плотную спираль; на один оборот приходится приблизительно два мономера актина. Хотя такое устройство создает видимость спирали из двух цепочек актина, обвивающих друг друга с шагом 37 нм, эта видимость ошибочна, так гипотетическая "одиночная" актиновая цепь сама по себе существовать не может.
11.1.5. Толстые филаменты состоят из миозина [2]
Миозин есть почти во всех клетках позвоночных и всегда находится в сократительных пучках, образуемых в цитоплазме актиновыми филаментами. Миозин - эволюционно гораздо менее консервативный белок, чем актин, и известно несколько его форм. При полимеризации in vitro миозин скелетных мышц, например, образует значительно более крупные филаменты, чем миозины немышечных клеток.
Миозин экстрагируют из скелетных мышц концентрированными солевыми растворами, под действием которых толстые филаменты деполимеризуются до составляющих их молекул миозина (рис. 11-8). Каждая молекула состоит из шести полипептидных цепей - двух одинаковых тяжелых цепей и двух пар легких цепей (рис. 11-9).
Протеолитический фермент папаин расщепляет молекулу миозина на длинный а-спиральный участок, называемый миозиновым стержнем (или миозиновым хвостом), и две раздельные глобулярные миозиновые головки, называемые также субфрагментами-1 или S1- фрагментами (рис. 11-10). Эти две части молекулы выполняют разные функции - хвост ответствен за самопроизвольную сборку толстых филаментов, а с помощью головок осуществляется движение этих филаментов относительно прилегающих актиновых нитей. Вначале мы опишем строение и самосборку хвостов, а затем рассмотрим, каким образом головки создают мышечное усилие.
11-4
11.1.6. Миозиновые хвосты самоорганизуются в биполярные толстые филаменты [3]
Подобно многим другим цитоскелетным белкам, хвосты миозина - это длинные стержневидные образования. Жесткость таких белков определяется наличием общего структурного элемента, в котором две а-спирали благодаря особому расположению гидрофобных аминокислотных остатков обвиваются друг около друга, образуя «скрученную спираль» (рис. 11-11). В миозине и во многих других белках цитоскелета эти две спирали направлены параллельно (ориентация N- и С-концов у них совпадает) и объединены в нить толщиной около 2 нм.
В то время как структура отдельных молекул миозина определяется гидрофобными взаимодействиями между двумя а-спиральными тяжелыми цепями (рис. 11 -11, A), структура толстых филаментов, образуемых миозином в мышце, зависит от ионных взаимодействий между хвостами. Именно поэтому растворы соли высокой концентрации, разрушающие ионные взаимодействия, но не влияющие на гидрофобные, экстрагируют из мышцы отдельные молекулы миозина. При снижении ионной силы раствора до физиологического уровня эти молекулы ассоциируют, образуя крупные филаменты, которые могут быть очень сходны с нормальными толстыми филаментами мышц. В мышечных клетках эти взаимодействия стабилизируются различными сопутствующими белками, и получающиеся в результате толстые филаменты образованы сотнями миозиновых хвостов, упакованных в плотные упорядоченные пучки, из которых торчат миозиновые головки расположенные «лесенкой» (рис. 11-12). Такая структура оказывается биполярной, с «голой» (без миозиновых головок) центральной областью, где соединяются противоположно направленные пучки миозиновых хвостов. Глобулярные головки миозина взаимодействуют с актином, образуя поперечные мостики между толстыми и тонкими филаментами.
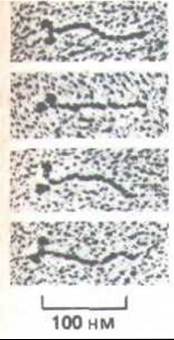
Рис. 11-8. Электронные микрофотографии молекул миозина (напыление платиной). Обратите внимание, что каждая молекула состоит из двух глобулярных головок, прикрепленных к фибриллярному хвосту (С любезного разрешения David Shotton.)

Рис. 11-9. Молекула миозина построена из двух тяжелых цепей (каждая длиной около 2000 аминокислотных остатков) и четырех легких цепей. Легкие цепи представлены молекулами двух типов (в одних около 190 аминокислотных остатков, в других около 170) - по одной молекуле каждого типа в каждой миозиновой головке.
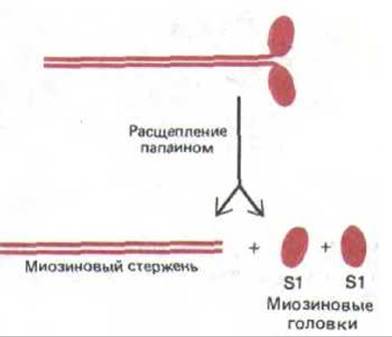
Рис. 11-10. При ограниченном расщеплении папаином молекула миозина распадается на стержень и две головки.
11-5
11.1.7. Источником энергии для мышечного сокращения служит гидролиз АТР [4]
Скелетная мышца превращает химическую энергию в механическую работу с весьма высокой эффективностью - в виде тепла теряется всего лишь 30-50% (для сравнения: тепловые потери при работе автомобильного двигателя составляют обычно 80-90% всей энергии, выделяющейся при сжигании бензина).
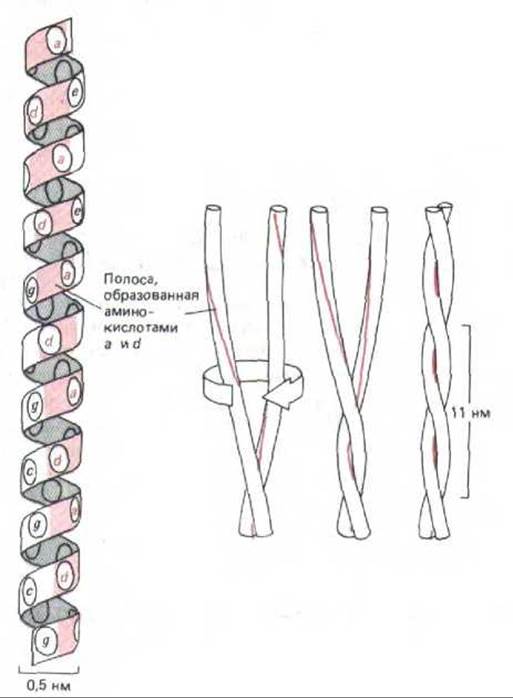
Рис. 11-11. Топология «скрученной спирали». Слева одиночная а-спираль представлена в виде цилиндра, где боковые цепи аминокислот обозначены семичленной последовательностью букв abcdefg (снизу вверх). Аминокислоты а и d в этой последовательности оказываются на поверхности цилиндра рядом, образуя «полосу» (выделена цветом), которая медленно оборачивается вокруг а-спирали. Белки, образующие скрученную спираль, как правило, имеют в положениях а и d гидрофобные аминокислоты. Поэтому, как показано справа, две а-спирали обвивают друг друга таким образом, что гидрофобные боковые цепи одной а-спирали попадают в пространство между гидрофобными боковыми цепями другой, тогда как более гидрофильные боковые цепи обращены к окружающей водной среде.
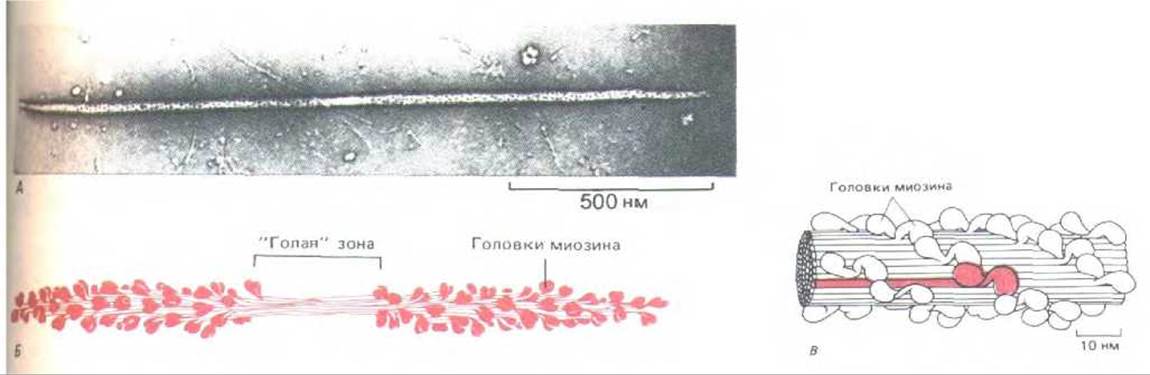
Рис. 11-12. Толстый миозиновый филамент. А. Электронная микрофотография толстого филамента из мышцы морского гребешка. Видна центральная «голая» зона. Б. Схема строения (без соблюдения масштаба). Молекулы миозина связаны хвостовыми участками в пучок, на поверхности которого выступают головки. «Голая» зона в центре содержит только хвосты миозина. В. Небольшой отрезок толстого филамента: реконструкция по электронным микрофотографиям. Одна из молекул миозина выделена цветом. (А-с любезного разрешения R. Craig; В-no R. A. Crowther, R. Pardon, R. Craig, J. Моl, Biol. 184: 429-439, 1985.)
Необходимую для мышечного сокращения энергию поставляет гидролиз АТР, однако содержание АТР в покоящейся и в активно работающей мышце различается мало, так как в мышечных клетках работает чрезвычайно эффективная система регенерации АТР. Фермент фосфокреатинкиназа катализирует реакцию между креатинфосфатом и ADP, в результате которой образуются АТР и креатин. (Креатин-фосфатвещество с еще большей энергией, чем АТР; рис. 11-13). После кратковременной вспышки мышечной активности падает внутриклеточный уровень именно креатинфосфата, хотя сам сократительный механизм использует АТР. Таким образом, креатинфосфат играет роль аккумулятора - он запасает энергию, «заряжаясь» за счет новых молекул АТР (синтезируемых при клеточных процессах окисления), когда мышца находится в покое.
11.1.8. Миозин действует как актин-зависимая АТРаза [5]
Происходящий при мышечном сокращении гидролиз АТР - прямое следствие взаимодействия между актином и миозином. Миозин и сам по себе действует как АТРаза, но в очищенном виде он работает сравнительно медленно. Для завершения полного цикла гидролиза одной молекулы АТР каждой молекуле миозина требуется примерно полминуты. При этом скорость-лимитирующей стадией оказывается не связывание АТР с миозином и не гидролиз концевой фосфатной связи (оба процесса протекают быстро), а освобождение продуктов гидролиза-ADP и неорганического фосфата - из комплекса с миозином. Оставаясь нековалентно связанными с его молекулой, они препятствуют присоединению и последующему гидролизу новых молекул АТР.
В присутствии актиновых филаментов АТРазная активность миозина резко возрастает. Каждая молекула миозина начинает гидролизовать от 5 до 10 молекул АТР в секунду, что сравнимо со скоростью гидролиза в сокращающейся мышце. Активация АТРазы миозина актиновыми филаментами отражает физическую ассоциацию этих белков, которая служит основой мышечного сокращения. Связывание миозина с актиновым филаментом ведет к быстрому отделению ADP и Pi от молекулы миозина, в результате чего последняя может связывать новые молекулы АТР и возобновлять цикл.
11.1.9. С актиновыми филаментами взаимодействуют головки миозина [6]
Как связывание с актиновыми филаментами, так и гидролиз АТР осуществляют глобулярные миозиновые головки. Изолированные головки, которые можно получить путем отщепления «хвостов» папаином (см. рис. 11-10), сохраняют и АТРазную активность, и актин-связывающие свойства интактных молекул миозина, поэтому их можно использовать для изучения взаимодействий между актином и миозином.

Рис. 11-13. Структура креатинфосфата. Это вещество играет роль «запасного аккумулятора» высоко-їнергетических фосфатных групп в мышцах и других тканях позвоночных. Фосфатная группа (выделена цветом) с помощью фермента греатинкиназы переносится на ADP с образованием АТР, когда в последнем возникает нужда.
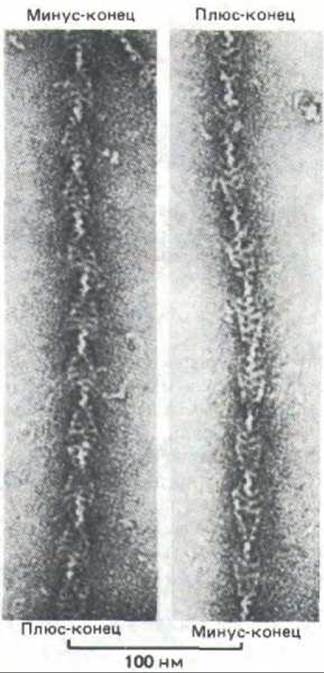
Рис. 11-14. Электронная микрофотография актиновых филаментов с присоединенными к ним изолированными головками миозина. Спиральное расположение связанных головок, повернутых в одном направлении, создает картину цепочки из наконечников стрел, выявляющую полярность актинового филамента. Конец, к которому обращены острия, называют минус-концом, а другой конец - плюс-концом, так как полимеризация актина на этих концах идет с различной скоростью (см. рис. 11-40). (С любезного разрешения R. Craig.)
Каждая молекула актина в составе актинового филамента способна связать одну миозиновую головку. Образующиеся при этом комплексы выдают структурную полярность актиновых филаментов; в электронном микроскопе негативно контрастированные препараты таких филаментов имеют весьма характерный вид: каждая миозиновая головка образует боковой выступ, и все множество этих выступов создает впечатление, что на филамент нанизаны наконечники стрел (рис. 11-14) Поскольку миозиновые головки присоединяются к каждой субъединице актина в одинаковой ориентации, такая картина означает, что все актиновые молекулы тоже ориентированы вдоль оси филамента в одном направлении. Таким образом, два конца актинового филамента структурно различаются. Их назвали соответственно минус-концом (или заостренным концом, т. е. тем, к которому направлены острия стрел) и плюс-концом (или оперенным концом, к которому обращены хвосты стрел). Термины «плюс» и «минус» связаны с тем фактом, что разные концы актинового филамента in vitro растут с различной скоростью (разд. 11.20.9).
Из рисунка 11-12 видно, что миозиновые головки, расположенные по разные стороны от центральной «голой» области толстого филамента, смотрят в противоположных направлениях. Так как головки должны взаимодействовать с тонкими филаментами в зоне перекрывания, сами тонкие филаменты с одной и с другой стороны саркомера должны иметь противоположную полярность. Это действительно удалось продемонстрировать, присоединяя миозиновые головки к актиновым филаментам, отходящим в обе стороны от изолированных Z-дисков: все миозиновые «стрелы» были направлены прочь от Z-диска. Таким образом, плюс-концы каждого актинового филамента закреплены в Z-диске, а минус-концы направлены в сторону толстых филаментов (рис. 11-15).
11.1.10. Миозиновые головки «шагают» по актиновому филаменту в направлении плюс-конца [7]
Мышца сокращается в результате взаимодействия головок миозина с прилегающими к ним актиновыми филаментами. В ходе этого взаимодействия миозиновые головки гидролизуют АТР. Гидролиз АТР и последующая диссоциация прочно связанных продуктов гидролиза (ADP и Рi) вызывают упорядоченную серию аллостерических изменений в конформации миозина. В итоге часть освобождающейся энергии превращается в двигательную работу. Общие принципы, лежащие в основе сопряжения гидролиза АТР с направленным перемещением белковых молекул, обсуждаются в разд. 3.4.11.
Анализ кинетики гидролиза АТР в процессе мышечного сокращения, данные электронной микроскопии и результаты рентгеноструктурного анализа указывают на вероятную последовательность событий, представленную на рис. 11-16. Свободная головка миозина связывает АТР (состояние 1) и гидролизует его. Этот процесс обратим, так как энергия гидролиза АТР первоначально запасается в напряженной конформации белка (когда ADP и PJ остаются связанными с ним - состояние 2). Переходя поочередно в то или другое из этих состояний, миозиновая головка в результате случайных движений может приблизиться к соседней субъединице актина и слабо связаться с ней; это приводит к освобождению Pi, что в свою очередь ведет к прочному связыванию головки с актиновым филаментом (состояние 3). В этом состоянии головка претерпевает конформационное изменение, которое и производит элементарный силовой акт, участвующий в подтягивании всего толстого филамента. В конце этого «рабочего хода» (состояние 4) происходит отделение ADP от головки, а затем присоединение к ней новой молекулы АТР, отделяющее головку от актинового филамента и возвращающее ее в состояние 1. Далее гидролиз связанного АТР подготавливает миозиновую головку к следующему циклу.
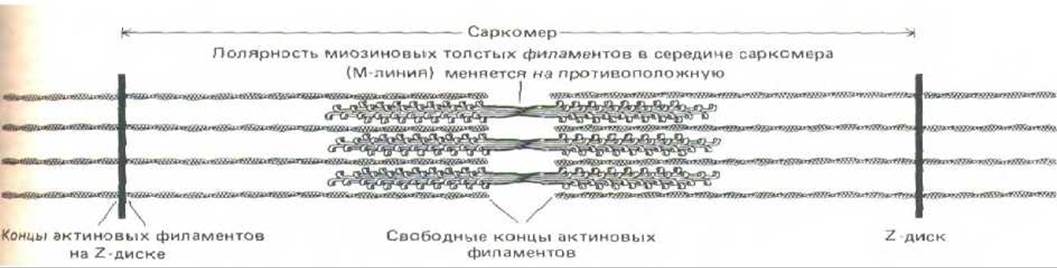
Рис. 11-15. Тонкие и толстые филаменты в саркомере перекрываются, причем их полярность симметрична относительно средней линии саркомера.
Поскольку каждый оборот цикла приводит к гидролизу и освобождению одной молекулы АТР, вся эта серия конформационных изменений связана с большим положительным изменением свободной энергии системы, что делает весь процесс однонаправленным (см. разд. 3.4.11). Поэтому каждая отдельная головка миозина «шагает» по актиновому филаменту в одном направлении - всегда в сторону плюс-концов (см. рис. 11-15). При циклических изменениях своей конформации головка тянет актиновый филамент, заставляя его скользить относительно миозинового; в те моменты, когда головка не контактирует с актином, она смещается за счет работы других миозиновых головок того же филамента. На «моментальном снимке» всего миозинового филамента в сокращающейся мышце было бы видно, что часть его головок находится в контакте с актиновыми филаментами, а часть остается свободной (для этого весьма существенна эластичность, «пружинистость» молекулы миозина). На каждом толстом филаменте сидит около 500 миозиновых головок, и каждая головка при быстром сокращении мышцы проходит примерно 5 рабочих циклов за секунду; в результат скорость скольжения тонких филаментов относительно толстых достигает 15 мкм/с.
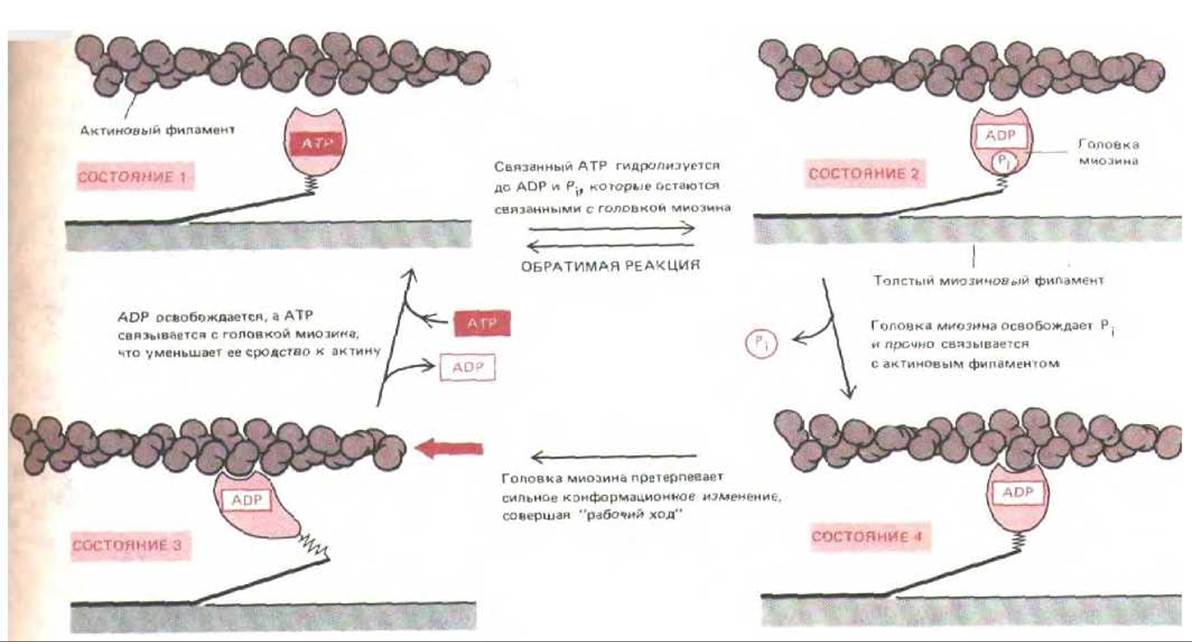
Рис. 11-16. Эта схема показывает, каким образом молекула миозина может использовать энергию гидролиза АТР, чтобы двигаться по актвому филаменту от его минус-конца к плюс-концу. При переходе из состояния 2 в состояние 3 присоединение миозиновой голов к актину приводит к тому, что она теряет связанный с ней фосфат и более прочно прикрепляется актиновому филаменту. Вслед за этим форма головки претерпевает пока еще не очень понятные изменения, которые сопровождаются высвобождением ADP и заставляют миозиновую головку «подтянуться» относительно актинового филамента (рабочий ход). Каждая из пары головок на молекуле миозина работает независимо от другой.
11.1.11. Мышечное сокращение инициируется внезапным повышением концентрации Са2+ в цитозоле [8]
Только что описанный молекулярный механизм создания силы включается лишь тогда, когда мышца получает сигнал от своего мотонейрона. Нервный импульс вызывает на плазматической мембране мышечной клетки потенциал действия, и в результате электрическое возбуждение быстро распространяется по серии мембранных впячиваний, называемых поперечными трубочками (Т-трубочками), которые отходят внутрь от плазматической мембраны, вступая в контакт с каждой миофибриллой. Отсюда сигнал каким-то образом передается саркоплазматическому ретикулуму - своеобразной оболочке из сообщающихся уплощенных пузырьков, которая окружает каждую миофибриллу подобно сетчатому чулку (рис. 11-17).
Щель между Т-трубочкой и саркоплазматическим ретикулумом имеет ширину всего лишь 10-20 нм, но как через нее передается сигнал, остается неясным. Электрическое возбуждение Т-трубочек приводит (неизвестным пока способом) к открытию в мембране саркоплазматического ретикулума кальциевых каналов (рис. 11-17), и ионы Са2+, которых в ретикулуме очень много, выходят в цитозоль. Именно этот внезапный подъем концентрации свободных ионов Са2+ в цитозоле вызывает сокращение миофибрилл. Так как время прохождения сигнала от плазматической мембраны через Т-трубочки и саркоплазматический ретикулум до каждого из саркомеров измеряется миллисекундами, сокращение всех миофибрилл в клетке происходит одновременно. Повышение концентрации Са2+ в цитозоле кратковременно, поскольку ионы Са2+ быстро перекачиваются обратно в саркоплазматический ретикулум Са2+ -АТРазой, которой в его мембране очень много (разд. 6.4.7). Обычно возвращение концентрации Са2+ в цитозоле к уровню покоя происходит за 30 мс, что приводит к расслаблению миофибрилл.

Рис. 11-17. Система мембран, передающая сигнал к сокращению от плазматической мембраны мышечной клетки ко всем ее миофибриллам. На электронной микрофотографии видны две Т-трубочки и большие каналы для выброса Са2+ в мембране саркоплазматического ретикулума, которые выглядят как прямоугольные «ножки», соединенные с мембраной соседней Т-трубочки. (Микрофотографию любезно предоставила Clara Ftanzini-Armstrong.)

Рис. 11-18. Здесь показано, каким образом на актиноном филаменте расположены тропомиозин и тропонин. Каждая молекула тропомиозина имеет семь регулярно расположенных участков с гомологичной последовательностью; как полагают, каждый такой участок связывается с мономером актина. Обратите внимание, что концы соседних молекул тропомиозина слегка перекрываются, как если бы они полимеризовались вдоль актинового филамента «головой к хвосту». (По G.N. Phillips, J.P. Fillers, С. Cohen, J. Моl. Biol. 192: 111-131, 1986, с изменениями.)
11.1.12. Сокращение скелетной мышцы регулируется ионами Са2+ при участии тропонина и тропомиозина [9]
Зависимость сокращения скелетной мышцы позвоночного от ионов Са2+ (и тем самым - от команд, передаваемых нервами) всецело определяется наличием специализированных вспомогательных белков, тесно связанных с актиновыми филаментами. Если миозин смешать в пробирке с очищенными актиновыми филаментами, АТРаза миозина активируется независимо от присутствия Са2+, тогда как в нормальной миофибрилле, где на актиновых филаментах «сидят» вспомогательные белки, активация миозиновой АТРазы зависит от Са2+.
Один из этих белков, названный тропомиозином (из-за сходства его с миозином на рентгеновских дифрактограммах), - жесткая стержневидная молекула длиной 41 нм. Как и хвост миозина, тропомиозин представляет собой димер, состоящий из двух одинаковых а-спиральных цепей по 284 аминокислоты в каждой. Цепи обвиваются друг около друга (см. разд. 11.1.6). Связываясь с актиновым филаментом по всей его длине, он стабилизирует филамент и придает ему жесткость (рис. 11-18).
Другой важный вспомогательный белок, участвующий в регулировании функции скелетных мышц позвоночных ионами кальция, - это тропонин. Он представляет собой комплекс из трех полипептидов-тропонинов Т, I и С (названных так за свои тропомиозин-связывающие, ингибиторные и Са2+-связывающие свойства соответственно). Тропониновый комплекс имеет удлиненную форму, причем субъединицы С и I образуют глобулярную головку, а тропонин Т-длинный хвост. Хвост тропонина Т связывается с тропомиозином и, как полагают, определяет положение всего комплекса на тонком филаменте (рис. 11-18). Тропонин I присоединяется к актину, и если его добавить к тропонину Т и тропомиозину, то образуемый ими комплекс будет ингибировать взаимодействие актина с миозином даже в присутствии Са2+.
Если же, наконец, добавить тропонин С и достроить таким образом тропониновый комплекс, его влияние на актин-миозиновые взаимодействия станет чувствительным к Са2+. Тропонин С способен связывать до четырех ионов Са2+, и в комплексе с Са2+ он ослабляет ингибирующее действие двух других компонентов тропонина на связывание миозина с актином. Тропонин С-близкий «родственник» кальмодулина - белка, который участвует в Са2+-зависимых ответах всех клеток, в том числе в активации миозина в гладких мышцах (разд. 11.1.15). Поэтому тропонин С можно рассматривать как специализированную форму кальмодулина, приобретшую участки стабильного связывания с тропонином I и тропонином Т и обеспечивающую тем самым способность миофибрилл чрезвычайно быстро реагировать на повышение концентрации Са2+.
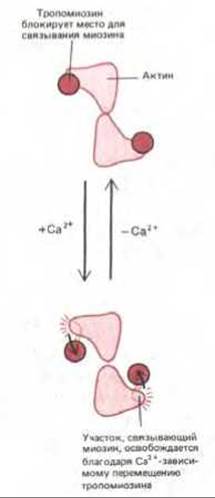
Рис. 11-19. Актиновый филамент в поперечном разрезе (схема): показано, каким образом в отсутствие Са2+ тропомиозин может блокировать взаимодействие миозиновых головок с актином.
На каждые семь мономеров актина в актиновом филаменте приходится только один тропониновый комплекс (рис. 11-18). Судя по данным структурных исследований, в покоящейся мышце связывание тропонина I с актином ведет к перемещению тропомиозина на актиновом филаменте в то самое место, с которым в сокращающейся мышце контактируют миозиновые головки, и в результате взаимодействие актина с миозином подавляется. При повышении уровня Са2+ тропонин С заставляет тропонин I «отцепиться» от актина, таким образом позволяя тропомиозину слегка изменить свое положение, и участок взаимодействия головок актина с миозином освобождается (рис. 11-19).
11.1.13. Другие вспомогательные белки поддерживают архитектуру миофибрилл и обеспечивают их эластичность [10]
Удивительная сила и быстрота мышечного сокращения обусловлена тем, что в каждой миофибрилле актиновые и миозиновые филаменты находятся на оптимальном расстоянии друг от друга и в правильном расположении. Тонкую организацию миофибрилл обеспечивает группа структурных белков, из которых больше дюжины уже идентифицировано (табл. 11-1), Локализация большинства этих белков в саркомере была выяснена иммуноцитохимическими методами (разд. 4.5.3).
Таблица 11-1. Компоненты миофибрилл скелетных мышц позвоночных1)
|
Белок |
Доля общего белка, % |
Мол. масса |
Субъединицы, мол. масса |
Функция |
|
Миозин |
44 |
510 |
2 х 223 (тяжелые цепи) |
Главный компонент толстых филаментов. Взаимодействует с актиновыми филаментами, создавая механическое усилие за счет гидролиза АТР |
|
Актин |
22 |
42 |
- |
Главный компонент тонких филаментов, по которым скользят толстые филаменты при мышечном сокращении |
|
Тропомиозин |
5 |
64 |
2 х 32 |
Стержневидный белок, который связывается с актиновыми филаментами по всей их длине |
|
Тропонин |
5 |
78 |
30 (Тn = Т) 30 (Тn = I) 18 (Тn = С) |
Комплекс из трех мышечных белков, расположен через равные интервалы на актиновых филаментах и участвует в регуляции мышечного сокращения ионами Са2+ |
|
Титин |
9 |
~2500 |
- |
Очень большой гибкий белок, образует эластичную цепь, соединяющую толстые филаменты с Z-дисками |
|
Небулин |
3 |
600 |
- |
Удлиненный нерастяжимый белок, связанный с Z-диском и ориентированный параллельно актиновым филаментам |
|
а-Актинин |
1 |
190 |
2 х 95 |
Актин-связывающий белок, который соединяет актиновые филаменты в области Z-диска. |
|
Миомезин |
1 |
185 |
- |
Миозин-связывающий белок, находящийся в области центральной М-линии толстых филаментов |
|
С-белок |
1 |
140 |
- |
Миозин-связывающий белок; образует полосы по обе стороны от М-линии толстых филаментов. |

Рис. 11-20. Электронная микрофотография молекул очищенного а-актинина (любезно предоставлена J. Heuser.)
Актиновые филаменты «заякорены» своими плюс-концами в Z-диске, где их удерживают в правильно организованной решетке другие белки. Из них лучше всего охарактеризован а-актинин - актин-связывающий белок, имеющийся в большинстве животных клеток. В мышечных клетках он находится в области Z-диска. Очищенный а-актинин - биполярная палочковидная молекула (рис. 11-20), которая может связывать актиновые филаменты в параллельные пучки. Аналогичную функцию в случае миозина может выполнять белок миомезин, который сшивает соседние миозиновые филаменты в области М-линии (посередине биполярного толстого филамента), собирая их в гексагональную упаковку. Стабилизирует упаковку миозиновых филаментов еще одна группа миозин-связывающих белков, выявляемых при окраске антителами как серия из 11 регулярно расположенных бледных полосок по обе стороны от М-линии.
В мышечных клетках есть также целая система очень плохо растворимых белковых филаментов, которые можно выделить лишь после полной экстракции миозина и актина из саркомера концентрированным раствором йодистого калия. Одна группа таких филаментов, построенных из очень крупного белка, названного титином, тянется параллельно толстым и тонким филаментам и соединяет толстые филаменты с Z-диском. Титиновые филаменты очень эластичны и, по-видимому, действуют как пружины, «центрируя» толстые филаменты между Z-дисками (рис. 11-21). Еще одна группа нерастворимых нитей - это промежуточные филаменты (разд. 11.5), которые расположены между Z-дисками соседних миофибрилл. Предполагается, что они удерживают саркомеры в определенных пространственных отношениях между собой и соединяют миофибриллы с плазматической мембраной мышечной клетки.
11.1.14. У позвоночных есть три основных типа мышц [11]
До сих пор мы рассматривали лишь один из трех главных типов мышц, имеющихся у позвоночных, а именно скелетные мышцы. Два других - это сердечная мышца, которая за среднее время жизни человека успевает совершить около трех миллиардов циклов сокращения и расслабления, и гладкая мускулатура, обеспечивающая более медленное и продолжительное сокращение, характерное для таких органов, как кишечник. Во всех трех типах мышечных клеток, а также в еще одном типе сократимых клеток - миоэпителиалъных клетках (см. разд. 17,6) - работает механизм скользящих нитей.
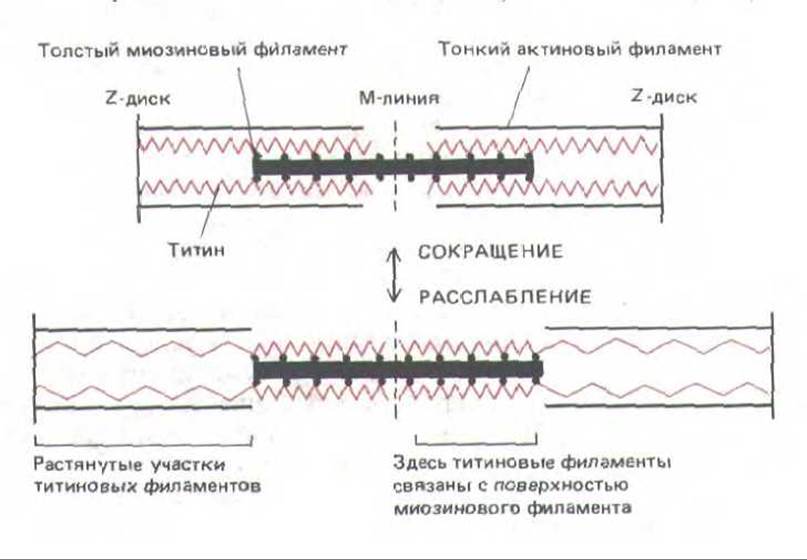
Рис. 11-21. Сеть из нитей титина, которые, как предполагается, соединяют в саркомерах скелетных мышц толстые миозиновые филаменты с Z-дисками. Эластичные титиновые нити, по-видимому, присоединены к толстым филаментам вдоль всей их поверхности, так что свободно изменять длину и обусловливать эластичность саркомера может только отрезок нити между концом толстого филамента и Z-диском. Такая упругая сеть удерживает толстые филаменты точно посередине между Z-дисками и позволяет мышцам растягиваться за пределы области перекрывания толстых и тонких филаментов без разрушения саркомера. Поперечные мостики между толстыми и тонкими филаментами для простоты не показаны. (По К. Wang, J. Wright, J. Cell Biol. 107: 2199-2212, 1988.)
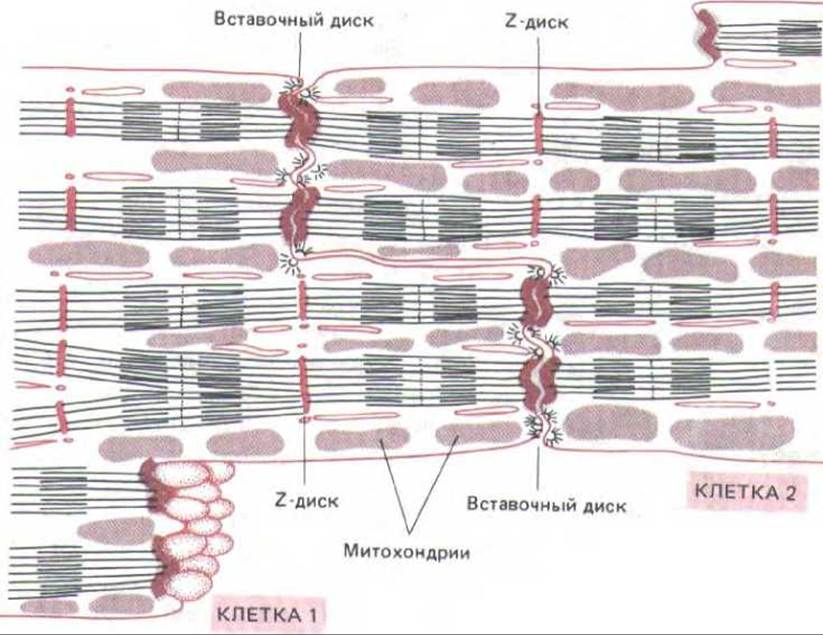
Рис. 11-22. Структура сердечной мышцы. Сердечная мышца состоит из множества отдельных клеток, каждая со своим ядром. Эти клетки соединены между собой с помощью специальных контактов, называемых вставочными дисками. В зоне каждого вставочного диска актиновые филаменты саркомеров соседних клеток входят в плотное вещество, связанное с плазматической мембраной, как если бы это был Z-диск. Таким образом, миофибриллы тянутся в мышце, игнорируя границы клеток.
Подобно скелетным мышцам, сердечная мышца выглядит исчерченной (поперечнополосатой), что отражает весьма сходную организацию актиновых и миозиновых филаментов. Сокращение тоже запускается сходным механизмом: потенциал действия, достигнув Т- трубочек, вызывает выброс из саркоплазматического ретикулума Са2+, который с помощью тропонин-тропомиозинового комплекса стимулирует сокращение. Однако клетки сердечной мышцы не являются многоядерными и соединены между собой конец в конец специальными вставочными дисками (рис. 11-22). Вставочные диски выполняют по крайней мере три функции: 1) они соединяют при помощи десмосом (разд. 14.1.4) каждую клетку со следующей; 2) они связывают тонкие филаменты, входящие в состав миофибрилл соседних клеток (играя роль, аналогичную роли Z-дисков внутри клетки); 3) в них находятся щелевые контакты (разд. 14.1.5), через которые потенциал действия быстро распространяется от клетки к клетке, синхронизируя их сокращение.
Наиболее «примитивная» мышца - в том смысле, что она имеет наибольшее сходство с немышечными клетками - лишена исчерченности, откуда ее название «гладкая» мышца. Она образует сократимые структуры желудка, кишки, матки, стенок артерий, железистых протоков и многих других частей тела, где необходимо медленное и продолжительное сокращение. Гладкомышечная ткань состоит из слоев удлиненных веретенообразных клеток, в каждой из которых одно ядро. В клетках есть и толстые, и тонкие филаменты, но они не организованы в столь упорядоченные структуры, как в скелетной мускулатуре и в сердце (в частности, они не образуют отдельных миофибрилл). Филаменты сократительного аппарата гладкомышечных клеток распределены более диффузно, хотя в основном они вытянуты вдоль длинной оси клетки, соприкасаясь под косым углом с плазматической мембраной в дисковидных контактах, соединяющих группы клеток вместе.
Сократительный аппарат гладкой мускулатуры неспособен к такому быстрому сокращению, как миофибриллы поперечнополосатых мышц. Однако он имеет то преимущество, что допускает гораздо большую степень укорочения и может поэтому осуществлять значительные перемещения, несмотря на отсутствие такой системы рычагов, как кости. Благодаря какой организации актиновых филаментов и миозина это становится возможным, пока не ясно; одна из гипотетических моделей представлена на рис. 11-23.
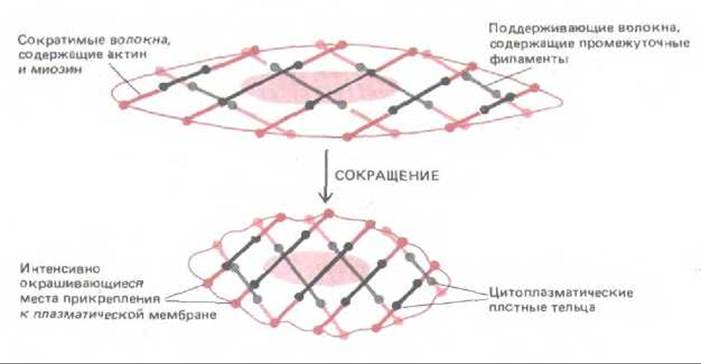
Рис. 11-23, Модель сократительного аппарата гладкомышечной клетки. На этой гипотетической схеме пучки сократительных филаментов, содержащих антин и миозин, присоединены одним концом к плазматической мембране, а другим концом - к несократимым пучкам промежуточных филаментов через цитоплазматические плотные тельца. Сократительные актомиозиновые пучки расположены с наклоном к длинной оси клетки (которая обычно гораздо сильнее вытянута, чем показано на схеме), и их сокращение намного укорачивает клетку. Показана только небольшая часть всех пучков.
11.1.15. И в гладкомышечных, и в немышечных клетках миозин активируется фосфорилированием его легких цепей [12]
Высокоспециализированные сократительные механизмы мышечных клеток, которые мы здесь рассмотрели, произошли от более простых силовых механизмов, имеющихся во всех эукариотических клетках. В связи с этим неудивительно то, что миозин немышечных клеток наиболее сходен с миозином гладких мышц - наименее специализированного типа мускулатуры. В клетках этого типа сокращение запускается повышением концентрации Са2+ в цитозоле (так же как и в клетках сердечной и скелетных мышц), однако ионы Са2+ действуют тут не через тропонин-тропомиозиновый комплекс. Инициация сокращения происходит главным образом за счет фосфорилирования одной из двух цепей молекулы миозина, что контролирует взаимодействие миозина с актином.
Две легкие цепи миозина, входящие в состав каждой миозиновой головки (см. рис. 11-9), неодинаковы, и при сокращении гладкомышечных и немышечных клеток фосфорилируется лишь одна из них. Когда она фосфорилирована, головка миозина может взаимодействовать с актиновым филаментом, что приводит к сокращению; при дефосфорилировании этой легкой цепи миозиновая головка стремится отделиться от актина, становясь тем самым неактивной. Это фосфорилирование катализируется специальным ферментом - киназоп легких цепей миозина, которая становится активной, лишь связываясь с комплексом Са2+-кальмодулин (разд. 12.4.3). Таким образом, сокращение здесь тоже находится под контролем концентрации Са2+ в цитозоле (рис. 11-24). Фосфорилирование происходит сравнительно медленно, так что максимальное сокращение развивается нередко за время порядка секунды (в поперечнополосатых мышцах - за несколько миллисекунд), но для гладкомышечных и немышечных клеток быстрая активация сокращения и не нужна.
Миозин этих клеток гидролизует АТР примерно в 10 раз медленнее, чем миозин скелетных мышц, что отражается, естественно, на скорости «шагания» его по актиновым филаментам и быстроте сокращения в целом. Однако не следует рассматривать гладкомышечные клетки как «плохой», медленно работающий вариант клеток скелетных мышц, пригодный на что-то только потому, что к этим клеткам предъявляется меньше требований. Они специально приспособлены для медленного продолжительного сокращения и способны поддерживать напряжение длительное время, гидролизуя при этом в 5-10 раз меньше АТР, чем требовалось бы для выполнения такой же задачи клеткам скелетных мышц. Кроме того, сокращение гладких мышц контролируется большим набором разнообразных сигналов, в том числе импульсами, приходящими от вегетативной нервной системы, и гормонами (например, адреналином). Многие из этих сигналов действуют через киназу легких цепей миозина. Так, во многих клетках адреналин, повышая уровень циклического AMP, вызывает фосфорилирование этой киназы, что резко уменьшает ее сродство к Са2+-кальмодулиновому комплексу; тем самым адреналин ингибирует фосфорилирование легких цепей миозина, заставляя гладкомышечную клетку расслабляться.

Рис. 11-24. Сокращение гладкой мышцы активируется в присутствии Са2+ с помощью киназы легких цепей миозина, фосфорилирующей определенный участок одного из двух типов легких цепей в миозине. Регуляция немышечного миозина осуществляется таким же образом (см. рис. 11-25).
11.1.16. При фосфорилировании легких цепей немышечный миозив способен объединяться в филаменты [13]
Хотя миозин есть практически во всех эукариотических клетках, стабильные толстые филаменты он образует только в сердечной и скелетных мышцах. Молекулы миозина в немышечных клетках собраны в меньшие комплексы в зависимости от обстоятельств; размеры и местоположение этих сократительных систем определяются внутриклеточными сигналами. Важным фактором, регулирующим степень агрегации миозина, служит его фосфорилирование киназой легких цепей, которое влияет не только на АТРазную активность миозина, но также на его форму и способность к самосборке.
Если немышечный миозин дефосфорилировать путем обработки фосфатазой, он становится легко растворимым. Седиментационный анализ показал, что единичные молекулы растворимого миозина имеют компактную конфигурацию, и, судя по данным электронной микроскопии, каждый миозиновый хвост складывается с самим собой, цепляясь за «липкий участок» на головке. В этой свернутой конформации миозиновые молекулы не способны эффективно образовывать филаменты. Когда киназа легких цепей миозина фосфорилирует головки, они теряют «липкость», хвосты освобождаются, распрямляются и могут ассоциировать друг с другом, образуя биполярные миозиновые филаменты (рис. 11-25 и 11-26).

Рис. 11-25. Сборка филаментов немышечного миозина контролируется фосфорилированием его легких цепей. Фосфорилирование вызывает два эффекта: оно изменяет конформацию миозиновой головки таким образом, что на ней обнажается актин-связывающий участок, и высвобождает миозиновый хвост из «липкого кармана» на миозиновой головке, тем самым позволяя молекулам миозина объединяться в короткие биполярные филаменты. Точно так же ведет себя гладкомышечный миозин.

Рис. 11-26. Короткие филаменты немышечного миозина, образовавшиеся в результате фосфорилирования его легких цепей (электронная микрофотография, негативный контраст). (С любезного разрешения John Kendrick-Jones.)

Рис. 11-27. Примеры встречающихся в немышечных клетках сократительных пучков актиновых филаментов, в состав которых входит также миозин.
11.1.17. В немышечных клетках могут временно создаваться сократимые комплексы мышечного типа [14]
Для немышечных клеток контроль над сборкой и разборкой миозиновых комплексов имеет особое значение, так как в них сократительные структуры из актиновых филаментов и миозина нередко образуются лишь для выполнения какой-нибудь специальной функции, после чего снова разбираются. В частности, при делении клетки под ее мембраной появляется так называемое сократимое кольцо - поясок из актиновых филаментов и миозина. Именно за счет его сокращения посередине клетки образуется перетяжка, что ведет затем к разъединению двух дочерних клеток (рис. 11-27; см. также разд. 13.5.14). Поскольку сократительное кольцо не является постоянной клеточной структурой, оно должно формироваться в начале деления. Этот процесс можно наблюдать, окрашивая делящиеся клетки флуоресцентными антителами к миозину. Например, в готовых к делению яйцах морского ежа молекулы миозина вначале равномерно распределены под плазматической мембраной, а затем, по мере образования сократительного кольца, мигрируют в экваториальную область; распределение их снова становится дисперсным, когда деление клетки завершилось. Каким образом этот процесс контролируется - неизвестно.
Другой пример временно существующих сократимых структур - это так называемые стрессовые волокна (или нити), характерные элементы цитоскелета культивируемых фибробластов (см. рис. 11-27). И по своей структуре, и по функциям они напоминают тонкие миофибриллы (рис. 11-28). Одним концом эти волокна связаны с плазматической мембраной в особых участках, называемых фокальными контактами (см. разд. 11.2.8), и похожи по составу и ультраструктуре на участки присоединения к плазматической мембране актиновых филаментов в клетках гладких мышц (см. рис. 11-23). Другим концом они связаны либо с густой сетью промежуточных филаментов, окружающей ядро клетки (см. рис. 9-1), либо с другим фокальным контактом. Стрессовые волокна образуются при механическом растяжении клетки (например, когда она распластывается по субстрату) и исчезают во время митоза, когда клетка округляется и теряет связь с субстратом. Если ликвидировать натяжение, «оторвав» лазерным лучом один конец стрессового волокна от фокального контакта, оторванное волокно тоже быстро исчезнет. Стрессовые волокна фибробластов, находящихся в тканях, судя по всему, способны сокращаться, передавая создаваемое усилие на окружающий коллагеновый матрикс; этот процесс играет большую роль в заживлении ран и в морфогенезе.
Некоторые сократительные структуры на основе актиновых филаментов оказываются более долгоживущими. Таковы, например, кольце вые пучки актиновых филаментов в опоясывающих десмосомах, расположенных вблизи апикальной поверхности клеток эпителия (разд. 14.1.3). Среди прочих функций, эти пучки, видимо, играют важную роль в изгибании эпителиальных пластов в ходе эмбриогенеза (разд. 11.6.9).

Рис. 11-28. Электронная микрофотография фибробласта в культуре (окраска антителами, меченными коллоидным золотом). Видно, что организация белков в стрессовых волокнах напоминает мышечную. Показано расположение двух типов актин-связывающих белков: а-актинин (крупные частицы золота) ассоциирован с периодически повторяющимися плотными участками в стрессовых волокнах (в поперечнополосатой мышце а -актинин находится в Z-дисках), тогда как головки миозина (мелкие частицы золота) видны по обе стороны от полос с а-актинином. Такая организация имеет некоторое сходство с саркомером (сравните с рис. 11-2) и указывает на то, что молекулы миозина здесь собраны в филаменты. (Фото любезно предоставлено М. de Brabander, J. de Mey, G. Langanger.)
11.1.18. Мышечные белки кодируются генами, составляющими мультигенные семейства [15]
Как мы видели, в мышечных клетках всех трех типов, а также в немышечных клетках сократительный аппарат имеет много общих черт, Различные типы сокращения, свойственные разным клеткам, отчасти определяются тканеспецифичностью экспрессии генов, кодирующих белки этого аппарата. У млекопитающих, например, имеются по меньшей мере шесть генов актина, шесть генов тяжелой цепи миозина, три тропомиозиновых гена и три гена тропонина Т. В некоторых случаях кодируемые разными генами белки несколько различаются по функции в других же случаях функциональных различий пока не обнаружено.
Из шести вариантов актина, экспрессируемых у млекопитающих один содержится только в скелетных мышцах, другой - в сердечной мышце, а еще два - только в гладкомышечных клетках (первый из них - в гладкой мускулатуре сосудов, а второй в мускулатуре других органов); и наконец, два последних варианта, известные как немышечные, или цитоплазматические, актины, являются, по-видимому, универсальными компонентами цитоскелета и в значительных количествах присутствуют в большинстве немышечных клеток. Все эти виды, или изоформы, актина очень сходны по аминокислотным последовательностям; например, мышечные актины отличаются от цитоплазматических менее чем по 7% аминокислот. Если не считать некоторых различий в N-концевой части молекулы, возможно, влияющих на процесс полимеризации актина, не ясно, имеют ли такие различия какое-либо функциональное значение, Экспрессия гена «сердечного» актина в культивируемых фибробластах не изменяет ни форму, ни поведение клеток, и синтезируемый белок легко включается в их нормальные актиновые структуры. Напротив, различия между миозинами влияют и на скорость сокращения, и на его регуляцию, а также на степень ассоциации молекул миозина в клетке.
11.1.19. Разнообразие мышечных белков увеличивается за счет альтернативных способов сплайсинга их мРНК [16]
Все сказанное выше о различных типах мышц дает лишь частичное представление об их реально существующем разнообразии. В скелетных мышцах взрослого человека, например, мы находим смесь мышечных клеток трех типов: белые мышечные клетки, приспособленные для быстрого анаэробного сокращения (АТР синтезируется в них в основном за счет гликолиза); красные мышечные клетки, специализированные для медленного и более продолжительного сокращения и использующие главным образом аэробный метаболизм (их цвет обусловлен высокой концентрацией запасающего кислород белка - миоглобина); и наконец, мышечные клетки промежуточного типа, синтезирующие АТР как аэробным, так и анаэробным путем (разд. 2.3.2). В каждом из этих типов есть еще подтипы, с помощью которых происходит «тонкая настройка» каждой мышцы на выполнение характерных для нее физиологических функций и на соответствующий метаболизм. При этом одни и те же мышцы у взрослого человека и у плода различны.
Белковый состав каждого из этих типов мышц имеет свои особенности. Очень важным источником разнообразия служит тканеспецифическая регуляция сплайсинга пре-мРНК, позволяющая комбинировать различные наборы экзонов, так что продуктами одного гена могут быть несколько слегка различающихся молекул мРНК (разд. 10.4.2). Характер сплайсинга пре-мРНК может изменяться под действием гормональных, нервных и иных факторов, и в результате изменяются аминокислотные последовательности определенных мышечных белков в зависимости от ткани и стадии онтогенеза. Например, ген тропонина Т, который экспрессируется в скелетных мышцах, благодаря альтернативному сплайсингу РНК дает по меньшей мере 10 различных форм белка. Эти варианты, вероятно, по-разному взаимодействуют с тропонином С и тропомиозином, модифицируя таким образом регуляцию мышечного сокращения.
Заключение
Сокращение мышц происходит в результате скольжения актиновых филаментов вдоль миозиновых. Головки молекул миозина, выступающие по бокам миозиновых филаментов, осуществляют АТР-зависимый цикл, в котором присоединяются к соседним актиновым филаментам, изменяют свою конформацию таким образом, что заставляют актиновые и миозиновые филаменты смещаться относительно друг друга, а затем снова отделяются от нитей актина. Эффективной работе этого цикла способствуют специальные вспомогательные белки, которые поддерживают пространственную организацию актиновых и миозиновых филаментов в виде параллельных, частично перекрывающихся пучков с правильной взаимной ориентацией и оптимальным расстоянием между ними. Еще два вспомогательных белка-тропонин и тропомиозин - обеспечивают регуляцию сокращения скелетных и сердечной мышц ионами Са2+.
Актин и миозин присутствуют также и в гладких мышцах, и в большинстве немышечных клеток. Сокращение в них осуществляется по тому же принципу, что и в сердечной и скелетных мышцах, но элементарные сократимые блоки здесь мельче и не обладают столь высокой степенью упорядоченности; кроме того, их активность и степень ассоциации находятся под контролем Са2+ -зависимого фосфорилирования одной из легких цепей миозина.
Сократительный аппарат мышечных и немышечных клеток точно настроен на выполнение специфических функций в зависимости от типа клеток. Это определяется тканеспецифическоп экспрессией различных генов, кодирующих мышечные белки, и тканеспецифической же регуляцией сплайсинга мРНК, благодаря которой один ген может давать слегка различающиеся варианты белков.