Основы молекулярной биологии. Часть 2: Молекулярные генетические механизмы - А.Н. Огурцов 2011
Вирусы
Литический путь роста вирусов
Несмотря на колоссальное разнообразие в деталях развития конкретных вирусов, жизненный цикл тех из них, которые демонстрируют литический путь развития, проходит через следующие этапы.
7.3.1. Этапы литического цикла.
1. Адсорбция - Вирион присоединяется белками своего капсида к специфическим рецепторам на поверхности инфицируемой клетки.
2. Введение генома - Виральный геном пересекает плазматическую мембрану. У вирусов растений и животных виральные белки также вводятся в инфицируемую клетку.
3. Репликация - Синтезируются вирусные мРНК, используя генетический аппарат клетки - либо транскрипционные механизмы в случае ДНК-вирусов, либо, в случае РНК-вирусов, ферментативный аппарат с участием ферментов вируса. В обеих случаях вирусные мРНК транслируются трансляционным аппаратом клетки. Размножение вирусного генома управляется либо исключительно вирусными белками, либо с участием белков инфицированной клетки.
4. Ассемблирование (сборка) - Вирусные белки и реплицированные геномы вируса ассоциируются, формируя дочерние вирионы.
5. Высвобождение — Инфицируемая клетка либо резко разрушается (лизис), высвобождая все синтезированные вирионы сразу, либо разрушается постепенно, так же постепенно высвобождая вирионы.
7.3.2. ДНК-вирусы прокариот. На рисунке 69 показан литический цикл бактериофага Т4, безоболочечного (nonenveloped) ДНК-вируса, который инфицирует Е. coli.
После того, как белки на конце "хвоста" Т4 связываются со специфическими рецепторами на поверхности клетки, вирусный геном вводится внутрь клетки (рисунок 69, этап 1).
Ферменты клетки транскрибируют вирусные "первичные" гены, синтезируя мРНК, с которой затем транслируются "первичные" вирусные белки (рисунок 69, этап 2).
Первичные белки реплицируют вирусную ДНК и индуцируют экспрессию "вторичных" вирусных белков, используя ферментативный аппарат клетки (рисунок 69, этап 3).
Вторичные вирусные белки - это белки, из которых затем собирается капсид, и ферменты, которые стимулируют "разборку" клеточной ДНК на нуклеотиды, обеспечивая тем самым необходимый запас "строительных материалов" для синтеза вирусных ДНК.
Дочерние вирионы ассемблируются в клетке (рисунок 69, этап 4) и высвобождаются, после того когда вирусные белки разрушат клетку (лизис), (рисунок 69, этап 5). Вирусы, освобожденные после лизиса клетки, инициируют новый цикл инфицирования в других клетках организма.

Рисунок 69 - Литический жизненный цикл бактериофага Т4 Е. coli
Капсидные белки вируса, как правило, синтезируются в больших количествах, поскольку для ассемблирования дочерних вирионов требуется много их копий. В каждой инфицированной клетке синтезируется и ассемблируется около 100-200 дочерних вирионов Т4, которые высвобождаются после лизиса клетки.
7.3.3. ДНК-вирусы эукариот. Литический цикл несколько сложнее у ДНК-вирусов, которые инфицируют эукариотические клетки. У большинства таких вирусов вирусный ДНК-геном транспортируется (вместе с некоторыми ассоциированными белками) внутрь ядра клетки.
Там вирусная ДНК транскрибируется в РНК, используя транскрипционный аппарат клетки. Процессинг вирусной про-РНК ферментами клетки образует вирусную мРНК, которая транспортируется в цитоплазму и транслируется в вирусные белки рибосомами, тРНК и факторами трансляции инфицированной клетки.
Вирусные белки затем транспортируются назад в ядро клетки, где некоторые из них либо реплицируют вирусную ДНК непосредственно, либо активируют белки клеточного ядра для репликации вирусной ДНК, как это происходит в случае вируса SV40.
Ассемблирование белков капсида с синтезированной вирусной ДНК происходит в ядре клетки, при этом формируются сотни и даже тысячи дочерних вирионов.
7.3.4. РНК-вирусы животных и растений. С другой стороны, большинство РНК-вирусов животных и растений не нуждаются в использовании генетического аппарата ядер клетки для литического размножения.
В некоторых из этих вирусов вирусные ферменты, которые попадают внутрь клетки при внедрении вирусной РНК, транскрибируют вирусную РНК в мРНК в цитоплазме клетки.
Эта мРНК транслируется в вирусные белки трансляционным аппаратом клетки. Один или несколько таких белков затем синтезируют копии вирусной РНК.
Наконец, дочерние РНК-геномы ассемблируются с синтезированными белками капсида в дочерние вирионы в цитоплазме.
После того, как завершен синтез сотен и тысяч новых вирионов, большинство инфицированных бактериальных клеток и некоторые из инфицированных клеток растений и животных разрушаются (лизис), высвобождая все вирионы одновременно.
Однако при многих вирусных инфекциях растений и животных не происходит такого дискретного литического "события", напротив, погибшая инфицированная клетка постепенно высвобождает вирионы по мере своей постепенной дезинтеграции.
7.3.5. Оболочечные вирусы. Многие вирусы животных имеют липопротеидную оболочку, которая происходит из плазматической мембраны инфицированной клетки, и которая содержит большое количество вирусных гликопротеинов.
Процессы адсорбции и высвобождения оболочечных вирусов (enveloped viruses) существенно отличаются от аналогичных процессов безоболочечных вирусов (nonenveloped viruses).
В качестве примера литической репликации оболочечного вируса рассмотрим вирус бешенства (rabies virus) (рисунок 70).
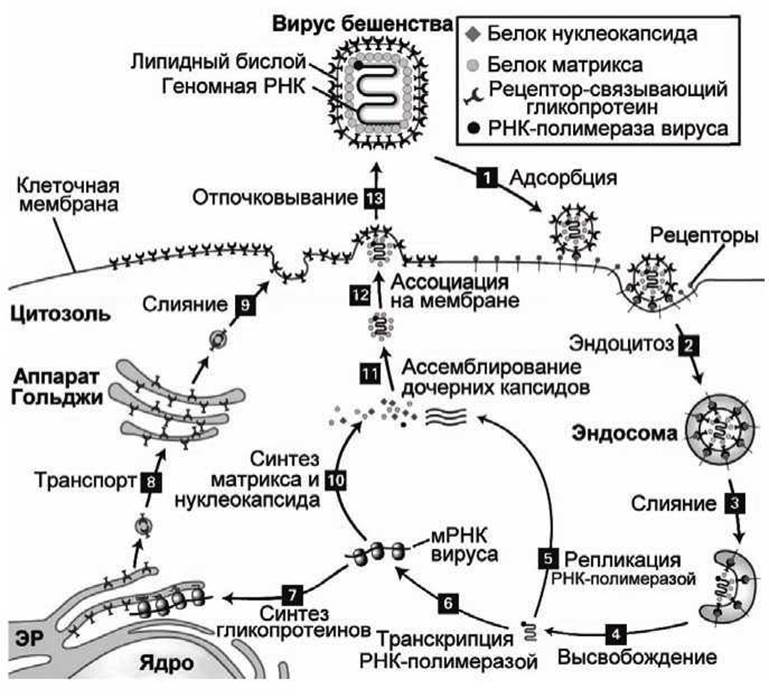
Рисунок 70 - Литический жизненный цикл вируса бешенства
Нуклеокапсид вируса бешенства состоит из однонитиевого РНК-генома, окруженного белковым капсидом. Как и другие литические РНК- вирусы, вирион бешенства реплицируется в цитоплазме и не требует использования ферментативного аппарата ядра инфицированной клетки. Вирус бешенства адсорбируется с помощью эндоцитоза, а высвобождение дочерних вирионов происходит посредством отпочковывания от плазматической мембраны инфицированной клетки.
Структурные компоненты вируса перечислены в верхней части рисунка. Заметим, что нуклеокапсид имеет спиральную, а не икосаэдрическую форму.
После адсорбции вириона к множественным копиям специфических мембранных белков инфицируемой клетки (рисунок 70, этап 1), происходит эндоцитозное поглощение вириона клеткой и формируется эндосома (рисунок 70, этап 2).
Клеточные белки (протонные насосы) в мембране эндосомы закачивают из цитозоля внутрь эндосомы протоны. Снижение эндосомальной pH приводит к конформационному изменению вирусных гликопротеинов, что приводит, в свою очередь, к слиянию вирусной липопротеидной оболочки с липидным бислоем мембраны эндосомы и высвобождением нуклеокапсида в цитозоль (рисунок 70, этапы 3 и 4).
РНК-полимераза вируса использует рибонуклеозидтрифосфаты (рНТФ) цитозоля для репликации РНК-генома вируса (рисунок 70, этап 5) и для синтеза вирусных мРНК (рисунок 70, этап 6).
С одной из вирусных мРНК с помощью рибосом эндоплазматического ретикулума (ЭР) транслируются трансмембранные гликопротеины, которые остаются внедренными в мембраны ЭР (рисунок 70, этап 7). К ним присоединяются необходимые углеводы в процессе дозревания в ЭР и аппарате Гольджи (рисунок 70, этап 8).
Везикулы с "созревшими" гликопротеинами сливаются с плазматической мембраной инфицированной клетки, тем самым, помещая рецептор-связывающие домены гликопротеинов снаружи клетки (рисунок 70, этап 9).
Одновременно другие вирусные мРНК транслируются на рибосомах клетки в белки нуклеокапсида, белки матрикса и вирусные РНК-полимеразы (рисунок 70, этап 10).
Все эти белки ассемблируются с реплицированной на этапе 5 вирусной геномной РНК и образуют дочерний нуклеокапсид (рисунок 70, этап 11), который затем присоединяется к цитозольным доменам вирусных трансмембранных гликопротеинов, которые уже внедрены в плазматическую мембрану инфицированной клетки (рисунок 70, этап 12).
Плазматическая мембрана оборачивается вокруг нуклеокапсида, формируя "почку", которая отпочковывается, высвобождая наружу клетки дочерний вирус.
Отпочковывание вирионов четко видно на электронных микрофотографиях инфицированных клеток, как показано на рисунке 71.
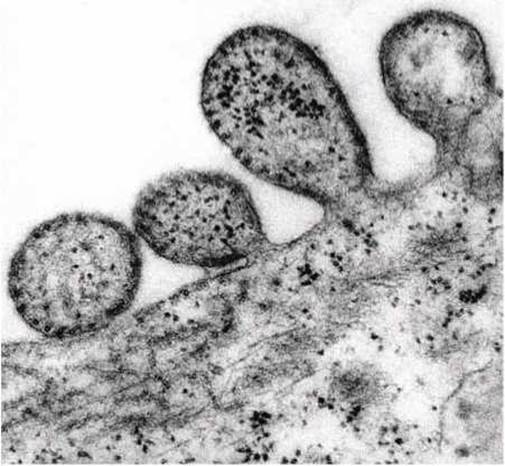
Рисунок 71 - Дочерние вирионы вирусов высвобождаются, отпочковываясь от плазматической мембраны инфицированной клетки
Десятки тысяч дочерних вирионов отпочковываются от инфицированной клетки прежде, чем она погибнет.