Общая микробиология - Шлегель Г. 1987
Неполные окисления
Образование вторичных метаболитов
С открытием пенициллина и других антибиотиков возникла новая обширная область промышленной микробиологии. Бактерии и грибы синтезируют множество веществ, которые по аналогии с подобного рода веществами растительного происхождения принято называть вторичными метаболитами. Многие из этих веществ играют важную роль как лечебные средства, стимулирующие препараты, добавки к кормам и т. п. В качестве продуцентов вторичных метаболитов микроорганизмы приобрели огромное экономическое значение. Открытие и исследование антибиотиков, а также получение новых полусинтетических антибиотиков оказало неоценимые услуги медицине. Мы еще не в состоянии предвидеть все возможности, которые откроются перед нами в будущем в связи с новыми исследованиями в этой области, и с новыми применениями вторичных метаболитов, синтезируемых микроорганизмами. Получение и отбор мутантов (с учетом регуляторных механизмов) позволят значительно расширить использование микробных синтезов.
10.4.1 Образование антибиотинов
Уже в прошлом веке было известно, что между различными микроорганизмами могут существовать как симбиотические, так и антагонистические взаимоотношения. Толчком к выяснению материальной основы антибиоза послужило наблюдение Флеминга, обнаружившего (1928), что колония гриба Penicillium notatum подавляла рост стафилококков. Выделяемое этим грибом вещество, которое диффундировало в агар, получило название пенициллина. С тех пор было выделено множество веществ с антибиотической активностью. Антибиотики - это вещества биологического происхождения, способные даже в низких концентрациях подавлять рост микроорганизмов. Различают вещества, подавляющие рост микробов (бактериостатические, фунгистатические) и убивающие их (бактерицидные, фунгицидные и т. д.).
Продуценты антибиотиков. К синтезу антибиотиков способны главным образом грибы из группы Aspergillales, актиномицеты и некоторые другие бактерии. На первом месте по химическому многообразию синтезируемых веществ стоят стрептомицеты. К настоящему времени подробно охарактеризовано более 2000 антибиотиков, однако в качестве химиотерапевтических средств применяется всего лишь около полусотни. Число описанных случаев антибиотических взаимодействий гораздо больше, но многие группы микроорганизмов, в том числе не поддающиеся культивированию или с трудом культивируемые бактерии и низшие грибы, в этом смысле еще недостаточно изучены.
Значение антибиотиков для образующих их организмов. Вопрос о значении антибиотиков для их продуцентов в условиях их естественного обитания - в почве - остается неясным. К образованию антибиотиков ведут специальные биохимические пути, относящиеся к вторичному метаболизму. Эти пути и обеспечивающие их ферменты не являются необходимыми для роста и выживания клеток. Генетический аппарат, который нужен для синтеза антибиотиков, для организма в случае их бесполезности был бы балластом, и организм освободился бы от него в процессе эволюции путем соответствующих делений. Поскольку в природе, очевидно, сохраняется лишь то, что целесообразно, нужно видеть в антибиотиках вещества, обеспечивающие их продуцентам селективное преимущество и в естественных условиях, т. е. в почве (например, преимущество в конкуренции за один и тот же субстрат). Однако такие антагонистические взаимоотношения в почве трудно обнаружить, поскольку антибиотики образуются в очень малых количествах; к тому же они обычно подавляют и рост самих продуцентов.
Постепенно утверждается представление, согласно которому в процессе эволюции может сохраняться и ненужный на первый взгляд генетический материал - даже в том случае, если в изученных до сих пор экспериментальных условиях он оказывается для организма балластом. Очевидно, природа более консервативна, чем это предполагалось на заре эры молекулярной биологии. В настоящее время антибиотики, а также другие вторичные метаболиты, прямую пользу которых для синтезирующих их клеток усмотреть трудно, причисляют, образно выражаясь, к «стружкам» обмена веществ или же к продуктам, возникшим на «игровой площадке» метаболизма. Этот пример ясно показывает, что изучение вторичного метаболизма бактерий, грибов и растений - одно из перспективных направлений в исследовании путей органической эволюции.
Методы выявления антибиотиков. Первые антибиотики были обнаружены случайно, по образованию зон подавления роста. В чашках с питательным агаром, густо засеянным тест-организмом (индикаторными бактериями), вокруг колоний гриба или стрептомицета рост отсутствовал: антибиотик, диффундирующий из колонии в агар, вызывал образование прозрачных участков в сплошном бактериальном газоне (рис. 10.4). Видами-индикаторами (тест-объектами) в таких опытах служат типичные представители различных групп микроорганизмов. Для качественного испытания продуцента антибиотика достаточно посеять его в середину чашки с питательным агаром, а индикаторные бактерии - в виде радиальных штрихов (штрих-тест, рис. 10.5). После инкубации по степени торможения роста различных индикаторных организмов судят о спектре действия антибиотика. Антибиотики различаются по действию на грам-положительные и грам-отрицательные бактерии, на дрожжи, дерматофиты и другие микроорганизмы.
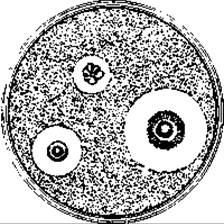
Рис. 10.4. Выделение антибиотиков бактериями или грибами можно обнаружить по образованию зон подавления роста индикаторных бактерий (Staphylococcus aureus), равномерно рассеянных на агаре.
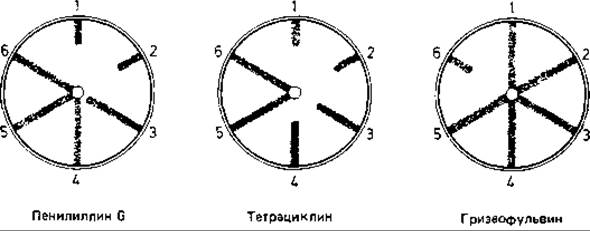
Рис. 10.5. Определение спектра действия трех антибиотиков с помощью штрихового теста. 1 - Staphylococcus aureus; 2 -Streptococcus; 3 - Escherichia coli; 4 - Pseudomonas aeruginosa; 5 - Candida albicans; 6 - Trichophyton rubrum.
В центр чашки Петри на агар с пептоном и гидролизатом казеина помещают диск из фильтровальной бумаги, пропитанный раствором испытуемого антибиотика (количество антибиотика ~ 10 мкг). Суспензии тест-организмов наносят платиновой петлей в виде радиальных штрихов (от одного до шести). В зоне диффузии антибиотика некоторые микроорганизмы не растут. (Wallhäusser К. Н.. Schmidt Н., Sterilisation, Desinfektion, Konservierung, Chemotherapie. Stuttgart: Thieme, 1967.)
Большинство антибиотиков было открыто в процессе предварительного отбора (скрининга). На рис. 10.6 представлена вся последовательность работы - от получения суспензии почвенной пробы до опыта на животных.
Количественное определение. Для количественной оценки действия антибиотика пользуются методом диффузии в агар (рис. 10.7), методом последовательных разведений и некоторыми другими методами. Для проведения теста с диффузией чашки заполняют до определенной высоты агаризованной средой, содержащей суспензию тест-организма. Затем в чашки вносят испытуемые растворы антибиотика. Их помещают в лунки, либо в стеклянный или металлический цилиндр, или же накладывают на агар пропитанные антибиотиком диски из фильтровальной бумаги. При положительной реакции во всех случаях после инкубации становится заметной зона подавления роста тест-организма. Диаметр этой зоны при соблюдении постоянных условий опыта (состав питательной среды, толщина слоя агара, плотность посева, время инкубации, температура и т.д.) пропорционален логарифму концентрации антибиотика (рис. 10.7).
При использовании метода последовательных разведений готовят серию разведений антибиотика в отношении 1 : 2 в питательном растворе, засеянном тест-организмом, и после инкубации определяют ту минимальную концентрацию антибиотика, при которой не наблюдается роста (минимальную бактериостатическую концентрацию).
Для установления синергического и антагонистического действия разных веществ, а также для исследования действия антибиотиков на другие организмы (на простейших, червей, водоросли, культуры клеток, вирусы) были разработаны специальные методы.
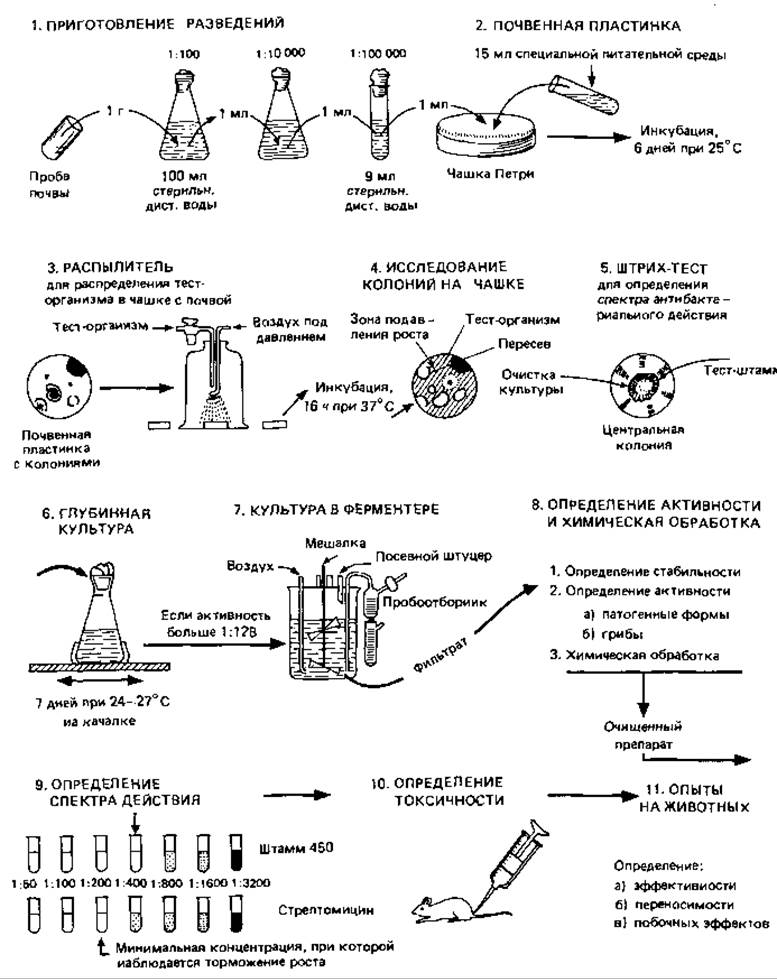
Рис. 10.6. План работы по отбору антибиотиков. (Wallhäusser К. Н., Schmidt Н., Sterilisation, Desinfektion, Konservierung, Chemotherapie. Stuttgart: Thieme, 1976.)
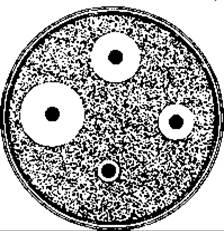
Рис. 10.7. Количественное определение антибиотика методом диффузии в чашке. Диски из фильтровальной бумаги, помещенные на поверхность засеянной агаризованной среды, содержат различные количества антибиотика. Диаметр зоны подавления роста тест-организма пропорционален концентрации антибиотика. (Zähner Н., Biologie der Antibiotica. Berlin: Springer, 1965.)
Важнейшие антибиотики, применяемые в медицине. Первое место среди них все еще принадлежит пенициллину, который синтезируют Penicillium notatum, Р. chrysogenum и некоторые другие грибы; удалось также получить полусинтетические пенициллины (путем расщепления природных пенициллинов до 6-аминопенициллановой кислоты, к которой затем химическим путем присоединяют различные боковые группы). О механизме действия пенициллина на бактерии уже говорилось ранее (разд. 2.2.3). Для человека пенициллин почти не токсичен и лишь в редких случаях вызывает побочные аллергические реакции. Многие бактерии образуют пенициллиназу, которая расщепляет ß-лактамовое кольцо и инактивирует пенициллин. Воздействуя на 6-аминопенициллановую кислоту хлорангидридами кислот, можно получать сотни пенициллинов (рис. 10.8). Многие полусинтетические пенициллины не расщепляются пенициллиназой и ввиду их устойчивости к действию кислот могут вводиться перорально.
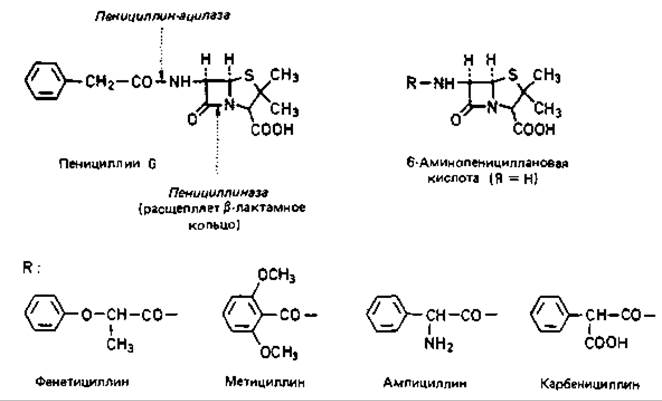
Рис. 10.8. Действие бактериальных ферментов - пенициллиназы и пенициллинацилазы - на пенициллин G. Замещая R в 6-аминопенициллановой кислоте различными радикалами, можно получить такие полусинтетические пенициллины, как фенетициллин, метициллин, ампициллин и карбенициллин.
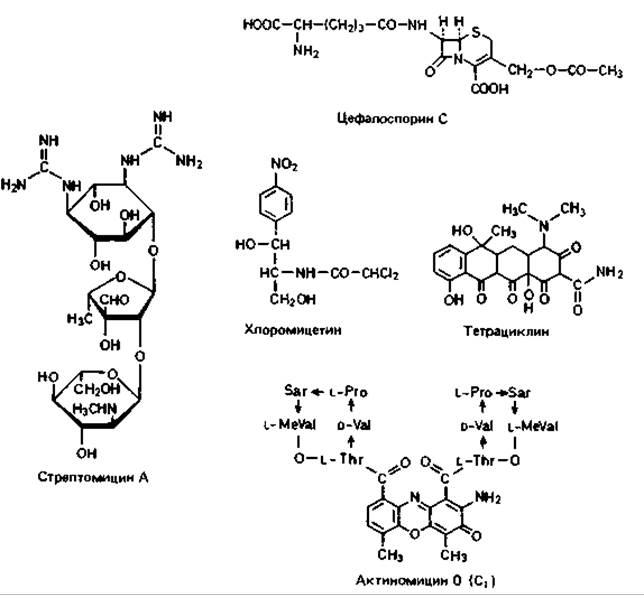
Рис. 10.9. Структурные формулы цефалоспорина С, стрептомицина А, хлоромицетина (хлорамфеникола), тетрациклина и актиномицина D (актиномицина С1).
Цефалоспорины - продукты одного из видов гриба Cephalosporium. Цефалоспорин С имеет ß-лактамовое кольцо и по своей структуре близок к пенициллину (рис. 10.9). Отщепляя боковую цепь и затем присоединяя к образовавшейся 7-аминоцефалоспорановой кислоте другие боковые группы, можно получать полусинтегические цефалоспорины (цефалотин, цефалоридин), которые по своему действию сходны с производными пенициллина.
Стрептомицин был впервые выделен из культуры Streptomyces griseus, однако его синтезируют и некоторые другие виды Streptomyces. Молекула стрептомицина состоит из трех частей: N-Memn-L-2-глюкозамина, метилпентозы и дигуанидинзамещенного инозитола (рис. 10.9). Успех применения стрептомицина объясняется его действием на ряд кислотоустойчивых и грам-отрицательных бактерий, нечувствительных к пенициллину. Однако стрептомицин вызывает у больных резко выраженные аллергические реакции. Этот антибиотик применяется также в ветеринарии и для борьбы с болезнями растений.
Хлоромицетин (хлорамфеникол) был впервые обнаружен в культурах Streptomyces venezuelae, но его можно получить и синтетическим путем (рис. 10.9). Он отличается исключительной стабильностью и действует на многие грам-отрицательные бактерии, включая спирохеты, риккетсии и актиномицеты, а также на крупные вирусы.
Тетрациклины тоже представляют собой метаболиты различных стрептомицетов (в том числе Streptomyces aureofaciens). Химически они очень близки между собой и имеют в основе структуры нафтацен (рис. 10.9). Наиболее известны хлортетрациклин (ауреомицин), окситетрациклин (террамицин) и тетрациклин. Тетрациклины отличаются широким спектром действия и хорошей переносимостью.
К макролидам относятся антибиотики разного происхождения с относительно большой молекулярной массой, для которых характерно макроциклическое лактоновое кольцо (эритромицин, карбомицин А, пикромицин и др.).
Актиномицин был выделен в 1940 г. (первым среди антибиотиков, образуемых стрептомицетами). Это смесь нескольких веществ; объединяет их только феноксазоновый хромофор. Роль заместителей играют различные полипептидные цепочки (рис. 10.9). Наконец, следует упомянуть еще группу полипептидных антибиотиков (грамицидин S, полимиксины, бацитрацин, ристоцетин и др.). В молекуле полимиксина В к кольцу из семи аминокислот присоединена с помощью пептидной связи боковая цепь (рис. 10.10). Полипептидные антибиотики обладают высоким сродством к плазматической мембране, поэтому они одинаково токсичны как для бактерий, так и для эукариот и не применяются в клинике. Благодаря своей способности избирательно транспортировать ионы через мембрану полипептидные антибиотики могут применяться в исследовательских целях в качестве ионофоров (см. разд. 7.7). Валиномицин, например, облегчает транспорт ионов калия через мембрану. В состав молекулы этого антибиотика входит кольцо из 12 звеньев (среди них валин, 2-гидроксиизовалерат и лактат). Структура этого кольца такова, что ион калия как раз помещается во внутреннем пространстве молекулы. Комплекс валиномицина с К+ благодаря присутствию валина и валерата липофилен и легко транспортируется через липидный слой мембраны. Поэтому добавление валиномицина к клеточной суспензии ведет к потере клетками ионов калия.
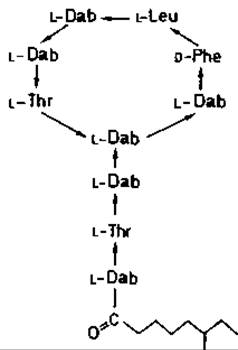
Рис. 10.10. Полимиксин В. L-Dab - 2,4-диаминомасляная кислота; L-leu-L- лейцин; D-Phe - фенилаланин; L-Thr - треонин; алифатическая боковая цепь - 6-метилоктановая кислота.
В фармацевтической промышленности для производства антибиотиков используются сейчас не исходные штаммы микроорганизмов, а более продуктивные мутанты. Штамм гриба, открытый Флемингом, синтезировал лишь около 3 мкг пенициллина на 1 мл среды. Современные штаммы-продуценты дают минимум в 2000 раз больше. Такое повышение выхода антибиотиков - результат мутаций и отбора более активных штаммов, улучшения состава питательных сред и оптимизации условий производства. Пути биосинтеза многих антибиотиков уже выяснены, и задача состоит сейчас в том, чтобы еще больше повысить продуктивность микроорганизмов путем получения и более целенаправленного отбора мутантов.
10.4.2 Минотоксины
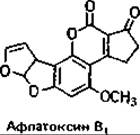
Микотоксинами называют вторичные метаболиты определенных видов грибов. В широком понимании к ним можно отнести также и образуемые грибами антибиотики. В узком смысле, однако, под микотоксинами понимают только такие продукты жизнедеятельности грибов, которые токсичны для высших животных и человека. Продуцентом микотоксина является, например, уже упоминавшийся возбудитель спорыньи Claviceps purpurea. Недавно микотоксины вновь привлекли к себе пристальное внимание, после того как был описан случай гибели тысяч индюшат от корма, содержавшего афлатоксины. Афлатоксины (производные кумарина) синтезируются отдельными штаммами Aspergillus flavus, A. parasiticus, A. oryzae и некоторыми другими видами грибов. Они могут присутствовать в разных заплесневелых продуктах (в арахисе, зерне, плодах масличных растений, в корме животных). Афлатоксины обладают канцерогенными свойствами.
К микотоксинам причисляют также токсины ядовитых видов базидиомицетов - Amanita phalloides (аманитатоксин), A. pantherina, А. muscaria, lnocybe patouillardii (грибной атропин и мускарин).
10.4.3 Другие вторичные метаболиты
Среди витаминов, образуемых микроорганизмами, заслуживают упоминания рибофлавин и витамин В12. Рибофлавин выделяют главным образом аскомицеты (Ashbya gossypii и Eremothecium ashbyii); однако дрожжи (Candida) и бактерии (Clostridium) тоже синтезируют в больших количествах флавины. Способность к образованию витамина В12 присуща бактериям, в метаболизме которых важную роль играют корриноиды (Propionibacterium, Clostridium). Этот же витамин образуют и стрептомицеты. Из мицелия зигомицетов (Blakesleea trispora и Choanephora circinans) получают каротиноиды, используемые как добавки к кормам для животных.
Что касается алкалоидов, то одни только алкалоиды спорыньи добывают из микроорганизма. Хотя в настоящее время склероции спорыньи (Secale cornutum) получают главным образом путем искусственного заражения ржи возбудителем спорыньи (Claviceps purpurea), глубинная культура определенных штаммов Claviceps paspali тоже начинает вызывать интерес с экономический точки зрения. Алкалоиды спорыньи, производные лизергиновой кислоты (эрготамин, эрготоксин), применяются при лечении сосудистых заболеваний и мигрени, а также известны как галлюциногены.
Принципы выращивания бактерий, дрожжей и других грибов все шире используются и при культивировании животных и растительных клеток. Разработаны методы выращивания растительных клеток на синтетических средах в ферментерах емкостью в тысячи литров. В таких условиях растительные клетки образуют ферменты и вторичные метаболиты в концентрациях, которые могут быть на 1-2 порядка выше, чем в интактных клетках. Неожиданным оказалось то, что в подобных культурах могут накапливаться и такие вещества, которые растение синтезирует лишь в малых количествах или же не синтезирует вовсе. Вероятно, со временем можно будет получать алкалоиды, гликозиды, стероиды, органические кислоты и другие вторичные метаболиты с помощью растительных клеток.
10.4.4 Другие продукты микробного происхождения
С помощью микроорганизмов можно получать разнообразные полисахариды, ферменты, антигены и яды. Продукты микробного происхождения дополняют вещества, получаемые классическим способом, а частично и заменяют их.
Для повышения вязкости жидкостей уже с давних времен применяются растительные слизи. В настоящее время их все больше вытесняют многочисленные бактериальные экзополисахариды (разд. 2.2.4) (табл. 10.1). В качестве добавок к мороженому, пудингам и кремам используют алгинаты. Они же нашли применение и как гидрофильные покрытия для поддержания корней растений во влажном состоянии. Полисахариды, добываемые из морских водорослей, постепенно вытесняются сходными продуктами, получаемыми с помощью Azotobacter или Pseudomonas. Разностороннее применение нашли слизи, образуемые фитопатогенной бактерией Xanthomonas campestris - ксантаны. Их структурную основу составляют цепи из молекул глюкозы, образованные (как и в целлюлозе) с помощью ß-1,4-гликозидных связей и несущие боковые цепочки из трисахаридов. Ксантаны применяются как наполнители в пищевой и косметической промышленности, как эмульгаторы для типографских красок и даже в качестве добавок к промывным водам в месторождениях нефти. Для приготовления пудингов и низкокалорийных супов используют курдланы, которые не подвергаются расщеплению в кишечнике человека. В главе 2.2.4 уже говорилось о применении декстрана как заменителя плазмы крови, а также как основы для адсорбентов, известных под коммерческим названием «сефадекс».
Таблица 10.1. Экзополисахариды, синтезируемые микроорганизмами, и их применение
|
Продукт |
Микроорганизмы-продуценты |
Применение |
|
Декстран (а-1,6-глюкан) |
Leuconostoc mesenteroides, Klebsiella, Acetobacter, стрептококки |
Заменители плазмы крови; адсорбенты в биохимической промышленности |
|
Алгинат (соединенные с помощью 1,4-гликозидных связей маннуроновые и гулуроновые кислоты) |
Azotobacter vinelandii, Pseudomonas aeruginosa |
Добавки к мороженому; быстрорастворимая смесь для приготовления пудингов, кремов; средства для пропитки тканей и бумаги; гидрофильная пленка для корней растений, новогодних елок; пленки для покрытия ран |
|
Ксантан (целлюлоза с трисахаридными боковыми цепями) |
Xanthomonas campestris |
Добавки к напиткам и плавленым сырам; быстрорастворимая смесь для приготовления пудингов, кремов; стабилизатор эмульсий; «французская приправа»1 |
|
Пуллулан (остатки мальтотриозы, соединенные с помощью ß-1,6-гликозидных связей) |
Aureobasidium (синонимы: Pullularia, Dematium) pullulans |
Покрытия для пищевых продуктов |
|
Курдлан (ß-1,3-глюкан) |
Alcaligenes faecalis var. myxogenes |
Желирующее средство для пудингов (низкокалорийно, так как не подвергается расщеплению в кишечнике) |
1 Смесь прованского масла с уксусом и горчицей - Прим. перев.
На смену ферментным препаратам, получаемым из животных и растений, тоже постепенно приходят микробные ферменты (табл. 10.2). Наряду с пепсином, трипсином и папаином применяют протеазы, выделяемые аэробными спорообразующими бактериями и грибами. Вместо применявшегося ранее для створаживания молока сычужного фермента, который получали из желудков телят, в настоящее время используют фермент реннин, выделяемый грибом Mucor rouxii и некоторыми другими грибами.
Таблица 10.2. Ферменты, синтезируемые микроорганизмами, и их применение
|
Ферменты (и катализируемые ими реакции) |
Микроорганизмы-продуценты |
Применение |
|
Инвертаза (гидролиз сахарозы) |
Aspergillus oryzae, дрожжи и другие грибы |
Приготовление инвертированного сахара для кондитерских изделий |
|
Протеазы (гидролиз белков) |
Bacillus subtilis и другие бактерии, а также грибы |
Добавки к моющим средствам; дубление |
|
Пектинолитические ферменты (гидролиз пектина) |
Грибы и Erwinia |
Осветление фруктовых соков |
|
Липазы (гидролиз липидов) |
Грибы и Pseudomonas |
Дубление; добавки к моющим средствам |
|
Глюкозооксидаза (окисление глюкозы до глюконата) |
Aspergillus niger, Gluconobacter oxidans |
Получение глюконовой кислоты |
|
Гексозоизомераза (изомеризация фруктозы) |
Streptomyces |
Получение фруктозы из глюкозы |
|
Амилаза (гидролиз крахмала) |
Bacillus subtilis, Aspergillus spec., другие грибы |
Приготовление сиропа из глюкозы; удаление аппретирующего крахма |
|
Целлюлазы (гидролиз целлюлозы) |
Trichoderma viride, Penicillium |
Получение глюкозы из целлюлозы |
Для превращения крахмала в сахар с целью получения спирта уже давно не пользуются проросшим зерном; вместо этого к крахмалу добавляют амилазы грибов. Инвертированный сахар, используемый в кондитерских изделиях, получают из сахарозы с помощью инвертазы из Aspergillus oryzae и других грибов. Фруктозу, необходимую для производства искусственного меда и сиропов, получают путем превращения глюкозы при участии гексозоизомеразы, источником которой служат некоторые виды Streptomyces или Lactobacillus brevis. Идут поиски путей использования дешевой целлюлозы, получаемой из древесины и соломы, для производства этанола с помощью микробных целлюлаз (источники - Trichoderma viride, Penicillium). В последнее время интенсивно разрабатываются также методы получения многих других ферментов; для повышения их стабильности, а также удобства обращения с ними ферменты применяют в иммобилизованной форме, т. е. фиксируют на материале-носителе (целлюлозе, агарозе, стеклянных шариках и др.).
Для более углубленного изучения представленных здесь проблем можно рекомендовать учебные пособия по промышленной микробиологии или биотехнологии. Генная инженерия (техника молекулярного клонирования, разд. 15.3.6) открыла и в этой области новые возможности для биотехнологии.