ИММУНОЛОГИЯ - Ройт А. - Мир 2000
Глава 12. Развитие иммунной системы в онтогенезе
■ Большинство клеток иммунной системы образуется из гемопоэтических стволовых клеток.
■ Развитие клеток разных типов (рядов, или линий, дифференцировки) зависит от межклеточных взаимодействий и цитокинов.
■ Лимфоидные стволовые клетки развиваются и созревают в первичных лимфоидных органах. Этот процесс называется лимфопоэзом.
■ Т-лимфоциты при развитии в тимусе подвергаются положительной и отрицательной селекции.
■ В-клетки млекопитающих развиваются главным образом в печени плода, а после рождения - в костном мозге. Этот процесс продолжается в течение всей жизни организма. В-клетки в местах своего развития также подвергаются отбору.
■ Репертуар антител, существующий у взрослых особей, формируется в процессе лимфопоэза путем рекомбинации генных сегментов, кодирующих ТкР и Ig.
■ В центрах размножения происходит олигоклональная пролиферация В-клеток, переключение изотипа антител, повышение аффинности и формирование иммунологической памяти.
Эффективное функционирование иммунной системы зависит от взаимодействия многочисленных клеточных и гуморальных компонентов, которые в пре- и постнатальный периоды созревают с различной скоростью. Многие клетки, участвующие в иммунном ответе, происходят от недифференцированных гемопоэтических стволовых клеток (ГСК). Под влиянием факторов микроокружения — взаимодействия с соседними клетками и присутствия растворимых или мембраносвязанных цитокинов - дифференцировка ГСК происходит в разных направлениях (рис. 12.1).
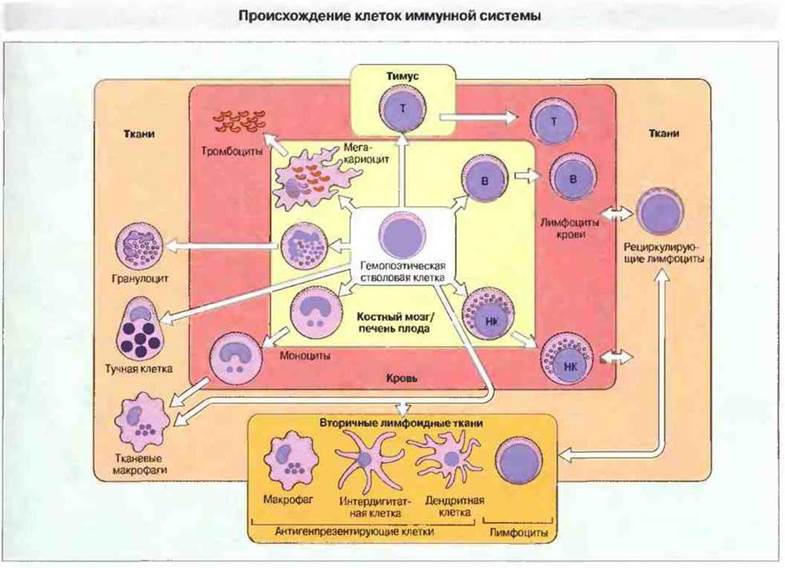
Рис. 12.1. Все изображенные на рисунке клетки происходят от гемопоэтической стволовой клетки. Тромбоциты, продуцируемые мегакариоцитами, поступают в кровоток. Гранулоциты и моноциты мигрируют из кровотока в ткани. Тучные клетки присутствуют во всех тканях. В-клетки у млекопитающих созревают в печени плода и костном мозге, а Т-клетки - в тимусе. Местом образования больших гранулярных лимфоцитов, обладающих активностью нормальных киллеров (НК), служит, вероятно, костный мозг. Лимфоциты мигрируют из кровотока, проходят через вторичные лимфоидные ткани и вновь поступают в кровоток. Роль антигенпрезентирующих клеток во вторичных лимфоидных тканях выполняют интердигитатные и дендритные клетки.
У млекопитающих в период внутриутробного развития ГСК присутствуют в желточном мешке, печени, селезенке и костном мозге. После рождения и в зрелом организме они обычно сохраняются лишь в костном мозге. Эти «самообновляющиеся» путем деления ГСК под влиянием разнообразных местных (в участках гемопоэза) факторов роста и дифференцировки дают начало большинству или даже всем клеткам иммунной системы.
Из ГСК образуются клетки четырех главных рядов (линий) дифференцировки:
✵ эритроидного (эритроциты),
✵ мегакариош(тарного (тромбоциты),
✵ миелоидного (гранулоииты и моноядерные фагоциты) и
✵ лимфоидного (лимфоциты). Антигенпрезентируюшие клетки в основном, но не исключительно, развиваются из миелоидных клеток-предшественников. Клетки миелоидного и лимфоидного рядов наиболее важны для функционирования иммунной системы.
МИЕЛОИДНЫЕ КЛЕТКИ
У человека миелопоэз начинается в печени, примерно на 6 неделе внутриутробного развития. Изучение роста колоний из индивидуальных стволовых клеток in vitro показало, что первая образующаяся из ГСК клетка-предшественник представляет собой колониеобразующую единицу (КОЕ), которая может дать начало образованию гранулоцитов, эритроцитов, моноцитов и мегакариоцитов (КОЕ-ГЭММ). Созревание этих клеток происходит под влиянием колониестимулируюших факторов (КСФ) и ряда интерлейкинов, в том числе ИЛ-1, ИЛ-3, ИЛ-4, ИЛ-5 и ИЛ-6 (рис. 12.2). Все они играют важную роль в положительной регуляции (стимуляции) гемопоэза и продуцируются главным образом стромальными клетками костного мозга, но также и зрелыми формами дифференцированных миелоидных и лимфоидных клеток. Другие цитокины (например, ТФРβ) могут осуществлять понижающую регуляцию (подавление) гемопоэза.
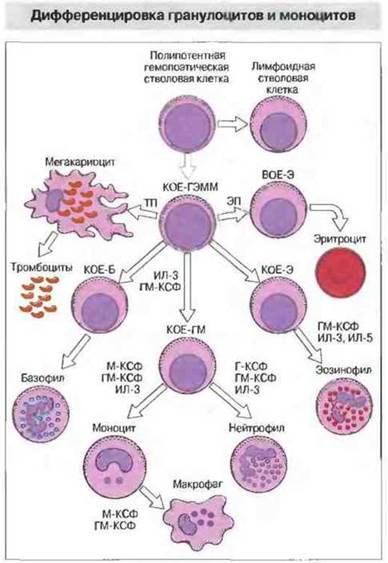
Рис. 12.2. Полипотентные гепомоэтические стволовые клетки превращаются в колониеобразующие единицы (КОЕ) КОЕ-ГЭММ может давать начало всем клеткам крови, за исключением лимфоцитов. Образование из стволовой клетки любого из пяти типов клеток [мегакариоцитов, эритроцитов - через этап предшественника, называемого взрывообразующей единицей эритроидного ряда (ВОЕ-Э), базофилов, нейтрофилов или эозимофилов] индуцирует ИЛ-3 и фактор, стимулирующий образование колоний гранулоцитов и макрофагов (ГМ-КСФ); эти же факторы необходимы для дальнейшей дифференцировки гранулоцитов и моноцитов. Образование эозинофилов (Э) и КОЕ-3 стимулируется ИЛ-5. Нейтрофилы и моноциты образуются из КОЕ-ГМ под действием соответственно Г-КСФ и М-КСФ. Оба эти фактора, как и другие цитокины (включая ИЛ-1, ИЛ-4 и ИЛ-6), стимулируют дифференцировку моноцитов в макрофаги. Образование мегакариоцитов стимулируется тромбопоэтином (ТП) (Б - базофил; ЭЛ - эритропоэтин; Г - гранулоцит; М - моноцит.)
Нейтрофилы и моноциты развиваются из общих клеток-предшественников
Образование нейтрофилов. Клеткой — предшественником нейтрофилов (вид гранулоцитов) и мононуклеарных фагоцитов (макрофагов) служит КОЕ-ГМ. При дифференцировке в нейтрофилы клетки проходят несколько морфологических стадий. Из миелобластов образуются промиелоциты и затем миелоциты, которые созревают и поступают в кровоток в виде нейтрофилов. Однонаправленная дифференцировка клеток КОЕ-ГМ в зрелые нейтрофилы обусловлена появлением у них на разных стадиях развития рецепторов для специфических факторов роста и дифференцировки.
По мере созревания гранулоцитов на их поверхности исчезают или появляются поверхностные дифференцировочные маркеры (рис. 12.3). Например, клетки КОЕ-ГМ экспрессируют молекулы МНС класса II и маркер CD38, отсутствующие на зрелых нейтрофилах. К другим молекулам поверхности, экспрессируемым в процессе дифференцировки, относятся CD13, CDI4
(представлен в небольшой концентрации), CD15 (Х-детерминанта группы крови Льюис), CD29 (β1-интегрин), VLA-4 (CD49d, α-цепь), лейкоцитарные интегрины CD11а, b, с и αD в ассоциации с β2-цепями CD18, рецепторы комплемента и Fcγ-рецепторы (CD 16) (см. рис. 2.42).
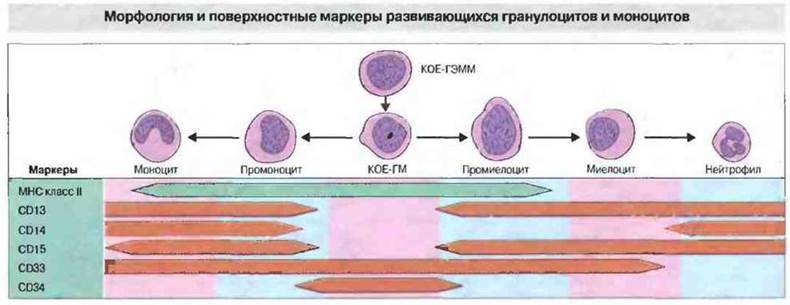
Рис. 12.3. Клетки моноцитарного и нейтрофильного линий дифференцировки образуются из общей клетки-предшественника, КОЕ-ГМ. Дифференцировка по каждому из этих путей сопровождается утратой маркера CD34. На моноцитах сохраняется CD33, тогда как на зрелых нейтрофилах эти молекулы, равно как и молекулы МНС класса It, отсутствуют. Маркер CD14 экспрессируется на моноцитах, но лишь в слабой степени на некоторых гранулоцитах, возможно при активации.
Функциональную активность гранулоцитов, находящихся на различных стадиях созревания, оценить трудно, но, по-видимому, полным функциональным потенциалом обладают только зрелые клетки. Ряд данных свидетельствует о том, что активность нейтрофилов, определяемая по фагоцитозу или хемотаксису, у плода ниже, чем в зрелом организме. Однако это может быть отчасти связано с меньшим содержанием опсонинов в сыворотке плода, а не с особенностями самих клеток. Для приобретения активности нейтрофилам необходимо непосредственное взаимодействие с микроорганизмами или с цитокинами, образующимися при иммунном ответе на антиген, (или с теми и другими вместе) в присутствии опсонинов. Это может лимитировать активность нейтрофилов на раннем этапе развития организма. Активация нейтрофилов цитокинами и хемокинами является также необходимым условием их миграции из крови в ткани.
Образование моноцитов. При дифференцировке по моноцитарному пути из КОЕ-ГМ вначале образуются пролиферирующие монобласты. Они дифференцируются в промоноциты и, наконец, в зрелые моноциты крови. Считается, что циркулирующие моноциты служат возобновляемым пулом для образования тканевых макрофагов, например макрофагов легких. Различные формы макрофагов составляют систему мононуклеарных фагоцитов (см. гл. 2).
Зрелые нейтрофилы и моноциты/макрофаги лишены CD34 и других маркеров ранних стадий дифференцировки. Однако моноциты, в отличие от нейтрофилов, продолжают экспрессировать большое количество молекул МНС класса II (рис. 12.3), необходимых для презентации антигена Т- клеткам. Моноциты синтезируют также многие из тех поверхностных молекул, которые характерны для зрелых нейтрофилов (см. рис. 2.28).
На стадиях дифференцировки определить функциональные возможности моноцитов, как и гранулоцитов, весьма трудно. Однако изучение in vitro некоторых миелоидных опухолей, клетки которых предположительно представляют собой моноциты на разных стадиях дифференцировки, свидетельствует о том, что как фагоцитарная активность, так и цитотоксичность, опосредуемая Fc-рецептором, достигают оптимального уровня только на стадии зрелых макрофагов. У новорожденного и взрослого человека моноциты вырабатывают цитокин ИЛ-1 с равной эффективностью, но у новорожденного эта функция слабее повышается под действием ИФγ, чем у взрослого.
Дендритные клетки развиваются из стволовых клеток костного мозга
Большинство классических антигенпрезентирующих клеток (АПК), включая макрофаги, клетки Лангерганса, интердигитатные и дендритные клетки, присутствует в организме уже при рождении. По всей вероятности, основная их масса образуется из стволовых клеток костного мозга. Возможно, они происходят из одной и той же клетки-предшественника CD34+(КОЕ-ГЭММ). Морфологические, цитохимические и функциональные особенности разных АПК должны тогда определяться последующим влиянием факторов микроокружения, например цитокинов. Другая возможность состоит в том, что АП К образуются из разных стволовых клеток и по разным направлениям дифференцировки. Важное исключение составляют фолликулярные дендритные клетки (ФДК), локализованные в центрах размножения внутри вторичных лимфоидных фолликулов и происходящие, возможно, от мезенхимных клеток. В первичных фолликулах периферических лимфоидных тканей ФДК присутствуют уже при рождении. В отличие от других АПК они лишены подвижности.
Уже на очень ранних стадиях развития организма АПК присутствуют в тимусе, причем их участие в МНС-рестрикции и селекции Т-клеток показывает, что по крайней мере некоторые из них к этому времени достигают полной зрелости. Однако активность АПК на ранних стадиях развития организма явно неоптимальна. У новорожденных крысят, например, образование антител к эритроцитам барана происходит только при одновременном введении АПК взрослых крыс (рис. 12.4).
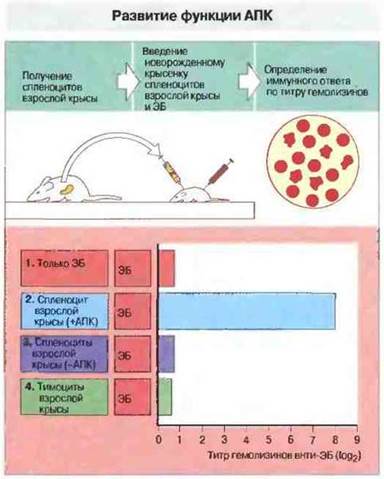
Рис. 12.4. Развитие функции антигенпрезентирующей клетки процессинга и презентации антигена. В этом опыте новорожденным крысятам вводили: 1) только эритроциты барана (ЭБ), 2) ЭБ + клетки селезенки (содержащей АПК) взрослых крыс, 3) ЭБ + клетки селезенки, лишенной АПК, или 4) ЭБ + зрелые тимоциты. Во всех случаях взрослые крысы принадлежали к той же линии, что и новорожденные. У крысят каждой группы регистрировали гуморальный иммунный ответ - появление антител. У новорожденных крысят, которым вводили только ЭБ, антитела к ЭБ антигенам не образовывались. Однако при одновременном введении спленоцитов взрослых крыс (вариант 2) иммунный ответ развивался. Ни зрелые спленоциты в отсутствие АПК, ни тимоциты сами по себе не вызывали продукции антител. Следовательно, АПК новорожденных особей неспособны эффективно осуществлять процессинг и презентацию ЭБ-антигенов.