Основы биохимии - А. А. Анисимов 1986
Углеводы
Регуляция постоянства содержания глюкозы в крови
Всосавшиеся из кишечника моносахариды (преимущественно глюкоза) через воротную вену доставляются прежде всего в печень, где часть глюкозы используется на образование запасных отложений гликогена. Содержание последнего в печени человека и животных зависит от режима питания; чем больше углеводов в рационе, тем больше гликогена в печени. Синтез и распад гликогена катализируются различными ферментами и контролируются независимо. Часть глюкозы используется самой печенью для получения энергии, необходимой для многочисленных реакций, протекающих в ней. Кроме того, определенное количество глюкозы в печени превращается в жиры. Так, при нормальном смешанном питании только 3—5% глюкозы превращается в гликоген (его среднее содержание в печени колеблется от 5 до 7%), 30% глюкозы идет на образование жиров и 60—70% окисляется до СO2 и Н2O. При обильном углеводном питании 10% глюкозы откладывается в печени в виде гликогена, 40% — превращается в жиры и 50% окисляется.
Сахар в крови, лимфе, спинно-мозговой жидкости представлен глюкозой, уровень которой очень тонко регулируется. Содержание глюкозы в артериальной и капиллярной крови здорового человека составляет 54—96 мг/100 мл при определении глюкозооксидазным методом и 80—120 мг/100 мл при определении по Хагедорну и Иенсену (вторым методом кроме глюкозы определяются одновременно некоторые другие редуцирующие вещества в крови). В венозной крови содержится меньше глюкозы, так как она потребляется тканями из крови. Единственный орган, выделяющий глюкозу в общую циркуляцию, — печень.
Сахара — компонент внутренней среды и у бесповозночных. Так, в гемолимфе насекомых они представлены в основном трегалозой. Из позвоночных наиболее постоянен уровень глюкозы натощак у человека и высших позвоночных. У птиц содержание глюкозы в крови выше, чем у млекопитающих. Для низших позвоночных характерны большие колебания сахара в крови в зависимости от внешней среды и биологического периода жизни. У холоднокровных животных (рыбы, амфибии, рептилии) глюкозы в крови меньше, чем у теплокровных, — 30—50 мг/100 мл. Существует зависимость между содержанием глюкозы в крови и степенью подвижности животных; например, у донных, малоподвижных рыб концентрация глюкозы в крови ниже, чем у подвижных рыб горных ручьев или быстротекущих рек. В крови жвачных глюкозы менее 50 мг/100 мл, так как у них из кишечника кроме глюкозы в кровь поступают продукты брожения клетчатки — органические кислоты.
После приема пищи, содержащей углеводы, уровень глюкозы в воротной вене печени человека может повыситься до 200—220 мг/100 мл. Однако при этом во всей остальной кровеносной системе содержание глюкозы у здорового человека или не будет изменяться (54—96 мг/100 мл), или несколько увеличится (пищевая гипергликемия), но в результате выведения избытка глюкозы с мочой через почки (пищевая глюкозурия) через 1,5—2 ч после принятия пищи придет в норму. Выведение глюкозы с мочой начинается при ее содержании в крови выше 120—150 мг/100 мл. Это может происходить при одновременном приеме 160—180 г сахарозы или 120— 150 г фруктозы (рис. 6.11).
Углеводное голодание определенной продолжительности или усиленное расходование глюкозы при активной физической нагрузке у здорового человека также не приводит к существенным отклонениям содержания глюкозы в крови от нормы. Таким образом, в организме непрерывно поддерживается постоянное количество глюкозы в крови, происходит гомеостатическая регуляция.
При гомеостазе изменение концентрации какого-либо вещества в организме само инициирует возникновение процессов, направленных на восстановление нормальной концентрации этого вещества, осуществляется ауторегуляция. В основе этих механизмов лежит взаимодействие прямых и обратных связей, поэтому в целом такого рода явления в живых организмах можно рассматривать в рамках и понятиях кибернетики — науки о законах связи, управления и контроля.
Простейшей формой регуляции уровня глюкозы в крови является осуществление гомеостатической, регуляторной функции печени. Этот физиологический механизм, филогенетически наиболее древний, недостаточен для обеспечения организма высокоразвитых животных и человека полноценным углеводным питанием. В процессе эволюции выработались мощные нервные и эндокринные механизмы, воздействующие как на гомеостатическую функцию печени, так и на спрсобность различных клеток потреблять глюкозу.
При рассмотрении гормонального звена регуляции обращает на себя внимание тот факт, что инсулин является единственным гормоном, обладающим резким сахаропонижающим действием. Остальные гормоны, влияющие на углеводный обмен в сторону увеличения уровня глюкозы в крови, получили название диабетогенных или контринсулярных. Инсулин выступает в роли репрессора синтеза ключевых ферментов глюконеогенеза и индуктора синтеза гексокиназы, фосфофруктокиназы, пируваткиназы и гликоген (крахмал)-синтазы. Глюкокортикоиды являются индукторами синтеза ферментов глюконеогенеза.
Инсулин секретируется ß-клетками островков Лангерганса поджелудочной железы в форме проинсулина. Основным проявлением недостаточности инсулина является повышение уровня глюкозы в крови (гипергликемия), избыточное выведение глюкозы с мочой (глюкозурия) и понижение содержания гликогена в печени. Недостаточность инсулина подавляет биосинтез жирных кислот из глюкозы и ацетата, а также биосинтез белков; усиливает синтез ферментов, участвующих в глюконеогенезе; нарушает соотношение между гликолизом и глюконеогенезом.
Наиболее вероятной в настоящее время представляется мембранная локализация первичного действия инсулина. Получены доказательства наличия специфического акцептора инсулина на внешней плазматической мембране жировых клеток, а также образование инсулин-рецепторного комплекса. Предполагают, что в жировых клетках и частично клетках печени в передаче инсулинового сигнала принимают участие аденилатциклаза и цАМФ. В мышцах инсулин легко проникает внутрь клетки.
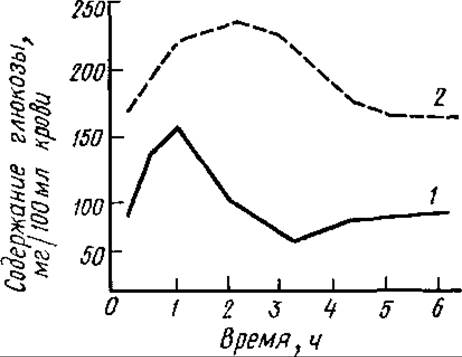
Рис. 6.11. Динамика содержания глюкозы в крови человека после приема сахаров:
1 — норма, 2 — при диабете
Мышцы и печень при недостатке инсулина не способны использовать глюкозу даже при высоком ее содержании в крови. Это явление получило название «голод среди изобилия». Ткани мозга и миокарда по мере нарастания гипергликемии усиливают утилизацию глюкозы. В этом достаточно ограниченном аспекте гипергликемию можно рассматривать как полезное приспособление. Недостаточность выделения инсулина лежит в основе возникновения заболевания — диабета. Многие последствия диабета напоминают эффект углеводного голодания, хотя содержание глюкозы в крови при этом заболевании резко повышается.
Глюкагон — гормон, продуцируемый а-клетками поджелудочной железы, активирует расщепление гликогена в печени, в результате чего освобождается глюкоза, поступающая в кровь.
Адреналин — гормон мозгового слоя надпочечников. Совместно с глюкагоном активирует гликогенфосфорилазу печени и мышц, увеличивает содержание глюкозы в крови. Фермент встречается в двух формах — активной (фосфорилаза а) и неактивной (фосфорилаза b). Молекулярная масса фосфорилазы а составляет 380 000. Фосфорилаза а состоит из четырех субъединиц, каждая из которых содержит остаток фосфосерина и молекулу кофермента — пиридоксальфосфата, ковалентно связанную с остатком лизина. Фосфатаза фосфорилазы вызывает гидролитическое расщепление связи фосфатной группы с остатком серина и образование димеров.
Неактивная гликоген-фосфорилаза b, состоящая из двух субъединиц, фосфорилируется в активную гликоген-фосфорилазу а киназой фосфорилазы. Последняя активируется циклическим АМФ, образуемым аденилатциклазой. Адреналин стимулирует образование цАМФ аденилатциклазой. Таким образом, адреналин ускоряет расщепление гликогена. С другой стороны, стимулируя аденилатциклазу, адреналин подавляет синтез гликогена из УДФ-глюкозы за счет накопления формы гликоген (крахмал)-синтазы, нуждающейся в высоких концентрациях глюкозо-6-фосфата.
Механизмы действия адреналина и глюкагона на поддержание уровня глюкозы в крови аналогичны.
Глюкокортикоиды (гормоны коркового слоя надпочечников) усиливают глюконеогенез — новообразование сахара из неуглеводов. Это приводит к увеличению количества глюкозы в крови и гликогена в печени. Соматотропний гормон гипофиза уменьшает утилизацию глюкозы периферическими тканями, усиливает глюконеогенез, угнетает продукцию инсулина, в итоге повышает содержание глюкозы в крови. Тироксин и трийодтиронин (гормоны щитовидной железы) в умеренных дозах усиливают всасывание моносахаридов в кишечнике. Избыток этих гормонов тормозит окислительное фосфорилирование и способствует повышению концентрации глюкозы в крови.
Содержание гормонов в крови находится под контролем центральной нервной системы, осуществляющей контроль за уровнем глюкозы в крови через эндокринную систему. Однако помимо опосредованного влияния на уровень глюкозы в крови центральная нервная система (ЦНС) осуществляет и прямое воздействие. Снижение концентрации глюкозы в крови ниже 60—70 мг% приводит к рефлекторному возбуждению соответствующих центров, расположенных в гипоталамусе. Возбуждение передается из ЦНС по нервным путям спинного мозга, переходит в симпатический ствол и по симпатическому нерву достигает печени. В результате такого возбуждения нервной системы часть гликогена печени распадается с образованием глюкозы. Этот процесс получил название мобилизации глюкозы. Когда концентрация глюкозы возвращается к исходному уровню, импульсы, идущие из ЦНС, ослабевают и расщепление гликогена задерживается.
Таким образом, за счет контроля со стороны ЦНС и эндокринной системы в крови автоматически поддерживается постоянный уровень глюкозы, происходит саморегуляция, которая может осуществляться на различных уровнях. Так, например, кровь с избыточным содержанием глюкозы, достигая поджелудочной железы, непосредственно стимулирует выделение инсулина. Последний усиливает поглощение глюкозы тканями, использование ее на синтез гликогена, в результате концентрация глюкозы снижается до нормы. На содержание глюкозы в крови, как показали исследования К. М. Быкова, определенное влияние оказывает и кора головного мозга. Примером этого является эмоциональная гипергликемия — повышенное содержание глюкозы в крови в возбужденном состоянии (у спортсменов перед стартом, у студентов перед экзаменом).