БИОХИМИЯ - Основные регуляторы и биологические жидкости человеческого организма - 2016 год
1. ФЕРМЕНТЫ
1.4. Факторы, влияющие на активность ферментов
Эффективность действия ферментов зависит от ряда факторов: температуры (оптимальная температура обычно лежит в пределах 30 - 50 °С), рН среды, некоторых специфических веществ, называемых активаторами и ингибиторами, а также от концентрации фермента и субстрата.
1.4.1. Температура (t, °С)
Поскольку ферменты имеют белковую природу, они термолабильны и при повышении температуры из-за необратимой денатурации теряют свою природную пространственную структуру, а, следовательно, и биологическую активность. В результате происходит уменьшение скорости, катализируемой ими реакции (рис. 3). Однако имеется несколько термостабильных ферментов, сохраняющих каталитическую активность при температуре 100 °С, к ним относится фермент мышечной ткани миокиназа.
Рис. 3. Зависимость скорости ферментативной реакции от температуры
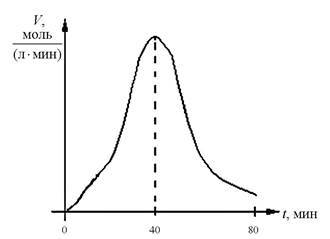
При понижении температуры активность ферментов падает, но она восстанавливается при повышении температуры до оптимального значения.
1.4.2. Реакция среды (рН)
При изменении величины рН среды активность ферментов снижается, так как изменяется заряд белковой молекулы и нарушается структура активного центра (рис. 4).
Рис. 4. Зависимость скорости ферментативной реакции от величины рН
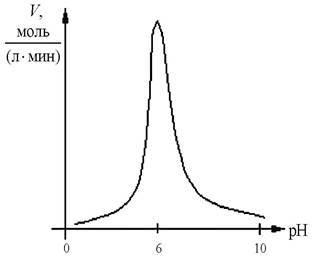
Максимально активны ферменты при рН = рI (поскольку в изоэлектрической точке заряд молекулы белка равен нулю).
1.4.3. Концентрация субстрата (СE)
С ростом концентрации субстрата скорость ферментативной реакции увеличивается до определенного предела - до тех пор, пока не будут заняты все активные центры фермента (рис. 5).
Рис. 5. Зависимость скорости ферментативной реакции от концентрации субстрата
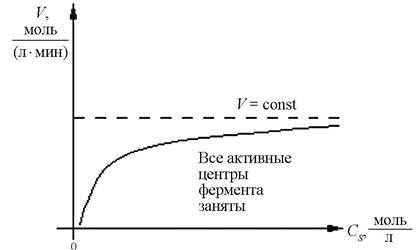
Дальнейшее увеличение концентрации субстрата на скорость реакции не влияет.
1.4.4. Концентрация фермента (СЕ)
С повышением концентрации фермента увеличивается и скорость химической реакции (рис. 6).
Рис. 6. Зависимость скорости ферментативной реакции от концентрации фермента
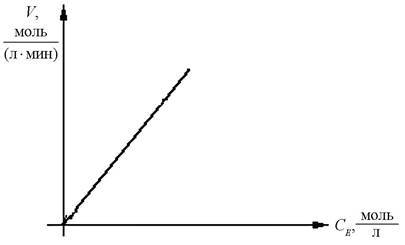
Скорость ферментативной реакции прямо пропорциональна концентрации соответствующего фермента.
1.4.5. Активаторы
Активаторы повышают скорость химической реакции за счет увеличения активности фермента. Ими могут быть ионы металлов (Na+, К+ , Са2+, Мg2+, Mn2+, Со2+, Ni2+), а также некоторые анионы, например Сl-.
Так, АТФ-аза мышц, катализирующая процесс превращения АТФ в АДФ, активируется ионами Са2+:
![]()
Ионы Сl- активируют амилазу слюны, расщепляющую крахмал с образованием декстринов и мальтозы.
Многие ферменты для проявления каталитической активности нуждаются в присутствии некоторых веществ непептидной природы - кофакторов.
1.4.6. Ингибиторы
Ингибиторы угнетают активность фермента. Иногда одно и то же вещество при различных концентрациях может быть и активатором, и ингибитором. Ионы тяжелых металлов (Аg+, Нg2+, Рb2+) угнетают активность почти всех ферментов.