Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ II. ЗАГАЛЬНІ ЗАКОНОМІРНОСТІ МЕТАБОЛІЗМУ
ГЛАВА 9. БІОЕНЕРГЕТИЧНІ ПРОЦЕСИ: ТРАНСПОРТ ЕЛЕКТРОНІВ; ОКИСНЕ ФОСФОРИЛЮВАННЯ В МІТОХОНДРІЯХ
9.3. МОЛЕКУЛЯРНА ОРГАНІЗАЦІЯ ЛАНЦЮГА БІОЛОГІЧНОГО ОКИСЛЕННЯ В МІТОХОНДРІЯХ
Система біологічного окислення, що локалізована в мембранах мітохондрій , здійснює дегідрування органічних субстратів та послідовний перенос відновлю- вальних еквівалентів на кисень через ряд проміжних переносників — транспортерів електронів та протонів. Ця система організована у вигляді ланцюга електронного транспорту, або дихального ланцюга мітохондрій.
Дихальний ланцюг мітохондрій — сукупність молекулярних компонентів (ферментів та коферментів), які вбудовані в ліпідний матрикс внутрішніх мітохондріальних мембран і здійснюють окислення біологічних субстратів та послідовне, ступеневе транспортування відновлювальних еквівалентів на кисень з утворенням молекули води.
Компоненти дихального ланцюга мітохондрій:
НАДН-дегідрогеназа — компонент дихального ланцюга, що окислює відновлений НАД+ (НАДН); входить до складу молекулярного комплексу внутрішніх мітохондріальних мембран НАДН-коензим Q-редуктази.
Сукцинатдегідрогеназа — компонент дихального ланцюга, що окислює янтарну кислоту; входить до складу молекулярного комплексу сукцинат-коензим Q-редуктази.
Коензим Q (убіхінон) — ліпідорозчинний хінон з ізопреноїдним бічним ланцюгом, що містить у тканинах ссавців десять п’ятивуглецевих ізопреноїдних залишків (Q10). Убіхінон виконує функцію колектора відновлювальних еквівалентів, акцептуючи протони та електрони не тільки від ФМН-залежної НАДН-дегідрогенази, а й від ФАД-залежних дегідрогеназ мітохондрій (сукцинатдегідрогенази та дегідрогеназ системи β-окислення жирних кислот тощо).
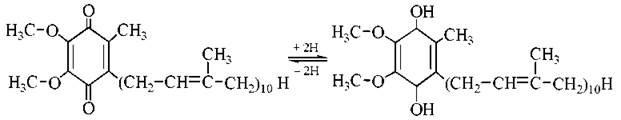
Цитохроми мітохондрій:
Цитохром b.
Цитохром c1.
Цитохром c.
Цитохром a.
Цитохром a3.
Залізо-сіркові білки, що містять негемове залізо (FeS), — це білки, асоційовані з флавопротеїнами мітохондрій (металофлавопротеїнами) та цитохромом b.
Послідовність передавання електронів від одного компонента дихального ланцюга мітохондрій до іншого визначається стандартними окислювально- відновлювальними потенціалами цих компонентів — табл. 9.1.
Таблиця 9.1. Стандартні окислювально-відновлювальні потенціали компонентів дихального ланцюга мітохондрій
Окислювально-відновлювальна пара |
Е0’, в |
НАДН / НАД+ |
- 0,32 |
Лактат / піруват |
- 0,19 |
Сукцинат / фумарат |
+ 0,03 |
Убіхінол / убіхінон |
+ 0,10 |
Цитохром b (Fe2+ / Fe3+) |
+ 0,12 |
Цитохром c1 (Fe2+/ Fe3+) |
+ 0,21 |
Цитохром c (Fe2+ / Fe3+) |
+ 0,25 |
Цитохром a (Fe2+ / Fe3+) |
+ 0,29 |
Цитохром a3 (Fe2+/ Fe3+) |
+ 0,55 |
H2O / 1/2O2 |
+ 0,82 |
Окремі ферменти та коферменти, що складають дихальний ланцюг, структурно об’єднані між собою в надмолекулярні (мультиензимні) комплекси, інтегровані в ліпідний матрикс внутрішніх мембран мітохондрій, що створює стеричні умови, необхідні для ефективного перебігу окислювально-відновлювальних реакцій.
Комплекси дихального ланцюга внутрішніх мембран мітохондрій
НАДН-коензим Q-редуктаза — ферментний комплекс (являє собою флавопротеїн, що містить ФМН), який окислює НАДН і передає відновлювальні еквіваленти на коензим Q (убіхінон); у складі НАДН-коензим Q-редуктази НАДН- дегідрогеназа асоційована з FeS-білками (так званий комплекс I).
Сукцинат-коензим Q-редуктаза — ферментний комплекс (ФАД-залежний флавопротеїн), який окислює сукцинат, відновлюючи коензим Q; до складу комплексу входить флавопротеїн сукцинатдегідрогеназа, асоційована з Fe S-білком (комплекс II).
Коензим Q-цитохром с-редуктаза (убіхінолдегідрогеназа) — ферментний комплекс, що складається з цитохрому b, FeS-білка та цитохрому c1; ферментний комплекс транспортує електрони з відновленого коензиму Q (QH,) на цитохром c (комплекс III).
Цитохром с-оксидаза — ферментний комплекс, що складається з цитохромів а та а3 (комплекс IV); комплекс здійснює кінцеву стадію біологічного окислення — відновлення електронами молекулярного кисню; він містить іони міді, як і інші оксидази.
Шляхи включення відновлювальних еквівалентів у дихальний ланцюг мітохондрій
1. Включення протонів і електронів у дихальний ланцюг через ФМН флавопротеїну НАДН-коензим Q-редуктази. Цим шляхом на молекулу убіхінону надходять відновлювальні еквіваленти, відщеплені від відповідних субстратів НАДН-залежними дегідрогеназами.
2. Включення протонів і електронів у дихальний ланцюг через ФАД сукцинаткоензим Q-редуктази та деяких інших ФАД-залежних дегідрогеназ. Цим шляхом на убіхінон надходять відновлювальні еквіваленти від янтарної кислоти — метаболіту циклу трикарбонових кислот та певних інших субстратів.
Послідовність включення окремих компонентів системи транспорту електронів і протонів у дихальний ланцюг мітохондрій подано на рисунку 9.2.
Як випливає з наведеної схеми, дихальний ланцюг мітохондрій організований таким чином, що перенос у ньому відновлювальних еквівалентів (електронів) відбувається в напрямку від електронегативного кінця (флавопротеїнів) до електропозитивного цитохрому а3. Більшість метаболітів (субстрати гліколізу, циклу трикарбонових кислот тощо) передає атоми водню в дихальний ланцюг через НАДН-дегідрогеназу (Е-ФМН); сукцинат та КоА-похідні жирних кислот віддають електрони та протони на коензим Q через специфічні флавопротеїни (Е-ФАД), минаючи ФМН-залежний флавопротеїн.
Убіхінон є останнім компонентом дихального ланцюга мітохондрій, що здатний транспортувати як електрони, так і протони. На рівні цитохрому b шляхи електронів і протонів розділяються — протони переходять з внутрішньої поверхні мітохондріальної мембрани на зовнішню, а електрони через послідовність цитохромів транспортуються на цитохром а3, який відновлює кисень:
![]()
Взаємодія відновленого кисню з вільними протонами мітохондріального матриксу призводить до утворення молекули води:
![]()
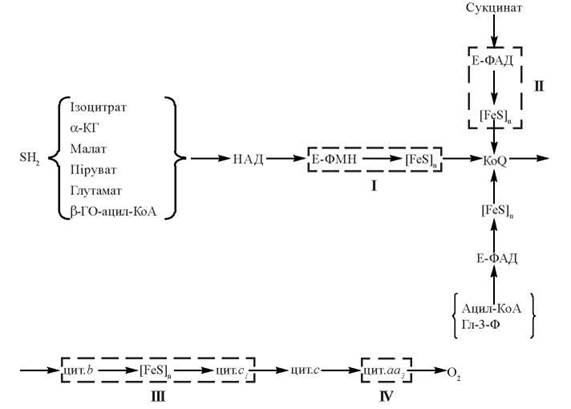
Рис. 9.2. Схема організації дихального ланцюга мітохондрій. I-IV — електронотранспортні комплекси мітохондріальних мембран. Позначення: α-КГ — α-кетоглутарат; β-ГО-ацил-КоА — β-гідроксиацил-КоА; Гл-3-Ф — гліцерол-3-фосфат.