Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ III. МЕТАБОЛІЗМ ОСНОВНИХ КЛАСІВ БІОМОЛЕКУЛ
ГЛАВА 18. МЕТАБОЛІЗМ АМІНОКИСЛОТ. ІІ. СПЕЦІАЛІЗОВАНІ ШЛЯХИ ОБМІНУ
18.3. СПЕЦІАЛІЗОВАНІ ШЛЯХИ ОБМІНУ ЦИКЛІЧНИХ АМІНОКИСЛОТ
Обмін фенілаланіну та тирозину
Особливістю метаболізму в тваринних організмах циклічних амінокислот фенілаланіну та тирозину є утворення з них численних фізіологічно активних сполук гормональної та медіаторної дії, а саме: катехоламінів (адреналіну, норадреналіну), тиреоїдних гормонів, меланінів (рис. 18.3).
1. Шляхи метаболізму фенілаланіну
1.1. Катаболічний шлях обміну полягає у втраті фенілаланіном аміногрупи (в реакції трансамінування) з утворенням фенілпірувату та кінцевого метаболіту фенілацетату, що екскретується з організму.
1.2. Шлях синтезу фізіологічно активних сполук починається з перетворення фенілаланіну на тирозин при дії ферменту фенілаланінгідроксилази з подальшим перетворенням тирозину (див. нижче).
2. Шляхи метаболізму тирозину
2.1. Катаболічний шлях обміну полягає у трансамінуванні тирозину і перетворенні на p-оксифенілпіруват, який окислюється до гомогентизинової кислоти у складній реакції, коферментну роль у якій виконує аскорбінова кислота (вітамін С); подальші перетворення полягають в окисленні гомогентизату до фумарилацетоацетату (фермент оксидаза гомогентизинової кислоти) та розщепленні фумарилацетоацетату до фумарату та ацетоацетату.
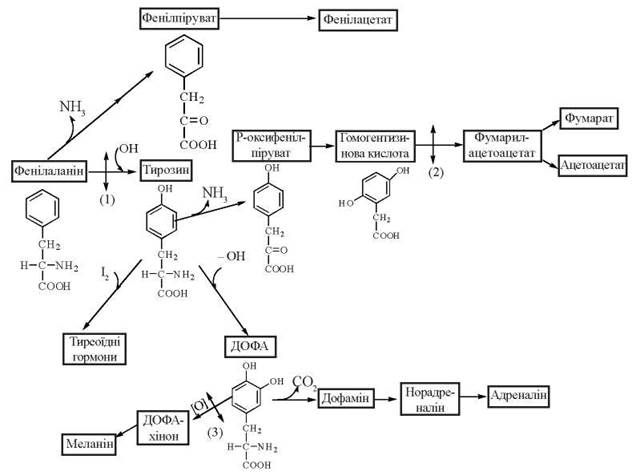
Рис. 18.3. Шляхи метаболізму циклічних амінокислот.
![]() — пункти метаболічного блоку: (1) — фенілкетонурія; (2) — алкаптонурія; (3) — альбінізм.
— пункти метаболічного блоку: (1) — фенілкетонурія; (2) — алкаптонурія; (3) — альбінізм.
2.2. Шлях синтезу катехоламінів та меланінів (пігментів шкіри). Шлях починається з окислення тирозину за участю специфічної гідроксилази до 3,4-діоксифенілаланіну (ДОФА), на рівні якого відбувається дивергенція двох обмінних шляхів: утворення катехоламінів (через декарбоксилювання до дофаміну) та меланінів (через окислення тирозиназою до дофахінону).
2.3. Шлях синтезу тиреоїдних гормонів — реалізується в клітинах щитовидної залози і полягає в утворенні йодованих тиронінів.
Спадкові порушення обміну циклічних амінокислот
Вперше уроджене порушення обміну циклічних амінокислот — алкаптонурія — була виявлена англійським лікарем А. Геродом (A. Garrod) в 1902 р., який до того ж довів генетичне походження захворювання, що стало вирішальною подією в становленні уявлення про спадкові порушення метаболізму.
Фенілкетонурія — ензимопатія, спричинена генетичним дефектом синтезу фенілаланінгідроксилази. Внаслідок блокування утворення тирозину з фенілаланіну останній в збільшеній кількості надходить на шлях утворення фенілпірувату та фенілацетату, які в надмірних концентраціях накопичуються в організмі хворих. Концентрація фенілаланіну в крові хворих зростає в десятки разів, досягаючи 100-800 мг/л (норма — 10-40 мг/л). Патологія проявляє себе ранніми порушеннями психічного розвитку дитини — фенілпіровиноградна олігофренія(oligophreniaphenylpyruvica).
Алкаптонурія — ензимопатія, що викликана генетично детермінованою недостатністю ферменту оксидази гомогентизинової кислоти. Характерним проявом захворювання є надмірне виділення гомогентизинової кислоти із сечею, яка при додаванні лугів набуває темного забарвлення; акумуляція гомогентизату в тканинах суглобів призводить до розвитку артритів.
Альбінізм — ензимопатія, біохімічною основою якої є спадкова недостатність ферменту тирозинази, що каталізує реакції, необхідні для утворення чорних пігментів меланінів. Відсутність меланінів у меланоцитах шкіри проявляється недостатньою (або відсутньою) пігментацією шкіри та волосся, підвищеною чутливістю шкіри до сонячного світла, порушенням зору.
Обмін триптофану
L-Триптофан є незамінною амінокислотою для організму людини та вищих тварин у зв’язку з відсутністю ферментних систем синтезу його вуглецевого скелета. Разом з тим, триптофан є попередником у біосинтезі таких фізіологічно активних сполук, як речовина гормональної і медіаторної дії серотонін та нікотинова кислота (вітамін РР), який синтезується в тваринному організмі у формі НАД. Існують два основні біохімічні шляхи перетворення триптофану (рис. 18.4):
- кінуреніновий шлях, за яким метаболізується понад 95 % ендогенного триптофану;
- серотоніновий шлях, що складає в кількісному відношенні близько 1% загальної кількості триптофану в організмі.
1. Вступ триптофану на серотоніновий шлях починається з гідроксилювання амінокислоти до 5-окситриптофану, який після декарбоксилювання перетворюється на серотонін.
В організмі людини серотонін підлягає окислювальному дезамінуванню з утворенням оксііндолоцтової кислоти, яка виділяється з сечею. Екскреція оксііндолацетату значно збільшена при карциноїдному синдромі, коли за серотоніновим шляхом перетворюється до 60 % триптофану.
2. Катаболізм триптофану кінуреніновим шляхом починається з окислення триптофану при дії гемвмісного ферменту триптофанпіролази до формілкінуреніну, який після відщеплення мурашиної кислоти перетворюється на кінуренін та 3-оксикінуренін. Подальші перетворення 3-оксикінуреніну пов’язані з дією ПАЛФ-залежного ферменту кінуренінази, яка розщеплює цей інтермедіат до аланіну та 3-оксіантранілової кислоти. 3-Оксіантранілова кислота — метаболіт, що після складних багатоступеневих перетворень призводить до хінолінової кислоти — попередника в синтезі нікотинаміду у формі коферменту НАД.
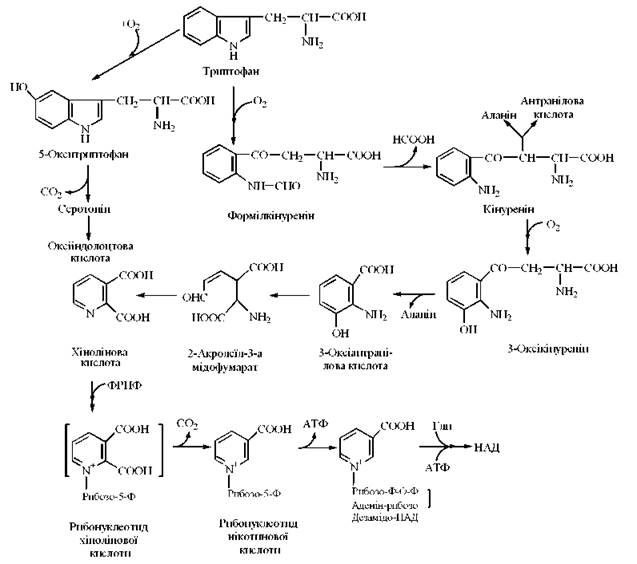
Рис. 18.4. Метаболічні перетворення триптофану.