Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ IV. МОЛЕКУЛЯРНІ МЕХАНІЗМИ СПАДКОВОСТІ ТА РЕАЛІЗАЦІЇ ГЕНЕТИЧНОЇ ІНФОРМАЦІЇ
ГЛАВА 19. БІОСИНТЕЗ НУКЛЕОТИДІВ
19.3. БІОСИНТЕЗ ДЕЗОКСИРИБОНУКЛЕОТИДІВ
Біосинтез РНК різних класів вимагає наявності пуринових (АТФ, ГТФ) та піримідинових (ЦТФ, УТФ) рибонуклеотидів, тоді як для біосинтезу генетичних ДНК необхідні дезоксирибонуклеотиди пуринового — дАТФ, дГТФ — та піримідинового — дЦТФ, дТТФ (ТТФ) ряду.
Попередниками дезоксирибонуклеотидів у клітинах є рибонуклеотиди у формі нуклеозиддифосфатів (НДФ) (переважно) та нуклеозидтрифосфатів (НТФ).
Механізм перетворення рибонуклеотидів на дезоксирибонуклеотиди
Перетворення НДФ на відповідні дНДФ досягається шляхом відновлення гідроксильної групи при С-2' рибози з утворенням 2'-дезоксирибози. Донором відновлювальних еквівалентів у цьому процесі є відновлений НАДФ (НАДФН + Н+):
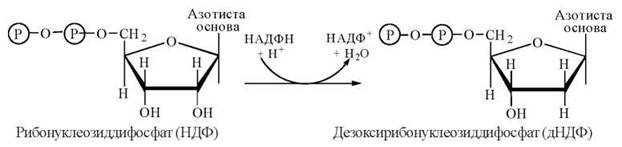
Вказана реакція є, в дійсності, складним біохімічним процесом, в якому беруть участь: низькомолекулярний (м.м. — 12 кД) SH-вмісний білок тіоредоксин і два окислювально-відновлювальні ферменти (редуктази) — тіоредоксинредуктаза та рибонуклеотидредуктаза, шо складають в сукупності електроно-транспортний ланцюг відновлення НДФ до дНДФ (рис. 19.4).
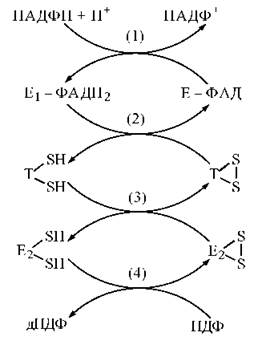
Рис. 19.4. Схема переносу відновлювальних еквівалентів від (НАДФН + Н+) на рибонуклеозиддифосфати:
Е1 — ФАДН — тіоредоксинредуктаза;
рибонуклеотидредуктаза;
SH
Т — тіоредоксин.
Процес відновлення НДФ до дНДФ за рахунок протонів та електронів (НАДФН + Н+) складається з таких реакцій:
(1) переносу водню від (НАДФН + Н+) на ФАД флавінового ферменту тіоредоксинредуктази;
(2) переносу водню від відновленої тіоредоксинредуктази на SH-групи тіоредоксину;
(3) переносу водню від відновленого тіоредоксину на SH-групи рибонуклеотидредуктази;
(4) переносу водню від відновлених сульфгідрильних груп рибонуклеотидредуктаза на НДФ з утворенням дНДФ.
Утворення дАТФ, дГТФ та дУТФ
За розглянутим механізмом іде утворення пуринових дезоксирибонуклеотидів:
![]()
та піримідинового дезоксирибонуклеотиду дУДФ:
![]()
дНДФ, які утворилися в цих реакціях, перетворюються на відповідні дНТФ (попередники в біосинтезі ДНК) в реакціях, що каталізуються нуклеозиддифосфокіназами:

Утворення тимідилових нуклеотидів
Біосинтез тимідилових нуклеотидів, що також містять 2'-дезоксирибозу, починається з тимідилату (тимідин-5'-монофосфату, дТМФ, ТМФ). Безпосереднім попередником дТМФ є дезоксиуридин-5'-монофосфат (дУМФ), який утворюється з дезоксиуридин-5'-дифосфату (дУДФ) внаслідок його дефосфорилювання:
![]()
Перетворення дУМФ на дТМФ — заключний крок в утворенні нуклеотиду, що потрібний для біосинтезу ДНК — відбувається шляхом метилювання дУМФ у такій реакції:
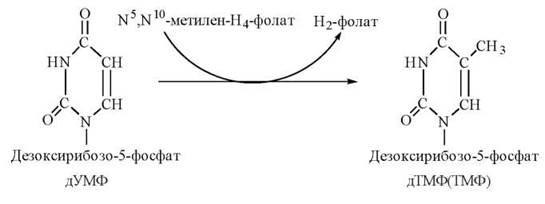
Процес каталізується ферментом тимідилатсинтазою, коферментом якої є N5,N10- метилен-Н4-фолат, що в результаті реакції окислюється до дигідрофолату. Подальше функціонування фолату як коферменту вимагає регенерації тетрагідрофолату в реакції, що каталізується дигідрофолатредуктазою:
![]()
Утворення тимідилових нуклеозидди- і трифосфатів — дТДФ(ТДФ), дТТФ(ТТФ) відбувається за рахунок їх фосфорилювання АТФ у кіназних реакціях:
![]()
Інгібітори синтезу дТМФ як протипухлинні засоби
Біосинтез нових молекул чотирьох дезоксирибонуклеозидтрифосфатів (дАТФ, дГТФ, дЦТФ та дТТФ), що необхідні для реплікації ДНК, практично не відбувається у фазі мітотичного (репродуктивного) спокою клітини (G0) і активується на стадіях клітинного циклу, що передують мітозу (глава 20). У зв’язку з цим, хімічні сполуки, які блокують синтез de novo зазначених дНТФ, унеможливлюють подвоєння (реплікацію) геномної ДНК та поділ клітин — концепція, що покладена в основу фармакологічної дії багатьох протипухлинних лікарських засобів.
Саме за таким механізмом реалізується затримка поділу клітин злоякісних пухлин, яка відбувається під впливом препаратів, що блокують синтез тимідилату дТМФ (рис. 19.5), а саме:
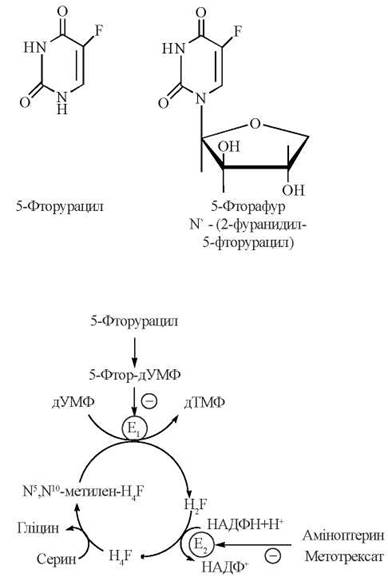
Рис. 19.5. Механізми антипухлинної дії сполук, що блокують синтез дТМФ (E1 — тимідилатсинтаза; Е2 — дигідрофолатредуктаза; H4F — тетрагідрофолат; H2F — дигідрофолат).
1) структурних аналогів дУМФ, що здатні до взаємодії з тимідилатсинтазою, блокуючи її каталітичну дію за механізмом конкурентного інгібірування; прикладом такого механізму є ефект протипухлинних засобів антиметаболітної дії 5-Фторурацилу (аналога урацилу) та Фторафуру (аналога уридину, що в організмі людини також утворює вільний 5-фторурацил):
Після надходження в організм 5-фторурацил перетворюється на 5-фтордезоксиуридин-5'-монофосфат (5-фтор-дУМФ), тобто безпосередній структурний аналог дУМФ — субстрату тимідилатсинтази; сполучення 5-фтор-дУМФ з ферментом протидіє зв’язуванню активного центру останнього із справжнім субстратом (дУМФ), що блокує утворення дТМФ;
2) похідних птерину Аміноптерину та Метотрексату, що, маючи подібність до частини молекули фолієвої кислоти, діють у біохімічних реакціях як її структурні аналоги і, у зв’язку з цим, виступають як конкурентні інгібітори дигідрофолатредуктази; гальмування каталітичної дії цього ферменту протидіє регенерації Н4-фолату з Н2-фолату і, таким чином, порушує біосинтез дТМФ.