Практическая химия белка - А. Дарбре 1989
Определение С-концевой последовательности аминокислот
Определение С-концевой последовательности
Расщепление при помощи цианамида
Предложена новая методика С-концевого последовательного расщепления белков (пептидов) [88], обладающего очевидными преимуществами по сравнению с тиоцианатным расщеплением(рис. 18.11). На первой стадии проводят при помощи карбодиимида конденсацию пептида с S-алкилтиурониевой солью, затем производное С-концевой аминокислоты отщепляют в водной среде при pH 10:11,5. Реакция отщепления проходит в две четко различимые стадии. Алкильная часть ацилированной изотиомочевины удаляется при обработке основанием, давая ацилцианамид. Цианогруппа подвергается нуклеофильной атаке атомом азота пептидной связи. Затем происходят циклизация и отщепление иминогидантоина от укороченного пептида. Иминогидантоины — довольно полярные соединения и в целом проявляют хроматографические свойства исходных аминокислот. Их можно детектировать после ТСХ опрыскиванием пластинок раствором нитропруссида — феррицианида или ГЖХ триметилсилилированных производных [88].

РИС. 18.11. Цианамидное расщепление [88].
Было найдено, что иодид S-н-бутилтиурония — наиболее реакционноспособный из всех изученных солей изотиурония. При взаимодействии пептида с этим реагентом в пиридине (безводном или содержащем ~1% концентрированной НСl) при 50 °С в течение 10—15 мин в присутствии 0,25 М карбодиимида (например, ДЦК) выход быстро протекающей реакции присоединения составил ~99%. Подобные результаты получены при использовании 0,1 М растворов реагентов и продолжительности реакции 20 мин. Присутствие воды снижает скорость реакции, особенно при использовании ДЦК, поэтому для получения больших выходов необходим большой избыток реагента. Реакцию отщепления можно проводить как с избытком, так и без избытка реагента. Единственным требованием является наличие водного раствора основания с pH 10—11,5. Были найдены условия реакции, близкие к оптимальным: пиридин — 1 М водный триметиламин (1:1), время реакции 10 мин при 50 °С. В этих условиях полный цикл расщепления модельного пептида проходит с выходом 96%. Метод находится в стадии разработки, но уже сейчас очевидны его ограничения — невозможность отщепления С-концевого Pro (из-за стерических затруднений) и Asp (из-за образования циклического ангидрида в присутствии карбодиимида) [88].
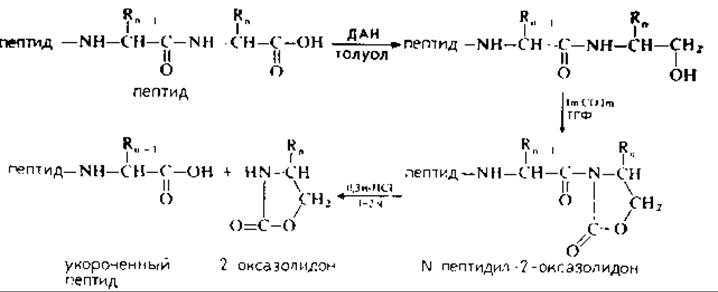
РИС. 18.12. Определение С-концевой последовательности избирательным восстановлением пептида дигидробис-(2-метоксиэтокси) алюминатом натрия (ДАН), превращением ациламиноспирта в пептидил-2-оксазолидон. Мягкий гидролиз последнего дает укороченный пептид и 2-оксазолидон С-концевой аминокислоты [75].