Практическая химия белка - А. Дарбре 1989
Фрагментация полипептидов химическими методами
Расщепление по остатку тирозина
N-Бромосукцинимид
При отсутствии в молекуле белка остатков триптофана избирательное расщепление по тирозину можно проводить с помощью N-бромосукцинимида [33, 148, 165]. При наличии триптофана пептидные связи тирозина будут расщепляться только при большом избытке реагента. По всей вероятности, расщепление по тирозину идет по следующему механизму.
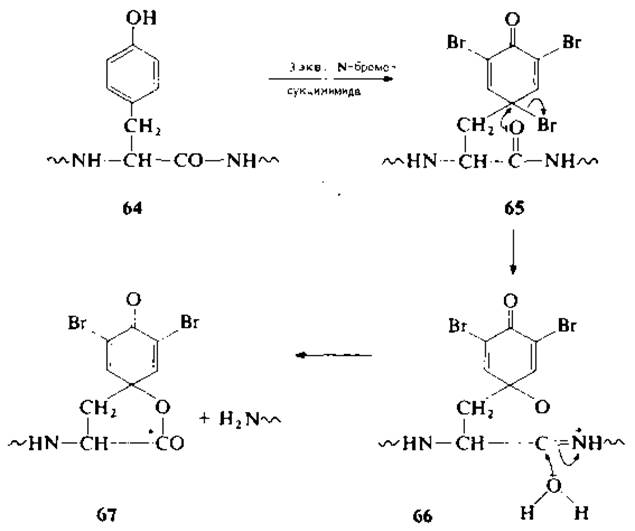
Остаток тирозина при взаимодействии с 2 экв. N-бромосукцинимида бромируется с образованием о/о'-дибромотирозина, который при реакции с 1 экв. (третьим) реагента превращается в трибромодиенон (65). Последний вступает в 1,5-взаимодействие с карбонильной группой, образуя спиро-у-иминолактон (66), легко гидролизующийся до дибромодиенонспиролактона (67) и пептидного фрагмента со свободной аминогруппой. Диенонспиролактон, который был выделен и идентифицирован [33, 165], — сильный хромофор с λmах = 260 нм (ε = 10 000:11 000). В случае простых пептидов контроль за ходом реакции можно вести по поглощению при 260 нм. N-Пептидная связь остатка тирозина устойчива в кислой среде при избытке N-бромосукцинимида.
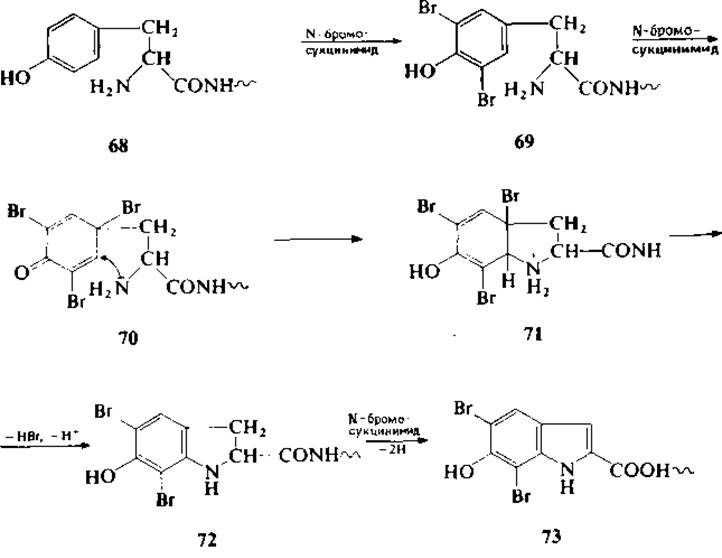
На модельных пептидах с N-концевым тирозином показано [208], что свободная cc-аминогруппа тирозина принимает участие в альтернативной последовательности реакций, включающей внутреннее присоединение по Михаэлю в промежуточном трибромодиеноне (70) с образованием в конечном счете дибромо-6-гидроксииндолпроизводного (73) (последовательность реакций 68→73).
Расщепление с помощью N-бромосукцинимида пептидной связи тирозина успешно применяется в структурных исследованиях белков и пептидов. В случае S-карбоксиметилрибонуклеазы, не содержащей триптофана, пептидные связи шести остатков тирозина расщеплялись с выходом 30—65% [148, 181]. Поскольку гистоны не имеют триптофана, но содержат тирозин, расщепление N-бромосукцинимидом находит широкое применение при анализе этих белков [19, 147]. Выход обычно неколичественный, но улучшается при избытке реагента (в последнем случае могут идти побочные реакции по остаткам гистидина и серусодержащим аминокислотам).
2.6.1.1. Методика [86]. К раствору гистона H1 (1 мг/мл) в 50%-ной уксусной кислоте прибавляют N-бромосукцинимид (0,09 мг/мг белка. После инкубации при 20 °С в течение 2 ч к реакционной смеси добавляют вторую порцию N-бромосукцинимида, равную первой, и вновь инкубируют в течение 4 ч.
В заключение 10-кратно разбавляют дистиллированной водой и высушивают диофильно. Пептидные фрагменты фракционируют в 0,01 М НСl на колонке с сефадексом G-100.