БИОХИМИЯ И МОЛЕКУЛЯРНАЯ БИОЛОГИЯ - В. ЭЛЛИОТ - 2002
ГЛАВА 11. СИНТЕЗ ГЛЮКОЗЫ В ОРГАНИЗМЕ (ГЛЮКОНЕОГЕНЕЗ)
Организм может синтезировать глюкозу из соединений, способных предварительно превратиться в пируват, т. е. из большинства аминокислот и лактата, поступающего в кровь из работающих мышц. Совокупность таких превращений называют глюконеогенезом. Глюкоза не может быть синтезирована из ацетил-СоА и жирных кислот. Глюконеогенез позволяет как бы сохранить энергию превращений в виде гликогена. Однако помимо этого глюконеогенез в ряде случаев спасает организм от гибели.
Мозг требует непрерывного обеспечения глюкозой. Это означает, что во избежание комы или смерти уровень глюкозы в крови должен поддерживаться в пределах нормы. Между тем запасы гликогена в печени невелики и полностью исчерпываются после суточного голодания.
Люди, однако, остаются живы и при более продолжительном отсутствии пищи. В этом случае поступление глюкозы в кровь обеспечивается печенью. Ни один другой орган (кроме почек, вклад которых невелик) не способен выполнить эту задачу. После суточного голодания печень должна удовлетворить потребность человека в глюкозе (около 100 г в день).
На удовлетворение основных энергетических потребностей организма запаса жиров хватает на недели, но жирные кислоты не проникают через гематоэнцефалический барьер и потому не могут использоваться мозгом. Мобилизация жиров приводит к образованию кетоновых тел, чье присутствие в крови в какой-то мере уменьшает потребность в глюкозе (см. с. 84), однако необходимость ее синтеза при этом не исчезает. Потребность мозга в глюкозе при голодании остается прежней. К тому же мозг лишь один из основных ее потребителей. В глюкозе нуждаются клетки сетчатки, мозгового слоя почек, эритроциты, т. е. все ткани и клетки, жизнедеятельность которых в значительной мере или полностью (эритроциты вообще лишены митохондрий!) поддерживается анаэробным метаболизмом.
Глюконеогенез в печени начинается с пирувата, который служит исходным соединением и при синтезе жирных кислот. Казалось бы, он может связать две ветви метаболизма. Однако превращение пирувата в ацетил-СоА у животных необратимо, поэтому они не могут переработать жирные кислоты в глюкозу.
Механизм синтеза глюкозы из пирувата
Среди реакций гликолиза три термодинамически необратимы (см. рис. 8.7):
1) АТР-зависимое фосфорилирование глюкозы гексокиназой (или глюкокиназой);
2) фосфорилирование фруктозо-6-фосфата фосфофруктокиназой;
3) превращение фосфоенолпирувата в пируват. Глюкоза синтезируется из пирувата с образованием тех же промежуточных соединений, что и при гликолизе, но для того, чтобы обойти необратимые реакции, приходится избирать иные пути.
Первый термодинамический барьер нужно преодолеть в ходе превращения пирувата в фосфоенолпируват. Поскольку спонтанное превращение енольной формы пирувата в кетоформу сильно экзоэргонично (большая отрицательная величина ∆G°′), реакция Фосфоенолпируват —> Пируват необратима. Поэтому у животных превращение пирувата в фосфоенолпируват происходит обходным путем, в две стадии с использованием двух макроэргических фосфатов, делающих это превращение термодинамически выгодным:

Схема этих превращений представлена на рис. 11.1.
Рис. 11.1. Глюконеогенез в печени: образование фосфоенолпирувата из пирувата (ФЕП - фосфоенолпируват). Обратите внимание, что эти реакции образуют холостой цикл, если не блокировать обратное превращение ФЕП в пируват. О том, как это достигается, см. в главе 12
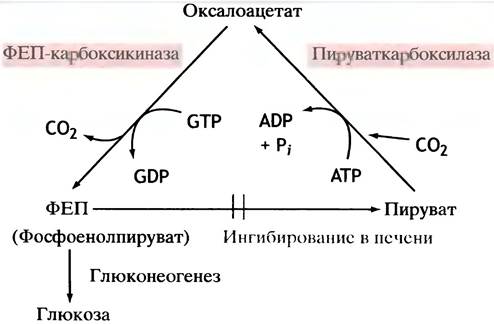
Почему на второй стадии используется GTP, а не АТР, непонятно. Энергетически оба эти вещества совершенно эквивалентны. Заметим, что реакция (1) - синтез оксалоацетата, катализируемый пируваткарбоксилазой, играет важную роль в регуляции цикла лимонной кислоты. Однако это не имеет отношения к глюконеогенезу.
Вторая реакция осуществляется фосфоенолпируват-карбоксикиназой. Такое название фермента объясняется тем, что обратную реакцию можно рассматривать как карбоксилирование фосфоенолпирувата, сопряженное с переносом фосфатной группы.
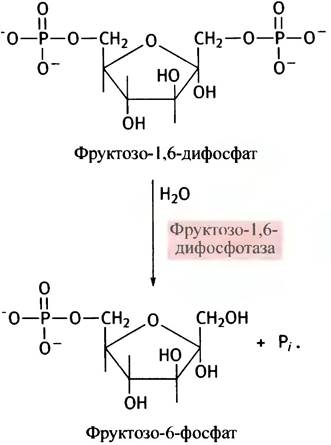
После образования фосфоенолпирувата все гликолитические реакции обратимы вплоть до реакции образования фруктозо-1,6-дифосфата, превращение которого из фруктозо-6-фосфата в ходе гликолиза необратимо. Это препятствие легко преодолевается, поскольку удаление фосфатной группы путем обычного гидролиза не требует затрат энергии.
Аналогичная реакция гидролиза в процессе глюконеогенеза имеет место при превращении глюкозо-6-фосфата в глюкозу (при гликолизе образование глюкозо-6-фосфата, катализируемое гексокиназой или глюкокиназой, необратимо).
В печени присутствует глюкозо-6-фосфатаза, которая гидролизует глюкозо-6-фосфат, после чего свободная глюкоза выходит из клетки. Совокупность реакций глюконеогенеза представлена на рис. 11.2. О том, как регулируется уровень глюкозы крови, рассказано в главе 12.
Итак, существуют четыре фермента, ответственные за глюконеогенез и не принимающие участия в гликолизе: пируваткарбоксилаза, фосфоенолпируваткарбоксикиназа, фруктозо-1,6-дифосфатаза и глюкозо-6-фосфатаза. Естественно, они сосредоточены преимущественно в печени. У крыс концентрация этих ферментов в печени в 20-50 раз больше, чем в скелетных мышцах.
Откуда печень получает пируват для глюконеогенеза?
Когда при голодании истощается запас гликогена, главным источником пирувата становится гидролитическое расщепление мышечных белков, в ходе которого образуются все 20 аминокислот. Хотя аланин - всего лишь одна из них, более 30% всех аминокислот, поступающих в печень, приходится на него. Аланин - одна из глюкогенных аминокислот; его углеводородный скелет используется печенью для строительства молекулы глюкозы (метаболизм аминокислот будет рассмотрен в главе 15).
Почему при расщеплении мышечных белков образуется так много аланина? В результате метаболизма многих аминокислот и цикла лимонной кислоты накапливается оксалоацетат, который превращается в пируват (см. рис. 11.1). Последний преобразуется в аланин; аминогруппа достается ему от других аминокислот.
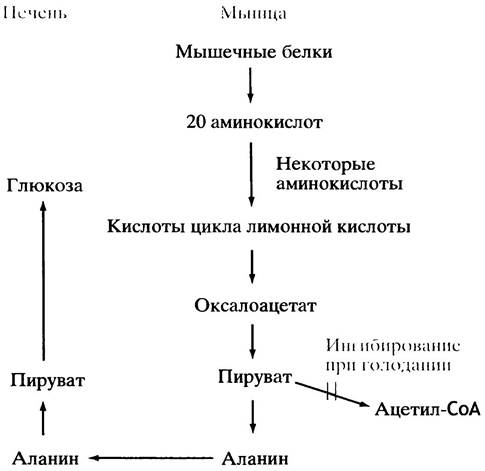
Заметим, что при голодании для производства энергии мышцы используют в основном жирные кислоты и кетоновые тела; поэтому они располагают достаточным количеством ацетил-СоА, и для его получения им не нужно окисление пирувата. Как будет показано в главе 12, высокое соотношение концентраций ацетил-СоА/ СоА приводит к инактивации пируватдегидрогеназы. Благодаря этому пируват, образующийся из аминокислот, используется для синтеза аланина. При расщеплении мышечных белков образуются различные аминокислоты, многие из которых превращаются в аланин; он переносится кровью в печень. (Кроме аланина в мышцах синтезируется и доставляется в печень для синтеза глюкозы также и глутамин; принцип его превращения тот же.) В печени аланин преобразуется снова в пируват, а затем - в глюкозу. Схема участия аланина в глюконеогенезе представлена на рис. 11.3.
Рис. 11.2. Глюконеогенез в печени: синтез глюкозы из пирувата. Реакции, отличающиеся от соответствующих гликолитических превращений, выделены цветом
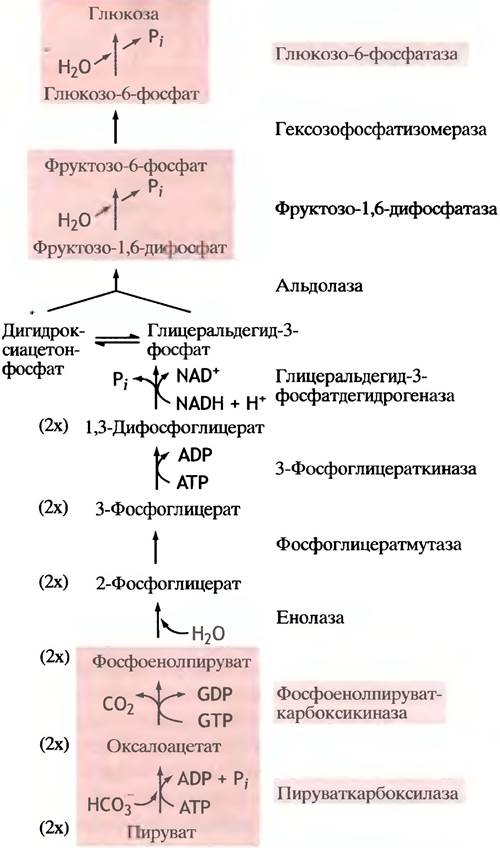
Рис. 11.3. Механизм, посредством которого при голодании мышечные белки обеспечивают печень пируватом для глюконеогенеза. Схема предполагает, что пируват не превращается в ацетил-СоА в ходе пируватдегидрогеназной реакции. Наряду с аланином из мышц поступает другой субстрат глюконеогенеза - глутамин
По мере того как при голодании в крови увеличивается содержание кетоновых тел, мозг более активно начинает использовать их вместо глюкозы для производства энергии. Это снижает (хотя и не устраняет) потребность в глюконеогенезе. Поскольку на производство 1 г глюкозы расходуется 2 г мышечных белков, замедление процесса их расщепления благотворно отражается на выживании голодающего организма.
В главе 15 подробно обсуждается схема глюкозо-аланинового цикла (см. рис. 15.9). На ней показано, как аланин, синтезированный в мышцах и доставленный в печень, перерабатывается там в глюкозу. Однако в рамках этой схемы пируват, необходимый для синтеза аланина, образуется в результате гликолиза. При этом имеет место следующая последовательность событий: глюкоза в печени —> глюкоза в мышцах —> аланин в мышцах —> аланин в печени —> глюкоза в печени.
Понятно, что такой цикл не приводит к увеличению количества глюкозы и не решает проблемы снабжения ею тканей, а является лишь формой транспорта аминного азота из мышц в печень.
Другой источник пирувата для глюконеогенеза важен не столько при голодании, сколько при нормальной жизнедеятельности организма. Речь идет о лактате, образующемся при анаэробном гликолитическом расщеплении глюкозы или гликогена (см. с. 101). Некоторые клетки, в частности мозгового вещества почек и сетчатки, фактически анаэробы, а в зрелых эритроцитах вообще нет митохондрий, и они не способны, следовательно, к окислительному фосфорилированию. При нормальном поступлении пищи главным источником лактата является гликолиз в интенсивно работающих мышцах. В таких условиях митохондрии не успевают реокислять накапливающийся NАDН. В результате восстановительные эквиваленты переносятся на пируват, который превращается в лактат. Последний переносится кровью в печень, а там перерабатывается снова в пируват, а затем в глюкозу и гликоген. Этот физиологический цикл по имени его первооткрывателя называют циклом Кори (рис. 11.4).
Рис. 11.4. Цикл Кори - физиологический цикл, который протекает в мышцах и печени. В мышцах очень невелико содержание трех ферментов, необходимых для глюконеогенеза, поэтому для переработки в глюкозу накопленный в мышцах лактат должен быть перенесен в печень. Избыток лактата образуется в мышцах при их активном сокращении в процессе анаэробного гликолиза
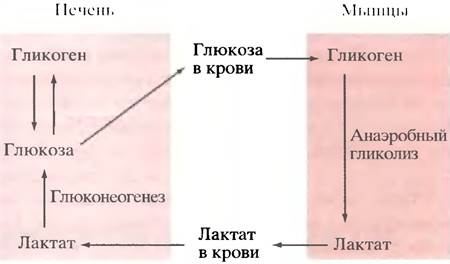
У цикла Кори есть две важнейшие функции: сберечь лактат для последующего использования и предотвратить так называемый лактат-ацидоз. При поступлении больших количеств молочной кислоты в кровь ее буферная емкость может быть исчерпана, что приведет к опасному снижению pH. Этому препятствует превращение лактата в глюкозу, которое сопровождается поглощением двух протонов (на восстановление 1,3-дифосфоглицерата расходуется 1 протон (Н+) и 1 молекула NАDН).
Синтез глюкозы из глицерина
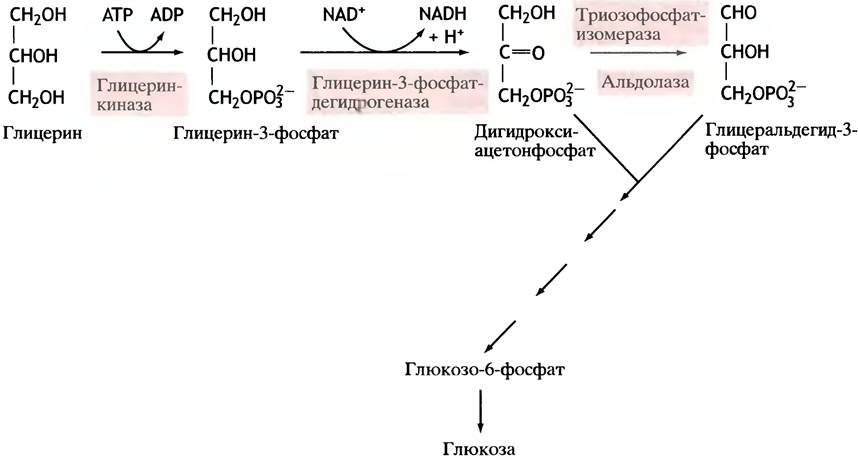
Еще одним источником углеродных соединений для глюконеогенеза служит глицерин, образующийся при гидролизе триглицеридов главным образом в жировой ткани. Он поглощается печенью и превращается там в глюкозу в соответствии со схемой, представленной на рис. 11.5. Первый этап - фосфорилирование глицерина осуществляется глицеринкиназой, которой в жировой ткани гораздо меньше, чем в печени. Все последующие превращения также сосредоточены в печени. Это вполне логично, поскольку в ситуации, когда образование глюкозы становится жизненно необходимым, эту задачу решает печень. Поэтому жировые клетки сами не используют глицерин.
Рис. 11.5. Превращение глицерина, высвобождающегося при гидролизе нейтральных жиров, в глюкозу. Основное количество глицерина образуется в жировых клетках, но поскольку в них нет глицеринкиназы, глюконеогенез из глицерина протекает в печени. Этот процесс обеспечивает образование глюкозы из глицерина при голодании
При продолжительном голодании после небольшого начального снижения уровень глюкозы в крови поддерживается неизменным в течение нескольких недель благодаря постоянному поступлению жирных кислот из жировых клеток. Удивительно, однако, что животным, в отличие от растений и бактерий, не был дарован природой более простой способ, не связанный с «поеданием» собственных мышц. Видимо, у эволюции на этот счет были какие-то неведомые нам соображения.
Синтез глюкозы посредством глиоксилатного цикла
Е. coli прекрасно существует, используя в качестве единственного источника углерода ацетат. В отличие от животных, бактерии способны превращать ацетил-СоА в С4-кислоты, задействованные в цикле лимонной кислоты, и использовать их для синтеза глюкозы и других необходимых компонентов клетки. В прорастающих семенах растений для синтеза глюкозы также используются запасенные триглицериды. Как же это удается бактериям и растениям?
Эти организмы обладают обычным циклом лимонной кислоты, но часть образующихся в нем соединений они могут использовать в других превращениях, не свойственных животным. Так, в цикле лимонной кислоты 2 углеродных атома ацетил-СоА вводятся сначала в молекулу оксалоацетата (С4) с образованием цитрата (С6), а затем 2 углеродных атома выводятся в виде 2 молекул СO2 (переход от С6- к С4-кислотам) с образованием сукцината. Этой безвозвратной потери удается избежать благодаря так называемому глиоксилатному пути, который позволяет вывести из цикла лимонной кислоты 2 атома углерода не в виде СO2, а в виде глиоксилата, который образуется непосредственно при расщеплении изоцитрата на сукцинат и глиоксилат:
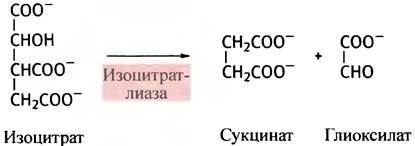
Глиоксилат (С2) далее реагирует с ацетил-СоА, превращаясь в малат - обычный компонент цикла лимонной кислоты.
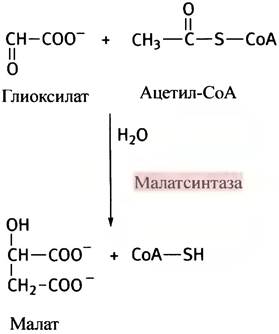
Общая схема, иллюстрирующая взаимосвязь всех рассмотренных процессов, представлена на рис. 11.6.
Рис. 11.6. Глиоксилатный цикл, с помощью которого растения и бактерии (у животных он отсутствует) осуществляют синтез углеводов из ацетил-СоА
Специфичные для этого цикла реакции выделены цветом. Штриховой линией отмечены реакции цикла лимонной кислоты, которые не задействованы в глиоксилатном цикле. Таким образом удается сохранить 2 молекулы СO2, необходимые для превращения цитрата в 2 молекулы оксалоацетата, одна из которых опять используется для синтеза цитрата, а другая превращается в фосфоенолпируват
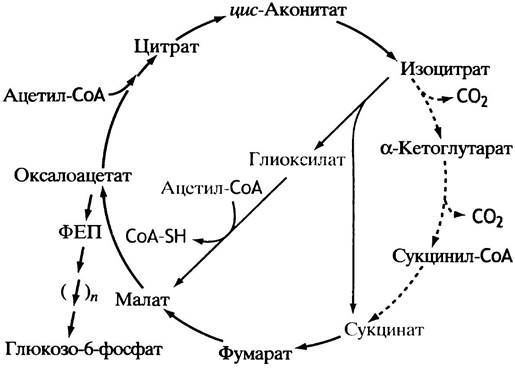
Их суммарный эффект сводится к тому, что ацетил- СоА плюс оксалоацетат превращаются в малат плюс сукцинат. И малат, и сукцинат могут быть преобразованы в оксалоацетат, одна молекула которого без ущерба для цикла может быть направлена на синтез глюкозы. В растениях эти реакции протекают в мембранах органелл, называемых глиоксисомами.
В заключение можно напомнить, что подавляющая доля углеводов на Земле образуется благодаря фотосинтезу, в ходе которого энергия солнечного света используется для фиксации СO2 в виде дифосфоглицерата - соединения, знакомого нам по гликолизу. Механизмы этого процесса и дальнейшего превращения дифосфоглицерата в глюкозу будут рассмотрены в главе 14 как составные части фотосинтеза.
Итак, мы познакомились с использованием жиров и глюкозы в качестве источников энергии, а также с механизмами синтеза этих веществ. Следует напомнить, что эти метаболические процессы не существуют изолированно, а образуют интегрированную метаболическую систему, все части которой взаимозависимы и нуждаются в регуляции.
Вопросы к главе 11
1. После суточного голодания запасы гликогена в печени истощаются, но в организме имеются довольно большие запасы жиров. Зачем при голодании протекает процесс глюконеогенеза, когда в организме есть практически безграничные запасы ацетил-СоА (из жирных кислот), которых вполне хватает для производства энергии?
2. Почему фосфоенолпируват, необходимый для протекания глюконеогенеза, не может быть получен путем фосфорилирования пирувата с помощью пируват- киназы?
3. Начиная от фосфоенолпирувата, глюконеогенез в печени осуществляется путем обращения реакций гликолиза. Какие два гликолитических фермента катализируют необратимые реакции? Как существование этих реакций сказывается на механизме глюконеогенеза?
4. Есть ли в мышцах глюкозо-6-фосфатаза? Поясните ответ.
5. Что такое цикл Кори и какова его физиологическая роль?
6. В жировых клетках практически нет глицеринкиназы - фермента, катализирующего превращение глицерина в глицерин-3-фосфат, хотя там образуется глицерин (путем гидролиза триглицеридов). В печени же этот фермент есть. Логично ли это? А если да, то почему?
7. Как бактериям и растениям, в отличие от животных, удается превратить ацетил-СоА в углеводы?