Основы биохимической инженерии Часть 1 - Бейли Дж., Оллис Д. 1989
Процессы переноса в биотехнологических системах
Теплообмен
В биологических реакторах необходимость в отводе теплоты или в обогреве культуральной жидкости может возникнуть по следующим причинам.
1. Подаваемый в реактор питательный раствор желательно стерилизовать нагреванием в проточном стерилизаторе или в стерилизаторе периодического действия. Температура стерилизации должна обеспечивать за общее время пребывания гибель практически всех микроорганизмов (разд. 9.9.4).
2. Если количество выделяющейся в процессе переработки субстрата теплоты недостаточно для поддержания температуры на заданном уровне, то реактор необходимо обогревать. Такая ситуация типична, например, для процессов переработки отходов в анаэробных условиях, оптимальная температура для которых составляет 55—60 °С (разд. 14.4.7).
8. При превращении субстрата выделяется избыточное (по отношению к оптимальным условиям, обеспечивающим, например, жизнеспособность живых клеток) количество теплоты, которое необходимо отводить. Такая ситуация характерна для большинства процессов с участием микроорганизмов.
4. Необходимость в дополнительном нагревании возникает также в процессах сушки суспензий клеток.
Здесь мы рассмотрим первые три случая, связанные с жизнеспособностью организмов. Что касается сушки, то этот физический процесс детально обсуждается в большинстве книг по химической технологии.
Теплообмен между культуральной жидкостью и другой средой конструктивно осуществляется несколькими путями, в том числе с помощью внешних рубашек, помещаемых в культуральную жидкость трубчатых спиральных теплообменников (змеевиков), циркуляции реакционной смеси через теплообменные аппараты, а также посредством упаривания или конденсации воды и других летучих компонентов жидкой фазы, содержащей клетки. Примеры способов теплообмена представлены на рис. 8.16. Теплообмен, очевидно, играет определенную роль и в поддержании разницы температур между термически стратифицированными естественными водоемами и почвой; установившиеся зоны с определенными диапазонами температур определяют соответствующие биологические ниши для совокупностей видов живых организмов. В настоящем разделе основное внимание мы будем уделять теплообмену в биологических реакторах.
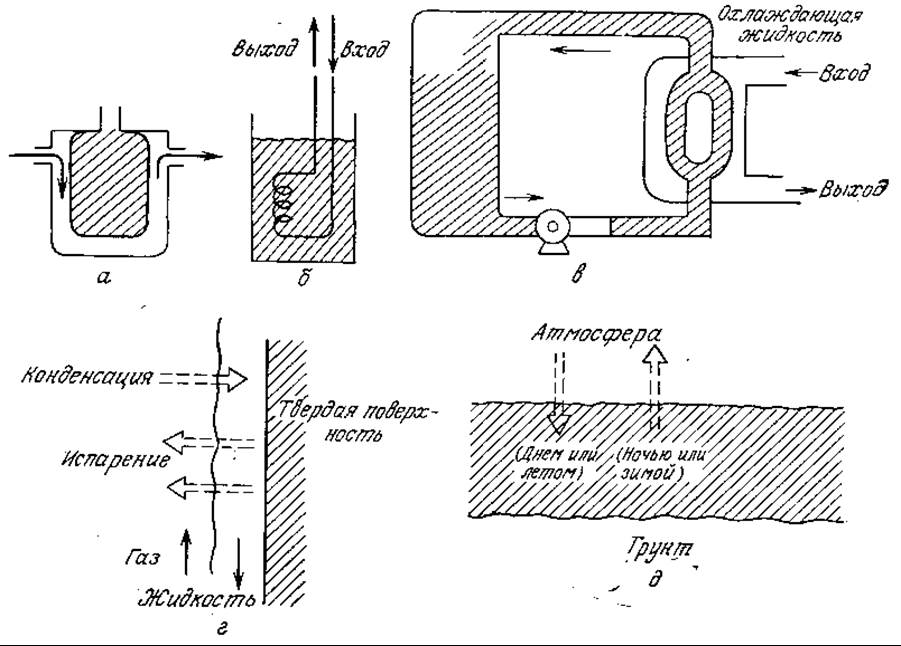
РИС. 8.16. Примеры теплообменных аппаратов и естественных процессов теплообмена: а — реактор с рубашкой; б — реактор с внутренним змеевиком; в — циркуляция реакционной массы через теплообменный аппарат; г — фазовые переходы; д — естественные температурные колебания.
Если принять, что скорости передачи и изменения других форм энергии пренебрежимо малы, то основное уравнение теплообмена в стационарном состоянии будет отражать связь между скоростью отвода (с помощью какого-либо теплообменного аппарата) и скоростью выделения теплоты. Следовательно,
![]()
Здесь ∆Т — характерная разность температур между содержимым реактора и охлаждающей или нагревающей жидкостью; А — площадь поверхности теплообмена; h — общий коэффициент теплообмена.
Как и в случае массообмена, наибольшее сопротивление теплопередаче оказывает относительно неподвижный тонкий слой жидкости вблизи твердой стенки, разделяющей нагреваемую и нагревающую жидкие среды, поскольку жидкая фаза обычно эффективно перемешивается и, следовательно, ее можно считать приближенно изотермичной. В этом разделе нас будут интересовать прежде всего вывод уравнений общего энергетического баланса и обзор математических выражений, определяющих h для различных систем нагревания, охлаждения и стерилизации, которые представляют интерес в микробиологических процессах. Методы оценки тепловой нагрузки, сопровождающей рост микроорганизмов, мы уже рассмотрели в гл. 5.
Таблица 8.6. Примерные величины коэффициентов теплопередачи hа
h, ккал/(м2⋅ч⋅град) |
|
|
Естественная конвекция |
|
Газы |
3—20 |
Жидкости |
100—600 |
Кипящая вода |
1000—20 000 |
|
Принудительная конвекция |
|
Газы |
10—100 |
Вязкие жидкости |
50—500 |
Вода |
500—10 000 |
Конденсирующиеся пары |
1000—100 000 |
а Из работы: Gröber Н., Erk S., Grigull U., Wärmeübertragung, 3d ed., p. 158, Springer-Verlag, Berlin, 1955.
Высокие коэффициенты теплопередачи (табл. 8.6) кипящей воды и конденсирующихся паров (обычно водяного пара) делают эти теплоносители особенно удобными в процессах стерилизации (разд. 9.9.4). Если необходимы более низкие температуры (например, в обогреваемых аппаратах для анаэробной переработки), то в таких случаях удобнее применять воду с температурой ниже 100 °С. Для вязких жидкостей характерно более высокое (по сравнению с водой) сопротивление теплопередаче; как и в случае массообмена, это связано с пониженной скоростью обмена между жидкой фазой и пленкой вблизи стенки, а также с пониженной теплопроводностью вязких жидкостей (аналогично малому коэффициенту диффузии О2).
Изучение изображенных на рис. 8.16 принципов теплообмена указывает на ряд проблем теплопередачи в биохимических реакторах. В системах с наружной охлаждающей или обогревающей рубашкой площадь теплопередающей поверхности А пропорциональна квадрату диаметра реактора (или диаметра лопастной мешалки) Di2. В то же время если мы хотим, чтобы скорость микробиологических процессов и потребление мощности на единицу объема оставались постоянными, то степень нагрева или охлаждения реактора должна быть пропорциональной Di3. Поэтому сосуды с рубашкой, обеспечивающие изотермические условия в лабораторных экспериментах, при резком повышении объемов реакторов часто приходится заменять на реакторы с внутренними или внешними обогревающими (например, при анаэробной переработке) или охлаждающими (в частности, при переработке углеводородов в белок одноклеточных организмов) змеевиками.
Понятно, что наличие системы внутренних трубопроводов изменяет картину перемешивания, структуру скоростей течения жидкости и, возможно, скоростей коалесценции пузырьков газа. Сложность такой ситуации еще раз напоминает нам о необходимости экспериментального определения параметров только в реакторах, конструкции которых в максимальной степени соответствуют конструкции реактора, в котором будет осуществляться крупномасштабный процесс; в процессах с участием микроорганизмов априорное проектирование реакторов приведет к еще более неопределенным результатам, чем в случае более простых систем. (Проблемы перемешивания в реакторах рассматриваются в тексте и в упражнениях гл. 9.) В частности, приведенные в разд. 8.10.1 уравнения показывают, что коэффициент теплопередачи h [выраженный в ккал/(м2⋅ч)] изменяется при переходе от одной охлаждающей спирали, перпендикулярной течению жидкости, к устройству из нескольких расположенных в шахматном порядке рядов спиралей, также перпендикулярному течению жидкости. Следовательно, первый ряд труб изменяет характер потока, омывающего последующие ряды труб.
В случае очень больших реакторов с большой тепловой нагрузкой (например, при росте бактерий на метаноле в реакторе объемом 1500 м3) внутренние змеевики уже не могут обеспечить необходимый отвод теплоты. В таких случаях приходится прибегать к циркуляции через внешний теплообменник или через теплообменник, являющийся составной частью реактора петлеобразной конструкции. Этот пример показывает, что иногда высокие тепловые нагрузки вкупе с другими факторами (например, высоким расходом мощности на аэрацию и перемешивание) обусловливают необходимость разработки биореакторов особых конструкций, резко отличающихся от обычных резервуаров с перемешиванием. Различные конструкции реакторов, способы смешения и принципы перемешивания вкратце будут рассмотрены в гл. 9.
Известно, что скорости выделения и отвода теплоты позволяют с достаточной точностью оценить тепловой баланс системы при условии, что мы четко понимаем физическую основу соответствующих расчетов и учитываем обеспечиваемую этими расчетами степень достоверности результатов. В этом разделе мы обсудим пути оценки потребности биотехнологических систем в теплообмене (аналогичной потребности в кислороде); следующий раздел будет посвящен проблеме определения коэффициента теплопередачи h.
Определение потребности системы в нагревании или охлаждении начинается с анализа общего энергетического баланса. При постоянном давлении в системе с незначительными изменениями потенциальной и кинетической энергии энергетический баланс можно рассчитать через изменения энтальпии, в том числе теплоты химических превращений, фазовых переходов (испарения, конденсации), тепловых потоков, сопровождающих процессы массообмена, теплопередачи от второй жидкости, используемой для охлаждения или нагревания. Введем следующие обозначения:
Qmet — скорость выделения теплоты в процессах роста и поддержания жизнедеятельности клеток;
Qag — скорость выделения теплоты за счет механического перемешивания реакционной массы;
Qgas — скорость выделения теплоты в результате аэрации;
Qасе — скорость накопления теплоты;
Qexch — скорость теплопередачи в окружение реактора или к теплоносителю теплообменного аппарата;
Qevap — скорость потери теплоты за счет испарения;
Qsen —скорость приращения энтальпии за счет разности теплосодержания потоков на входе в реактор и на выходе из него.
Тогда
Qmet + Qag + Qgas = Qacc + Qexch + Qevap + Qsen (8.119)
Куни, Ванг и Мателес [52] применяли это уравнение для расчета Qmet на основе экспериментального определения Qacc путем контроля изменения температуры в практически изолированном реакторе. В таких условиях величины Qevap и Qsen очень малы, a Qexch вносит большой вклад по сравнению с разностью Qacc — Qag, хотя последние параметры сами по себе выше Qexch. Как мы только что отмечали, Qąceконтролировали калориметрически, a Qag вычисляли для каждого значения скорости потока газа и скорости вращения мешалки по уравнению Мичела и Миллера [уравнение (8.81)].
При расчете стационарного режима работы реактора Qaсc принимается равным нулю, хотя при программированном изменении температуры, необходимом для достижения оптимального выхода в периодическом процессе (разд. 10.7), здесь могут возникнуть дополнительные осложнения. Параметр Qag для аэрируемых или неаэрируемых систем определяется с помощью рассмотренных ранее уравнений для расчета потребляемой реактором мощности.
Если мы пренебрегаем Qevap (хотя этот параметр может быть существенным в реакторах со струйным течением), а также пока не учитываем Qsen, то единственным важным параметром остается Qmet. Методы оценки и определения величины Qmet были рассмотрены в гл. 5. При расчете реакторов большого объема заданные рабочая температура и параметры течения определяют Qevap и Qsen, а скорость вращения мешалки и ее диаметр определяют Qag (скорректированный с учетом выбранной скорости аэрации). Конструкция барботера и скорость потока газа определяют Qgas. Что касается оставшихся параметров Qacc и Qexch, то независимо от того, находится ли реактор в изотермических условиях или нет, в каждый момент

Последнее уравнение устанавливает величину теплопередачи, необходимую для поддержания заданной температуры или определенной скорости накопления теплоты (если оно вообще необходимо).
Мы можем использовать уравнение (7.35а), описывающее мгновенную скорость образования клеточной массы в единице объема реактора периодического действия:
![]()
Соответствующая мгновенная скорость выделения теплоты в микробиологическом процессе Qmet (теплота/время), очевидно, будет определяться уравнением
![]()
Здесь Y∆ — коэффициент (г клеток/ккал), рассмотренный в разд. 5.10.4. Там же были представлены методы определения Y∆, а также иллюстративный материал, свидетельствующий об увеличении выделения метаболической теплоты при утилизации более восстановленных субстратов (табл. 5.12).
Соответствующее уравнение для изотермического стационарного процесса в проточном реакторе выглядит следующим образом:
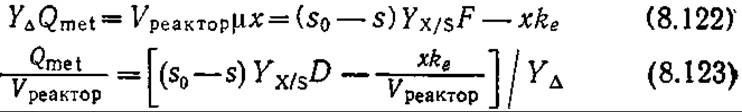
Как мы упоминали выше, Yх/s может зависеть от возраста культуры в периодическом процессе и скорости разведения D в проточной системе. Зависимость Yх/s (а следовательно, и Y∆) от затрат на поддержание клеточного метаболизма отражена в уравнении (7.26).
Таблица 8.7. Зависимость расходов на производство белка одноклеточных организмов от природы субстратаa
Субстрат |
Расходы в центах на производство 1 фунта (450 г) клеток, |
|||
Субстрат |
Перенос O2 |
Охлаждение |
Всего |
|
Малеат (отходы) |
0 |
0,46 |
0,75 |
1,2 |
Эквиваленты глюкозы (меласса) |
3,9 |
0,23 |
0,54 |
4,7 |
Парафины |
4,0 |
0,97 |
1,4 |
6,4 |
Метанол |
5,0 |
1,2 |
1,9 |
8,Г |
Метан |
1,6 |
3,3 |
3,7 |
8,6 |
Этанол |
8,8 |
0,75 |
1,3 |
11,0 |
Изопропанол |
11,6 |
2,7 |
3,1 |
17,4 |
Ацетат |
16,7 |
0,62 |
1,1 |
18,4 |
а Abbott В. Clamen A., The Relationship of Substrate, Growth Rate, and Maintenance Coefficient to Single Cell Protein Production, Biotech. Bioeng., 15, 117 (1973).
Выполненные в 1973 г. Абботтом и Кламеном экономические расчеты показывают, что при производстве биомассы бактерий расходы как на теплообмен, так и на массообмен (перенос кислорода) составляют значительную часть общей стоимости продукции (табл. 8.7) [43].