ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 1. ОСНОВЫ БИОХИМИИ СТРОЕНИЕ И КАТАЛИЗ - 2011
ЧАСТЬ I. СТРОЕНИЕ И КАТАЛИЗ
10. ЛИПИДЫ
10.2. Структурные липиды в мембранах
Биологические мембраны состоят из двойного слоя липидов, который служит барьером для проникновения полярных молекул и ионов. Мембранные липиды проявляют амфифильные свойства: один конец их молекулы гидрофобный, другой — гидрофильный. Благодаря гидрофильным взаимодействиям с водой их агрегаты из молекул образуют упаковку в виде пластов, называемых мембранными бислоями. В этом разделе мы опишем пять главных типов мембранных липидов: глицерофосфолипиды, в которых гидрофобные области представлены остатками двух жирных кислот, связанными с глицерином; галактолипиды и сульфолипиды содержат также две жирные кислоты, этерифицированные глицерином, но здесь, в отличие от фосфолипидов, отсутствует фосфат; тетраэфирные липиды архей, в которых две очень длинные алкильные цепи связаны простой эфирной связью с глицерином обоими концами; сфинголипиды, в которых одна жирная кислота связана с жирным амином сфингозином; и стерины, соединения с жесткой системой из четырех конденсированных углеводородных колец.
Гидрофильные области в этих амфифильных соединениях могут быть представлены простыми функциональными группами, как, например, на одном конце кольцевой системы стерина всего одна группа -ОН, но гидрофильные свойства могут быть обусловлены и гораздо более сложной структурой. В глицерофосфолипидах и некоторых сфинголипидах полярная группа «головки» присоединяется к гидрофобной части фосфодиэфирной связью; это фосфолипиды. Другие сфинголипиды не содержат фосфата, но несут на своих полярных концах простой сахар или сложный олигосахарид; это гликолипиды (рис. 10-7). Мембранные липиды чрезвычайно разнообразны, что обусловлено различными комбинациями жирнокислотных «хвостов» и полярных «головок». Расположение фосфолипидов в мембранах и структурная и функциональная роль, которую они там играют, будут рассмотрены в следующей главе.
Рис. 10-7. Некоторые широко распространенные типы запасных и мембранных липидов. Все изображенные здесь липиды имеют в своем составе либо глицерин, либо сфингозин в качестве основы (скелета) (розовые полоски), с которыми связаны одна или более длинноцепочечных алкильных групп (желтые) и полярные «головки» (голубые). В триацилглицеридах, глицерофосфолипидах, галактолипидах и сульфолипидах алкильные цепи появляются от остатков жирных кислот, образующих сложноэфирную связь. Сфинголипиды содержат одну- единственную жирную кислоту, образующую амидную связь со сфингозиновым скелетом. Мембранные липиды архей содержат очень длинные разветвленные алкильные цепи, каждый конец которых образует простую эфирную связь с глицериновой частью. В фосфолипидах полярная «головка» присоединяется через фосфодиэфирную связь, в то время как в гликолипидах гликозидная связь напрямую соединяет сахар «головки» и глицерин.
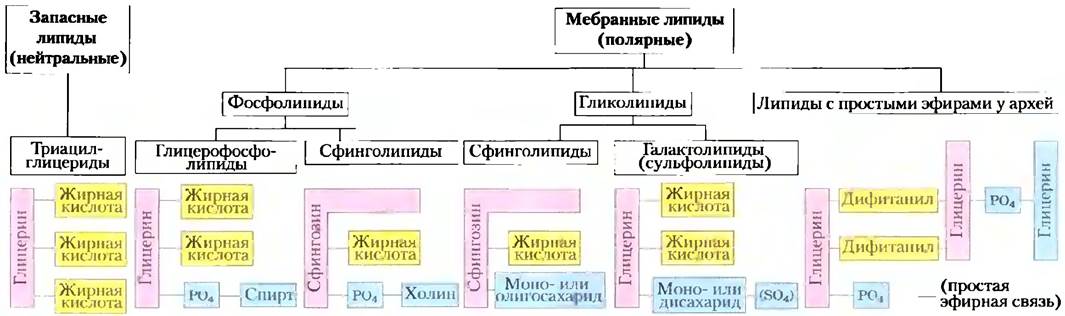
Глицерофосфолипиды — производные фосфатидной кислоты
Глицерофосфолипиды, называемые также фосфоглицеридами, — это мембранные липиды, у которых остатки двух жирных кислот связаны сложноэфирной связью с первым и вторым углеродными атомами глицерина, а к третьему углероду фосфодиэфирной связью присоединена сильно полярная или заряженная группа. Глицерин — прохиральная структура; в нем нет асимметрических атомов углерода, но присутствие связанного фосфата на одном конце превращает его в хиральное соединение, которое правильно называется L-глицеро-3-фосфат-D-глицеро-1 -фосфатом либо sn-глицеро-3-фосфатом (рис. 10-8). Глицерофосфолипиды получают названия как производные исходного соединения — фосфатидной кислоты (рис. 10-9) — в зависимости от типа полярного спирта в «головке».
Рис. 10-8. L-глицеро- 3-фосфат, основа фосфолипидов. Сам по себе глицерин не хиральная молекула, поскольку имеет плоскость симметрии, которая проходит через С-2. Однако глицерин можно превратить в хиральное соединение, введя заместитель, такой как фосфат, к любой из груш -СН2OН, т. е. глицерин прохирален. Для глицерофосфатов используется DL-номенклатура (см. с. 117), где изомеры называют согласно их стереохимическому родству с изомерами глицеральдегида. В этой номенклатуре стереоизомер глицерофосфата, найденный в большинстве липидов, правильно называть L-глицеро-3-фосфат или D-глицеро-1-фосфат. В другой номенклатуре стереоизомеров используют стереоспецифическую нумерацию (sn-система), и, по определению, С-1 — та группа прохирального соединения, которая занимает про-5-положение. В этой номенклатуре глицерофосфат в фосфолипидах называется sn-глицеро-3-фосфат.
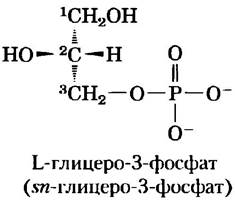
Рис. 10-9. Глицерофосфолипиды. Из глицерофосфолипидов наиболее распространены диацилглицериды, в которых остатки спиртов «головки» связаны фосфодиэфирной связью. Фосфатидная кислота, фосфомоноэфир, служит исходным соединением. Каждое производное называется по спиртовой группе «головки» (X), с приставкой «фосфатидил-». В кардиолипине две молекулы фосфатидной кислоты делят один глицерин. R1 и R2 — остатки жирных кислот.
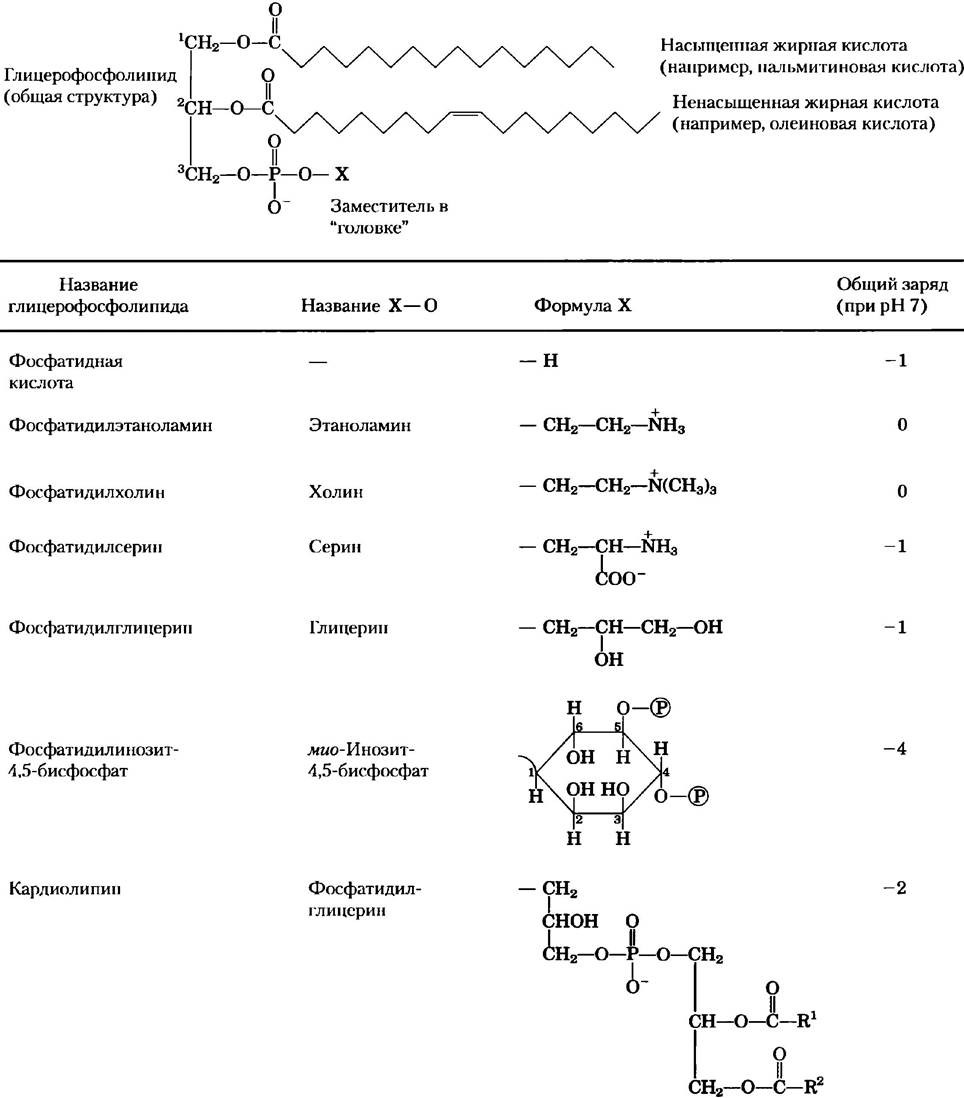
Например, фосфатидилхолин и фосфатидил- этаноламин содержат в своих полярных «головках» холин и этаноламин. Во всех этих соединениях группа «головки» соединена с глицерином фосфодиэфирной связью, в которой фосфатная группа несет отрицательный заряд при нейтральных pH. Полярный спирт может быть заряженным отрицательно (как в фосфатидилинозит-4,5- бисфосфате), нейтральным (фосфатидилсерин) или заряженным положительно (фосфатидилхолин, фосфатидилэтаноламин). Как мы увидим в гл. 11, эти заряды вносят очень существенный вклад в поверхностные свойства мембран.
В состав глииерофосфолипидов могут входить любые природные жирные кислоты. Например, фосфолипид фосфатидилхолин может иметь разный состав, каждый содержит свой уникальный набор жирных кислот. Распределение разных видов молекул специфично для различных организмов, разных тканей одного и того же организма и различных глицерофосфолипидов в одной и той же клетке или ткани. Как правило, глицерофосфолипиды содержат С16- или С18-насыщснную жирную кислоту при С-1 и С18-С20-ненасыщенную жирную кислоту при С-2. За редким исключением, биологическая роль вариаций жирных кислот и групп «головки» пока остается неясной.
Некоторые фосфолипиды содержат жирные кислоты, связанные простой эфирной связью
Некоторые ткани животных и одноклеточные организмы богаты липидами, в которых одна из двух ацильных цепей образует с глицерином простую эфирную, а не сложноэфирную связь. Связанная простой эфирной связью цепь может быть насыщенной, как в алкилэфирных липидах, или может содержать двойную связь между С-1 и С-2, как в плазмалогенах (рис. 10-10). Сердечная ткань позвоночных уникально богата липидами с простой эфирной связью; около половины сердечных липидов составляют плазмалогены. В мембранах галофильных бактерий, инфузорий и некоторых беспозвоночных также высоко содержание липидов с простой эфирной связью. Функциональная роль липидов с простой эфирной связью в этих мембранах неизвестна; возможно, их устойчивость к фосфолипазам, отщепляющим от мембранных липидов жирные кислоты, связанные сложноэфирной связью, важна для некоторых функций.
Рис. 10-10. Липиды с простой эфирной связью. Плазмалогены содержат связанную простой эфирной связью алкенильную цепь в том месте, где у большинства глицерофосфолипидов находится связанная сложноэфирной связью жирная кислота (сравните с рис. 10-9). Фактор активации тромбоцитов несет связанную простой эфирной связью длинную алкильную цепь при атоме С-1 глицерина, но в положении С-2 находится связанный сложноэфирной связью остаток уксусной кислоты, что делает это соединение гораздо более растворимым в воде, чем большинство глицерофосфолипидов и плазмалогенов. Спиртом «головки» и в плазмалогенах, и в факторе активации тромбоцитов является холин.
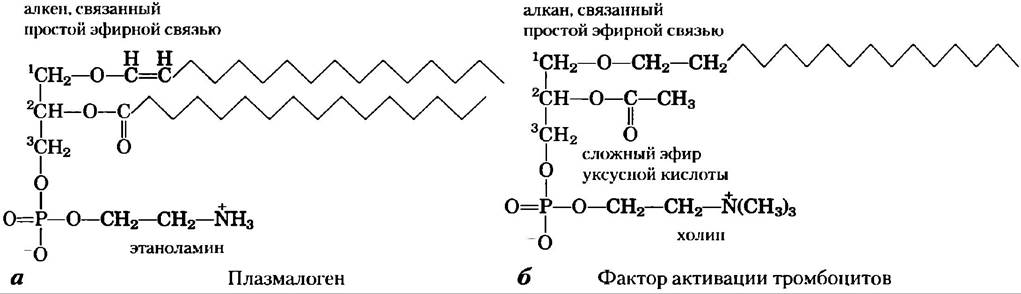
■ По крайней мере, один липид с простой эфирной связью, фактор активации тромбоцитов, потенциально является сигнальной молекулой. Он высвобождается из лейкоцитов, называемых базофилами, и стимулирует агрегацию тромбоцитов и высвобождение серотонина (вазоконстриктора сосудосуживающего агента). Он также оказывает разнообразные эффекты на печень, гладкую мускулатуру, сердце, ткани матки и легких и играет важную роль при воспалительных и аллергических реакциях. ■
Хлоропласты содержат галактолипиды и сульфолипиды
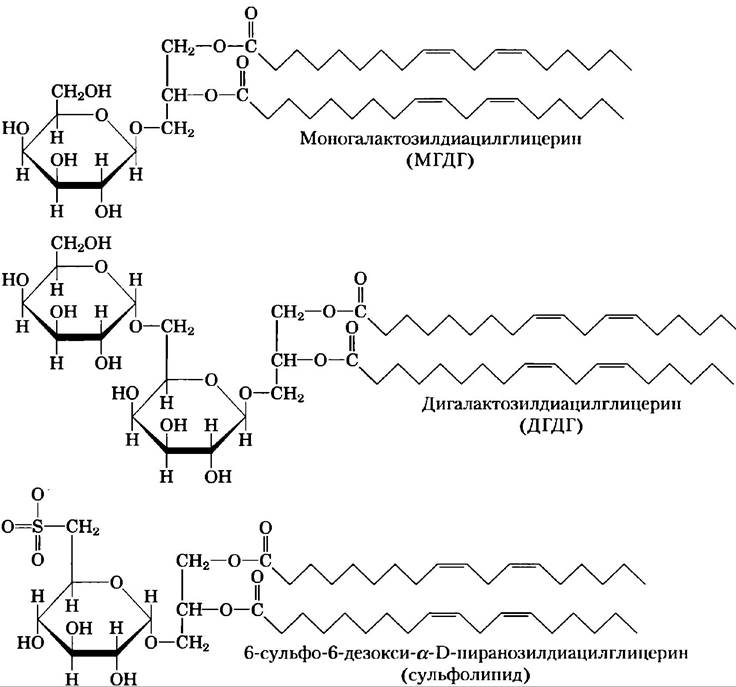
Вторую группу мембранных липидов составляют галактолипиды — липиды, преобладающие в растительных клетках; в них один или два остатка галактозы связаны с атомом С-3 1,2-диацил- глицерина гликозидной связью (рис. 10-11, см. также рис. 10-7). Галактолипиды локализованы в тилакоидных мембранах (внутренние мембраны) хлоропластов; на их долю приходится 70-80% всех мембранных липидов сосудистых растений. По всей вероятности, это самые распространенные в биосфере липиды. Часто количество фосфата как питательного компонента почвы ограничено, и, возможно, эволюционные воздействия, направленные на сохранение фосфата для более важных целей, способствовали тому, что растения создали липиды, не содержащие фосфат. В мембранах растений встречаются также сульфолипиды, в которых сульфонированный остаток глюкозы присоединяется к диацилглицерину гликозидной связью. В сульфолипидах сульфонат «головки» несет фиксированный отрицательный заряд подобно фосфатной группе в фосфолипидах (рис. 10.11).
Рис. 10-11. Три гликолипида мембран тилакоидов хлоропластов. В моногалактозилдиацилглицеридах (МГДГ) и дигалактозилдиацилглицеридах (ДГДГ) почти все ацильные группы происходят из линолевой кислоты (18:2(∆9,12)), и группы «головки» не заряжены. В сульфо- липиде 6-сульфо-6-дезокси-α-D-глюкопиранозилдиацилглицериде сульфонат несет фиксированный отрицательный заряд.
Археи содержат уникальные мембранные липиды
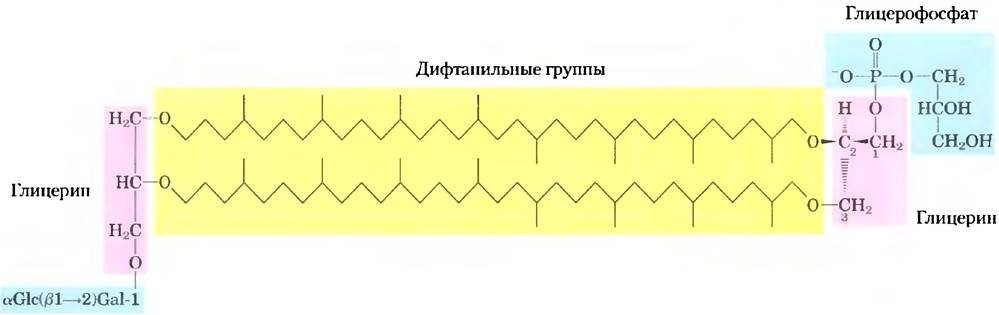
У архей, большинство которых существуют в экологических нишах с экстремальными условиями, например при высокой температуре (кипящей воды), низком pH, высокой ионной силе, мембранные липиды содержат длинноцепочечные (32 атома углерода) разветвленные углеводороды, каждым концом соединенные с глицерином (рис. 10-12). Простые эфирные связи этих соединений гораздо устойчивее к гидролизу при низких pH и высокой температуре, чем сложноэфирные связи, найденные в липидах бактерий и эукариот. В полностью вытянутой форме липиды архей в два раза длиннее, чем фосфолипиды и сфинголипиды, и простираются на всю ширину наружной мембраны. На каждом конце этой протяженной молекулы находится полярная «головка», состоящая из глицерина, связанного с остатками либо фосфата, либо сахара. Общее название этих соединений глицеринди- алкилглицеринтетраэфиры (ГДГТ), отражает их уникальную структуру. Глицериновая часть липидов архей не тот же стереоизомер, что в липидах бактерий и эукариот; центральный углерод находится в R-конфигурации у архей, а в других «царствах» — в R-конфигурации (рис. 10-8).
Рис. 10-12. Типичный липид мембраны архей. В этом дифитанилтетраэфирном липиде дифитанильные участки (желтые) — это длинные углеводороды, составленные из восьми пятиуглеродных изопреновых групп, сконденсированных конец к концу (о конденсации изопреновых единиц см. рис 21-36; ср. также дифтаниловые группы с 20-углеродной фитиновой боковой цепью хлорофилла на рис. 19-47, а). В данной протяженной форме дифитанильные группы примерно вдвое длиннее, чем 16-углеродная жирная кислота, обнаруживаемая обычно в мембранных липидах бактерий и эукариот. Глицериновые участки в липидах архей находятся в R-конфигурации, в противоположность липидам бактерий и эукариот, где они имеют S-конфигурацию. Липиды архей отличаются и заместителями в глицериновой части. В молекуле, которая здесь изображена, один глицерин связан с дисахарид-α-глюкопиранозил- (1 —> 2)-β-галактофуранозой; другой глицерин соединен с глицерофосфатной «головкой».
Сфинголипиды — производные сфингозина
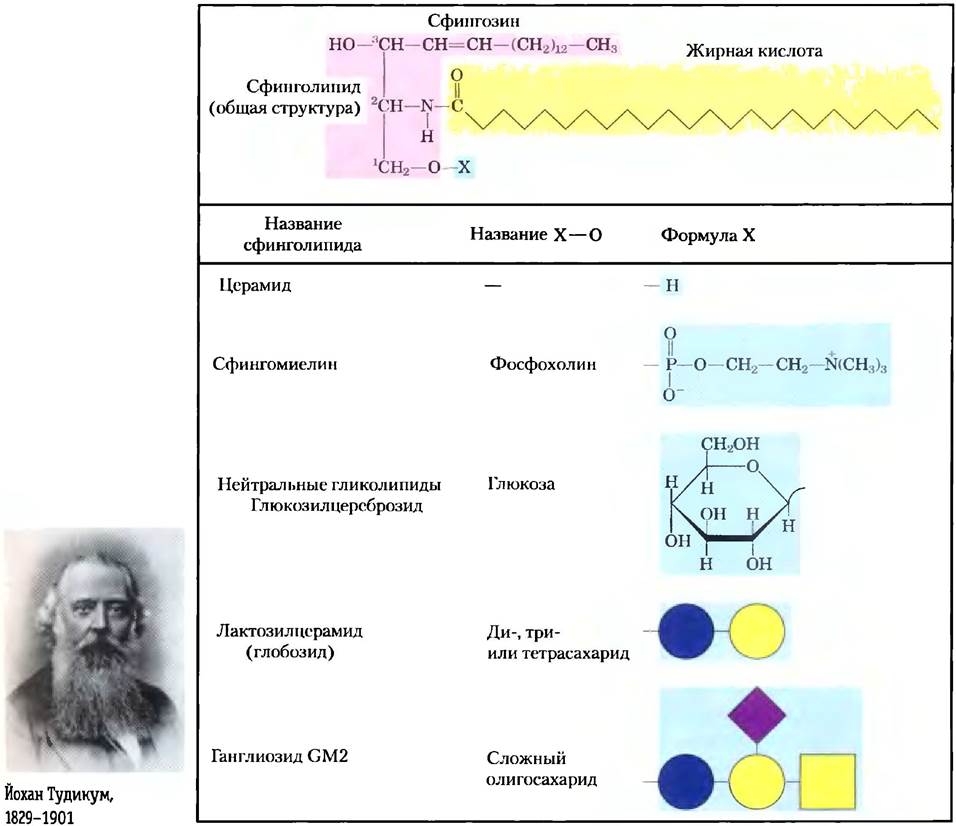
Сфинголипиды — четвертый большой класс мембранных липидов — также состоят из полярной «головки» и двух неполярных «хвостов», но, в отличие от глицерофосфолипидов и галакто- липидов, они не содержат глицерина. Сфинго- липиды несут одну молекулу длинноцепочечного аминоспирта сфингозина (4-сфингснина) или одного из его производных, одну молекулу длинноцепочечной жирной кислоты и полярную «головку», которая в одних случаях соединена гликозидной связью, в других — фосфодиэфирной (рис. 10-13).
Рис. 10-13. Сфинголипиды. Первые три углерода на полярном конце сфингозина аналогичны трем углеродам глицерина в глицерофосфолипидах. Аминогруппа при С-2 образует амидную связь с жирной кислотой. Эта жирная кислота обычно насыщенная или мононенасыщенная, с 16,18, 22 или 24 углеродными атомами. Церамид — простейшее соединение данной группы. Другие сфинголипиды отличаются по полярной группе «головки» (X), связанной с С-1. Ганглиозиды имеют очень сложные олигосахаридные «головки». Здесь используются стандартные сокращения для сахаров (см. табл. 7-1).
Углероды С-1, С-2 и С-3 в сфингозине аналогичны трем углеродам глицерина в глицерофосфолипидах. Когда жирная кислота присоединяется амидной связью к -NН2 при С-2, получается церамид, который структурно схож с диацилглицерином. Церамид — это структурный «прародитель» сфинголипидов.
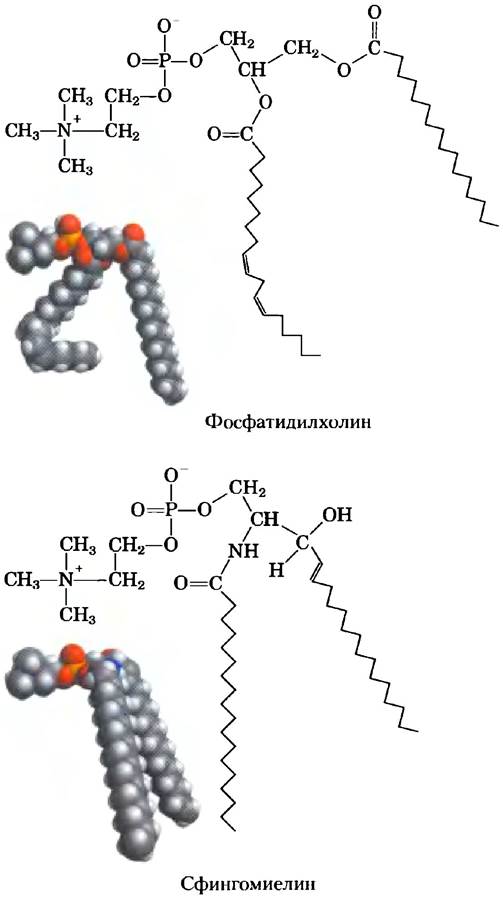
Существуют три подкласса сфинголипидов, все они производные церамида, но имеют различия в полярных «головках»: сфингомиелины, нейтральные (незаряженные) гликолипиды и ганглиозиды. Сфингомиелины содержат фосфохолин или фосфоэтаноламин в качестве полярных групп «головки» и поэтому относятся наряду с глицерофосфолипидами к фосфолипидам (рис. 10-7). Действительно, по свойствам и трехмерной структуре сфингомиелины напоминают фосфатидилхолины, их полярные «головки» также не несут заряда (рис. 10-14). Сфингомиелины присутствуют в плазматических мембранах животных клеток, особенно важное место они занимают в миелине — мембранной оболочке, которая окружает и изолирует аксоны некоторых нейронов; отсюда и название «сфингомиелины».
Рис. 10-14. Сходство формы и молекулярной структуры фосфатидилхолина (глицерофосфолипид) и сфингомиелина (сфинголипид) хорошо видно при сравнении их структурных формул и пространственных моделей.
Гликосфинголипиды, которые находятся, главным образом, на внешней поверхности плазматических мембран, содержат группы «головки» из одного или более сахаров, связанных непосредственно с ОН-группой углерода С-1 церамидной части; в них нет фосфата. Цереброзиды несут единственный сахар, связанный с церамидом; обнаружено, что цереброзиды с галактозой характерны для плазматических мембран клеток нервной ткани, а цереброзиды, содержащие глюкозу, находятся в плазматических мембранах клеток других тканей. Глобозиды — нейтральные (незаряженные) гликосфинголипиды с двумя или более сахарами, которые обычно представлены D-глюкозой, D-галактозой или N-ацетил-D-галактозамином. Цереброзиды и глобозиды иногда называют нейтральными гликолипидами, поскольку при pH 7 они не имеют заряда.
Ганглиозиды, самые сложные сфинголипиды, в качестве полярных «головок» содержат на концах олигосахариды и один или более остатков N-ацетилнсйраминовой кислоты (Nеu5Ас), (часто ее называют просто сиаловой кислотой). Сиаловая кислота придает ганглиозидам отрицательный заряд при pH 7, и это отличает их от глобозидов. Ганглиозиды с одним остатком сиаловой кислоты входят в серию GМ (М от моно-), с двумя остатками — в серию GD (D от ди-) и так далее (GТ означает три остатка сиаловой кислоты, GQ — четыре).
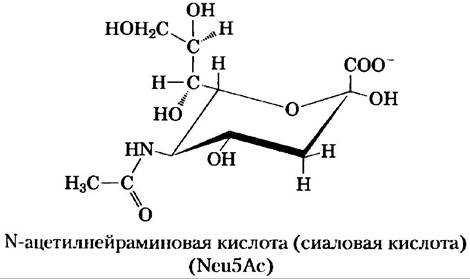
Сфинголипиды на поверхностях клеток — участки биологического распознавания
Когда более 100 лет назад врач и химик Йохан Тудикум открыл сфинголипиды, их биологическая роль казалась загадочной, как сфинкс (отсюда и название). В клеточных мембранах человека выявлено по крайней мере 60 различных сфинголипидов. Многими из них особенно богаты плазматические мембраны нейронов, некоторые, несомненно, служат распознающими участками на клеточной поверхности, но до сих пор только для нескольких сфинголипидов открыта их специфическая функция. Углеводные части некоторых сфинголипидов характеризуют группы крови людей и, таким образом, определяют тип крови, которую человек может безопасно получать при переливаниях (рис. 10-15).
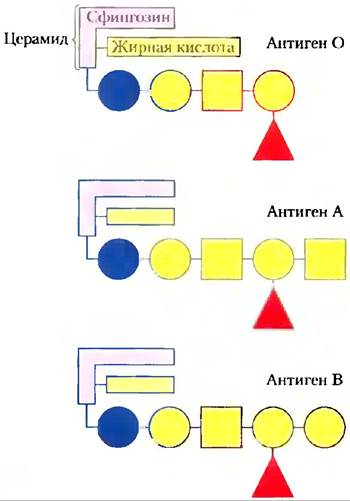
Рис. 10-15. Гликосфинголипиды как факторы, определяющие группу крови. Группы крови человека (O, А, В) отчасти определяются олигосахаридными «головками» (показаны голубым) этих гликосфинголипидов. Обнаружено также, что три определенных олигосахарида связаны с некоторыми белками крови людей с типами крови O, А и В соответственно. Здесь использованы стандартные обозначения сахаров (см. табл. 7-1).
Ганглиозиды сконцентрированы на внешней поверхности клеток и представляют собой точки узнавания для внеклеточных молекул или поверхностей соседних клеток. Виды и количество ганглиозидов в плазматической мембране разительно изменяются в процессе эмбрионального развития. Образование опухоли индуцирует синтез нового комплемента ганглиозидов, и было установлено, что очень низкие концентрации специфического ганглиозида индуцируют дифференцировку в культуре опухолевых клеток нервной ткани. Изучение биологических функций различных ганглиозидов остается плодотворной основой для будущих исследований.
Фосфолипиды и сфинголипиды разрушаются в лизосомах
В большинстве клеток мембранные липиды непрерывно разрушаются и замещаются новыми. Для каждой гидролизуемой связи в лизосомах содержится специфический гидролитический фермент (рис 10-16). Фосфолипазы типа А удаляют одну из двух жирных кислот, образуя лизофосфолипид (эти эстеразы не разрушают простую эфирную связь в плазмалогенах). Лизофосфолипазы удаляют оставшуюся жирную кислоту.
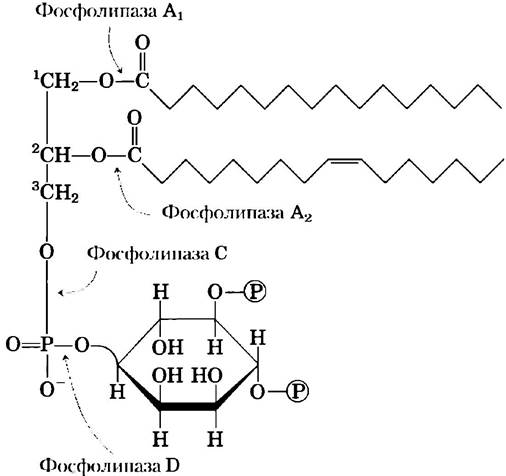
Рис. 10-16. Специфичность фосфолипаз. Фосфолипазы А1 и А2 гидролизуют сложноэфирные связи целых (интактных) глицерофосфолипидов в положениях С-1 и С-2 глицерина. Когда одна из жирных кислот удаляется фосфолипазой типа А, вторая жирная кислота отщепляется от молекулы лизофосфолипазой (не показана). Фосфолипазы С и D расщепляют каждая одну из фосфодиэфирных связей в «головке». Некоторые фосфолипазы действуют только на один тип глицерофосфолипида, как, например, на фос- фатидилинозит-4,5-бисфосфат (изображен на рисунке) или на фосфатидилхолин; другие менее специфичны.
Ганглиозиды разлагаются под действием целого набора лизосомальных ферментов, которые катализируют поэтапное удаление сахарных звеньев и образуют в конце концов церамид. Генетический дефект в любом из этих гидролитических ферментов приводит к накоплению в клетке ганглиозидов, что сопровождается тяжелыми последствиями для здоровья (доп. 10-2).
Стерины имеют четыре конденсированных углеродных кольца
Структурные липиды стерины присутствуют в мембранах большинства клеток эукариот. Характерной структурой в молекулах этой пятой группы мембранных липидов является стероидное ядро, состоящее из четырех конденсированных колец, три из которых содержат шесть атомов углерода, а одно — пять (рис. 10-17). Стероидное ядро почти планарное и относительно жесткое; конденсированные кольца делают невозможным вращение вокруг связей С-С. Холестерин, главный стерин в тканях животных, проявляет амфифильные свойства, поскольку содержит полярную «головку» (гидроксильная группа при С-3) и большую неполярную углеводородную часть (стероидное ядро и боковая углеводородная цепь при С-17), равную по длине примерно 16-углеродной жирной кислоте. Похожие стерины найдены и у других эукариот,
Например, сигмастерин у растений и эргостерин у грибов. Бактерии не могут синтезировать стерины, однако несколько видов бактерий могут включать экзогенные стерины в свои мембраны. Стерины всех эукариот, так же как жирорастворимые витамины, хиноны и долихолы, описанные в разд. 10.3, синтезируются из простых пятиуглеродных изопреновых субъединиц.
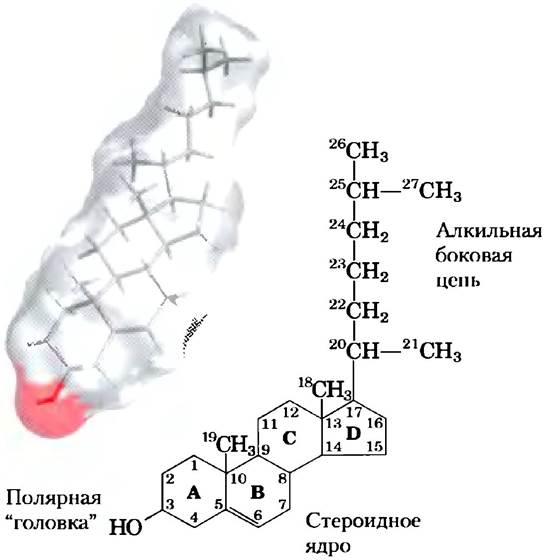
Рис. 10-17. Холестерин. Смоделированная из палочек структура холестерина видна сквозь контур объемной модели молекулы. В химической структуре кольца обозначены буквами А-D, чтобы упростить номенклатуру производных стероидного ядра, а атомы углерода пронумерованы цифрами (голубого цвета). Гидроксильная группа (розовая на обоих изображениях молекулы) при С-3 и есть полярная «головка». Для депонирования и транспорта стерина эта гидроксильная группа конденсируется с жирной кислотой, образуя сложный эфир стерина.
Помимо роли мембранных компонентов, стерины служат предшественниками разнообразных продуктов, обладающих специфической биологической активностью, например, стероидные гормоны — мощные биологические сигнальные молекулы, регулирующие экспрессию генов. Желчные кислоты являются полярными производными холестерина, которые действуют как детергенты в кишечнике, эмульгируя поступающие с пищей жиры с тем, чтобы сделать их более легкодоступными для пищеварительных липаз.
Мы вернемся к холестерину и другим стеринам в последующих главах, чтобы рассмотреть структурную роль холестерина в биологических мембранах (гл. 11), передачу сигналов стероидными гормонами (гл. 12) и поразительный путь биосинтеза холестерина и его транспорт посредством липопротеиновых переносчиков (гл. 21).
Дополнение 10-2. МЕДИЦИНА. Наследственные болезни человека, возникающие в результате аномального накопления мембранных липидов
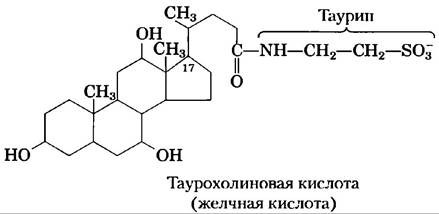
Полярные липиды мембран претерпевают непрерывный метаболический круговорот, скорость их синтеза обычно уравновешивается скоростью распада. Распад (деградация) липидов осуществляется гидролитическими ферментами в лизосомах, причем каждый фермент способен гидролизовать только одну определенную связь. Если деградация сфинголипида нарушается в результате дефекта в одном из этих ферментов (рис. 1), в тканях накапливаются продукты неполного распада, вызывая серьезные заболевания.
Рис. 1. Пути распада GМ1, глобозида и сфингомиелина с образованием церамида. Красными кружочками с крестиком отмечены дефекты фермента, осуществляющего определенную стадию гидролиза, рядом дано название болезни в результате накопления продукта неполного распада.
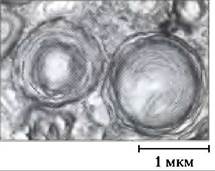
Например, причиной болезни Нимана-Пика является редкий генетический дефект фермента сфингомиелиназы, которая отщепляет от сфингомиелина фосфохолин. Сфингомиелин накапливается в головном мозге, селезенке и печени. Болезнь проявляется в раннем детстве и приводит к замедленному умственному развитию и ранней смерти. Чаще встречается болезнь Тея-Сакса, при которой ганглиозид GМ2 накапливается в мозге и селезенке (рис. 2) из-за недостатка фермента гексозоаминидазы А. Симптомами этой болезни являются прогрессирующее замедление развития, паралич, слепота и смерть в возрасте 3-4 лет.
Рис. 2. Электронная микрофотография части клетки головного мозга ребенка с болезнью Тея-Сакса демонстрирует аномальные отложения ганглиозида в лизосомах.
Генетические консультации могут предсказать и предотвратить многие наследственные болезни. При тестировании будущих родителей удается выявлять аномальные ферменты, затем при анализе ДНК — определить точную природу генетического дефекта; таким образом возможно оценить опасность для потомства. При наступлении беременности таким же образом можно тестировать пробы, взятые из плаценты (ворсинки хориона) или из жидкости, окружающей плод (амниоцентез).
Краткое содержание раздела 10.2 Структурные липиды в мембранах
■ Полярные липиды с полярными «головками» и неполярными «хвостами» — главные компоненты мембран. К наиболее распространенным относятся глицерофосфолипиды, которые содержат жирные кислоты, образующие сложноэфирную связь с двумя гидроксильными группами глицерина, и второй спирт (полярная «головка»), связанный с третьим гидроксилом глицерина фосфодиэфирной связью. Другими полярными липидами являются стерины.
■ Глицерофосфолипиды различаются по структуре их полярной «головки»; наиболее часто встречающимися фосфолипидами являются фосфатидилэтаноламин и фосфатидилхолин. При pH, близком к 7, полярные «головки» глицерофосфолипидов несут электрический заряд.
■ Мембраны хлоропластов чрезвычайно богаты галактолипидами, состоящими из диацил- глицерина, связанного с одним или двумя остатками галактозы, и сульфолипидами — диацилглицеринами с присоединенным сульфонированным остатком сахара, благодаря которому они имеют отрицательно заряженную «головку».
■ Археи содержат уникальные мембранные липиды с длинноцепочечными алкильными группами, связанными простой эфирной связью с глицерином на обоих концах и с остатками сахара и/или фосфата, присоединенными к глицерину, образуя полярную или заряженную «головку». Эти липиды стабильны в жестких условиях, при которых существуют археи.
■ Сфинголипиды содержат не глицерин, а сфингозин — длинноцепочечный алифатический аминоспирт. Помимо фосфорной кислоты и холина, сфингомиелин содержит две длинные углеводородные цепи, одна из них происходит из жирной кислоты, другая из сфингозина. Три других класса сфинголинидов — это цереброзиды, глобозиды и ганглиозиды, которые в своем составе содержат сахара.
■ Стерины несут четыре конденсированных кольца и гидроксильную группу. Холестерин, основной стерин животных, является и структурным компонентом мембран, и предшественником разнообразных стероидов.