Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Вода
Аминокислоты различаются по своим кислотно-основным свойствам
Мы довольно подробно проанализировали кривую титрования аланина, изображенную на рис. 5-10. А как ведут себе другие 19 аминокислот? К счастью, есть возможность сделать некоторые упрощающие обобщения, касающиеся кислотно-основных свойств аминокислот различных классов.
Все аминокислоты, содержащие одну а-аминогруппу, одну карбоксильную группу и одну неионизируемую R-гpyппy, дают кривые титрования, сходные с кривой титрования аланина. Вся эта группа аминокислот (см. табл. 5-3) характеризуется очень близкими, но не одинаковы ми значениями рК’1, лежащими в интервале от 2,0 до 3,0 и рК'2, лежащими в интервале от 9,0 до 10,0, о чем свидетельствуют цифры, приведенные для некоторых из этих аминокислот в табл. 5-4. Таким образом, все аминокислоты этой группы ведут себя подобно аланину и дают кривые титрования такого же типа, как на рис. 5-10.
Таблица 5-4. Величины рК' ионизируемых групп некоторых аминокислот при 25°С
|
Аминокислота |
рK'1 |
pK'2 |
рК’ |
|
—СОС—NH+3 |
R-группы |
||
|
Глицин |
2,34 |
9,6 |
|
|
Аланин |
2,34 |
9,69 |
|
|
Лейцин |
2,36 |
9,60 |
|
|
Серин |
2,21 |
9,15 |
|
|
Треонин |
2,63 |
10,43 |
|
|
Глутамин |
2,17 |
9,13 |
|
|
Аспарагиновая кислота |
2,09 |
9,82 |
3,86 |
|
Глутаминовая кислота |
2,19 |
9,67 |
4,25 |
|
Гистидин |
1,82 |
9,17 |
6,0 |
|
Цистеин |
1,71 |
10,78 |
8,33 |
|
Тирозин |
2,20 |
9,11 |
10,07 |
|
Лизин |
2,18 |
8,95 |
10,53 |
|
Аргинин |
2,17 |
9,04 |
12,48 |
Аминокислоты с ионизируемой R- группой (см. табл. 5-3) имеют более сложные кривые титрования, складывающиеся из трех участков, соответствующих трем возможным стадиям ионизации: следовательно, они имеют три значения рК'. Стадия, соответствующая титрованию ионизируемой R-группы, в какой-то степени сливается с двумя остальными. На рис. 5-12 показаны кривые титрования двух представителей этой группы - глутаминовой кислоты и гистидина. Изоэлектрические точки аминокислот этого класса определяются типом присутствующей в них ионизируемой R-группы. Например, глутаминовая кислота, содержащая две карбоксильные группы и одну аминогруппу, имеет изоэлектрическую точку 3,22 (среднее между двумя величинами рК' для двух карбоксильных групп), т.е. намного ниже, чем у аланина. Аналогичным образом изоэлектрическая точка у лизина, содержащего две аминогруппы, равна 9,74, что гораздо выше, чем у аланина.
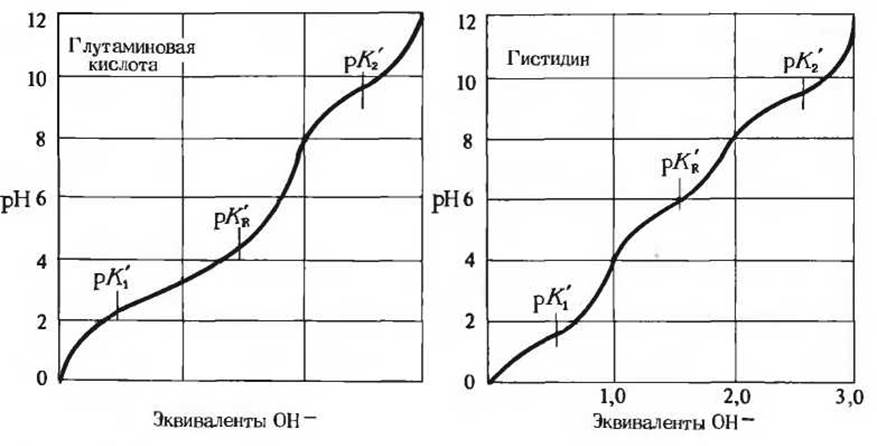
Рис. 5-12. Кривые титрования глутаминовой кислоты и гистидина. Величина рК' R-группы обозначена как pKR'.
Другое важное обобщение, касающееся кислотно-основных свойств 20 стандартных аминокислот, состоит в следующем. Практически только одна аминокислота, гистидин, обладает значительными буферными свойствами при значениях pH, близких к pH межклеточной жидкости и крови. Как можно видеть из табл. 5-4 и рис. 5-12, R-группа гистидина имеет рК' 6,0, что придает ей значительную буферную емкость при pH 7. Все остальные аминокислоты имеют величины рК' слишком далекие от pH 7, чтобы их растворы можно было использовать в качестве эффективных буферов при этом значении pH. Содержащийся в эритроцитах белок гемоглобин, выполняющий функцию переносчика кислорода, характеризуется очень высоким содержанием остатков гистидина. Это придает ему значительную буферную емкость при pH около 7, что весьма важно для той роли, которую играют эритроциты в переносе кровью кислорода и углекислого газа (гл. 25).