Основы биохимии Том 2 - А. Ленинджер 1985
Биоэнергетика и метаболизм
Биосинтез липидов
Путь биосинтеза жирных кислот отличается от пути их окисления
Биосинтез триацилглицеролов у животных представляет собой очень активный метаболический процесс. В значительной степени это обусловлено тем, что животные могут запасать эти соединения в больших количествах. В организме человека (в печени и мышцах) может содержаться лишь несколько сотен граммов гликогена, которых хватает для обеспечения потребности организма в энергии не более чем на 12 часов. На долю же триацилглицеролов в организме мужчины весом 70 кг приходится около 12 кг. Накопленной в них энергии достаточно для поддержания основного обмена человека в течение 8 недель. В тех случаях, когда углеводы потребляются с пищей в избытке и организм уже не способен откладывать их в виде гликогена, они превращаются в триацилглицеролы, которые в больших количествах могут накапливаться в клетках жировой ткани. Больше всего таких клеток находится в подкожной жировой клетчатке и в брюшной полости. Растения также могут запасать энергию в виде высококалорийного топлива - триацилглицеролов; особенно много этих соединений содержится в различных плодах, орехах и семенах.
Полярные липиды мембран, такие, как фосфолипиды и сфинголипиды, в организме животных не запасаются, но они также постоянно синтезируются для восполнения потерь, обусловленных разрушением мембран в ходе метаболических процессов. Например, время полужизни молекул мембранных фосфолипидов в печени крысы составляет менее трех суток.
В этой главе мы сначала рассмотрим биосинтез жирных кислот - основных строительных блоков триацилглицеролов и полярных липидов. Более 90% энергии, запасаемой в триацилглицеролах, приходится на долю жирных кислот. Жирные кислоты придают триацилглицеролам и фосфолипидам характерные для них гидрофобные свойства. Затем мы перейдем к синтезу триацилглицеролов, простейших мембранных фосфолипидов и холестерола - существенного компонента ряда мембран и предшественника таких важных стероидных соединений, как желчные кислоты, половые гормоны и гормоны коры надпочечников.
Прежде всего вспомним, что жирные кислоты в липидах животных тканей имеют в основном четное число атомов углерода. Этот факт уже давно позволил выдвинуть предположение о том, что как окисление, так и синтез жирных кислот осуществляются путем соответственно отщепления и присоединения двухуглеродных фрагментов. После того как выяснилось, что при окислении жирных кислот происходит последовательное окислительное отщепление ацетильных групп в виде ацетил-СоА, естественно было предположить, что биосинтез жирных кислот просто протекает в обратном направлении с использованием тех же ферментативных реакций, что и при их окислении. Однако оказалось, что биосинтез жирных кислот идет иным путем - с участием других ферментов и в других частях клетки. Более того, было установлено, что биосинтез жирных кислот происходит с образованием трехуглеродных промежуточных продуктов и требует также присутствия СО2.
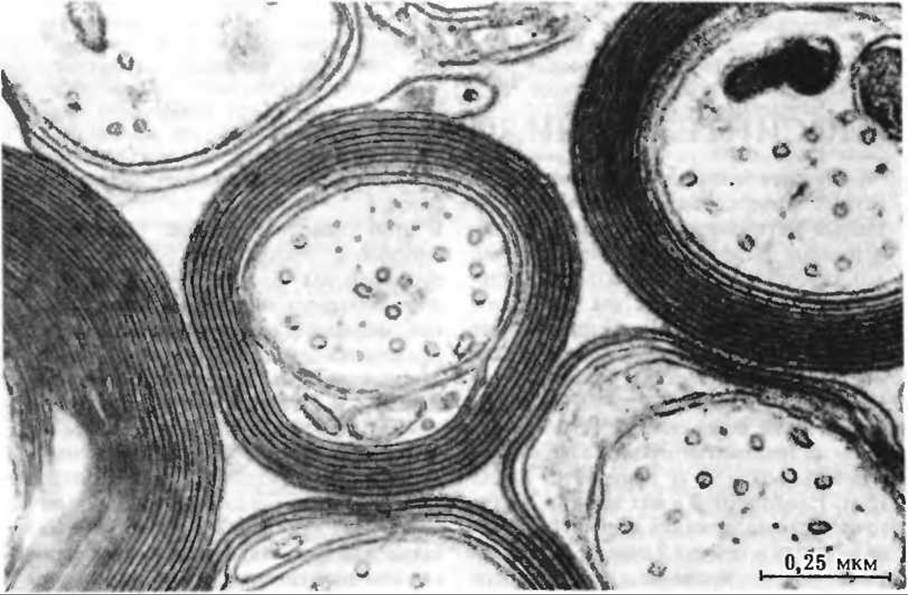
Поперечный срез, на котором видны миелиновые оболочки аксонов нескольких нервных волокон. Миелиновая оболочка, состоящая главным образом из полярных липидов и некоторых белков, образована плазматической мембраной шванновской клетки. В процессе роста шванновская клетка многократно обертывается вокруг аксона (цитоплазма ее при этом оттесняется к периферии). Образовавшаяся таким путем миелиновая оболочка играет в нервных волокнах роль изолятора и обеспечивает более быстрое проведение нервных импульсов.
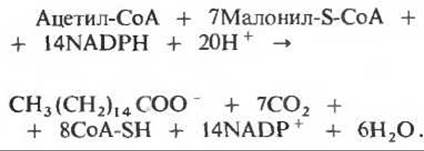
Теперь мы знаем, что синтазная система для жирных кислот катализирует суммарную реакцию, в ходе которой одна молекула ацетил-СоА и семь трехуглеродных молекул малоновой кислоты в виде тиоэфира малонил-СоА (рис. 21-1) последовательно соединяются друг с другом, в результате чего образуется 16-углеродная пальмитиновая кислота и выделяется семь молекул СО2:
Следует отметить, что источником восстановительного потенциала, необходимого для создания углеродного скелета жирной кислоты с одинарными связями, служит NADPH. Первая, причем неожиданная, особенность этой реакции состоит в том, что роль непосредственных предшественников семи из восьми двухуглеродных единиц молекулы пальмитиновой кислоты играют трехуглеродные остатки малоновой кислоты. Единственная молекула ацетил-СоА, необходимая для синтеза жирной кислоты, служит «затравкой». Углеродные атомы метильной и карбоксильной групп этой молекулы занимают соответственно 16-е и 15-е положения в образовавшейся молекуле пальмитиновой кислоты (рис. 21-2). Начиная с ацетильного остатка, рост цепи по направлению к карбоксильному концу продолжается путем последовательного присоединения двухуглеродных фрагментов, каждый из которых образуется из малонил-СоА (рис. 21-2). После ацетил-СоА каждый последующий двухуглеродный фрагмент образуется из двух углеродных атомов малонильной группы, находящихся в непосредственной близости от СоА; одновременно с этим освобождается 3-й углеродный атом неэтерифицированной карбоксильной группы с образованием СО2. Однако в конечном счете все углеродные атомы жирных кислот образуются из ацетил-СоА, поскольку, как мы увидим дальше, сам малонил-СоА образуется из ацетил-СоА и двуокиси углерода.
Вторая важная отличительная особенность механизма биосинтеза жирных кислот состоит в том, что промежуточные продукты в этом процессе представляют собой тиоэфиры не СоА, как это имеет место при окислении жирных кислот, а низкомолекулярного ацилпереносящего белка (АПБ), у которого есть реакционноспособные —SH-группы.
Третья характерная черта биосинтеза жирных кислот заключается в том, что этот процесс протекает в цитозоле эукариотических клеток, тогда как окисление жирных кислот происходит в основном в митохондриях. Синтезированные в цитозоле жирные кислоты, как мы увидим дальше, используются в качестве строительных блоков для синтеза трнацилглицеролов или фосфолипидов.
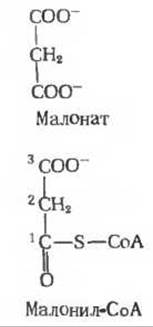
Рис. 21-1. Малонил-СоА-непосредственный предшественник двухуглеродных единиц цепей жирных кислот. Малонил-СоА представляет собой производное малоната - эффективного конкурентного ингибитора сукцинатдегидрогеназы (разд, 9.13). Поэтому может показаться странным, что именно малонил-СоА служит нормальным предшественником в биосинтезе жирных кислот. Однако малонил-СоА как таковой не ингибирует активность сукцинатдегидрогеназы, возможно, из-за того, что у него нет двух свободных карбоксильных групп, ориентированных в пространстве соответствующим образом и обеспечивающих комплементарное взаимодействие сукцината с центром его связывания в молекуле фермента. Кроме того, свободный малонат не является предшественником малонил-СоА; последний, как мы увидим далее, образуется непосредственно из ацетил-СоА путем его карбоксичирования.
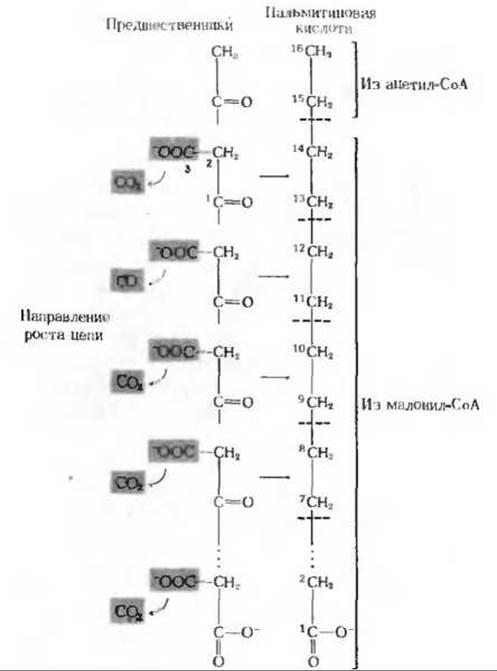
Рис. 21-2. Источник атомов углерода при биосинтезе жирных кислот. В процессе роста цепи 1-й и 2-й углеродные атомы малонильных групп встраиваются в цепь, а 3-й атом выделяется в виде СО2.