Биохимия человека Том 1 - Марри Р. 1993
Биоэнергетика и метаболизм углеводов и липидов
Регуляция метаболизма углеводов
Регуляция уровня глюкозы в крови
Источники глюкозы крови
А. Углеводы, содержащиеся в пищевом рационе.
Большинство углеводов, поступающих в организм с пищей, гидролизуется с образованием глюкозы, галактозы или фруктозы, которые через воротную вену поступают в печень. Галактоза и фруктоза быстро превращаются в печени в глюкозу (см. рис. 21.2 и 21.3).
Б. Различные глюкозообразующие соединения, вступающие на путь глюконеогенеза (рис. 22.2). Эти соединения можно разделить на две группы: (1) соединения, превращающиеся в глюкозу и не являющиеся продуктами ее метаболизма, например аминокислоты и пропионат; (2) соединения, которые являются продуктами частичного метаболизма глюкозы в ряде тканей; они переносятся в печень и почки, где из них ресинтезируется глюкоза. Так, лактат, образующийся в скелетных мышцах и эритроцитах из глюкозы транспортируется в печень и почки, где из него вновь образуется глюкоза, которая затем поступает в кровь и ткани. Этот процесс называется циклом Корн или циклом молочной кислоты (рис. 22.6). Источником глицерола, необходимого для синтеза триацилглицеролов в жировой ткани, является глюкоза крови, поскольку использование свободного глицерола в этой ткани затруднено. Ацилглицеролы жировой ткани подвергаются постоянному гидролизу, в результате которого образуется свободный глицерол, который диффундирует из ткани в кровь. В печени и почках он вступает на путь глюконеогенеза и вновь превращается в глюкозу. Таким образом, постоянно функционирует цикл, в котором глюкоза из печени и почек транспортируется в жировую ткань, а глицерол из этой ткани поступает в печень и почки, где превращается в глюкозу.

Рис. 22.6. Цикл молочной кислоты (цикл Кори) и глюкозо-аланиновый цикл.
Следует отметить, что среди аминокислот, транспортируемых при голодании из мышц в печень, преобладает аланин. Это позволило постулировать существование глюкозоаланинового цикла (рис. 22.6), по которому глюкоза поступает из печени в мышцы, а аланин — из мышц в печень, за счет чего обеспечивается перенос аминоазота из мышц в печень и «свободной энергии» из печени в мышцы. Энергия, необходимая для синтеза глюкозы из пирувата в печени, поступает за счет окисления жирных кислот.
В. Гликоген печени.
Концентрация глюкозы в крови
У человека в период между приемами пищи концентрация глюкозы в крови варьирует от 80 до 100 мг/100 мл. После приема пищи, богатой углеводами, концентрация глюкозы увеличивается до 120—130 мг/100 мл. Во время голодания концентрация глюкозы падает приблизительно до 60—70 мг/100 мл. При нормальном состоянии организма уровень глюкозы в крови колеблется в указанных пределах. У жвачных концентрация глюкозы значительно ниже — около 40 мг/100 мл у овец и 60 мг/100 мл у крупного рогатого скота. Это, по-видимому, связано с тем, что у данных животных практически все углеводы, поступающие с пищей, расщепляются до низших (летучих) жирных кислот, которые заменяют глюкозу в качестве источника энергии в тканях при нормальном питании.
Регуляция концентрации глюкозы в крови
Поддержание содержания глюкозы в крови на определенном уровне является примером одного из самых совершенных механизмов гомеостаза, в функционировании которого участвуют печень, внепеченочные ткани и некоторые гормоны. Глюкоза легко проникает в клетки печени и относительно медленно в клетки внепеченочных тканей. Следовательно, прохождение через клеточную мембрану является лимитирующей скорость стадией при потреблении глюкозы внепеченочными тканями. Поступившая в клетки глюкоза быстро фосфорилируется при действии гексокиназы. С другой стороны, вполне возможно, что более значительное влияние на потребление глюкозы печенью или на выход глюкозы из этого органа оказывают активность некоторых других ферментов и концентрации ключевых промежуточных продуктов. Тем не менее концентрация глюкозы в крови является важным фактором, регулирующим скорость потребления глюкозы как печенью, так и внепеченочными тканями.
Роль глюкокиназы. Следует особо отметить, что глюкозо-6-фосфат ингибирует гексокиназу и, следовательно, потребление глюкозы внепеченочными тканями, зависящее от гексокиназы, которая катализирует фосфорилирование глюкозы и регулируется по принципу обратной связи. С печенью этого не происходит, поскольку глюкозо-6-фосфат не ингибирует глюкокиназу. Этот фермент характеризуется более высоким значением Км (более низким сродством) для глюкозы, чем гексокиназа; активность глюкокиназы повышается в пределах физиологических концентраций глюкозы (рис. 22.7); после приема богатой углеводами пищи фермент «настраивается» на высокие концентрации глюкозы, поступающей в печень по воротной вене. Отметим, что этот фермент отсутствует у жвачных, у которых лишь небольшое количество глюкозы поступает из кишечника в систему воротной вены.
При нормальном содержании глюкозы в крови (80—100 мг/100 мл) печень, по-видимому, поставляет глюкозу в кровь. При увеличении же уровня глюкозы в крови ее выход из печени прекращается, а при достаточно высоких концентрациях начинается поступление глюкозы в печень. Как показали опыты, проведенные на крысах, при концентрации глюкозы в воротной вене печени 150 мг/100 мл скорость поступления глюкозы в печень и скорость ее выхода из печени равны.
Роль инсулина. В состоянии гипергликемии увеличивается поступление глюкозы как в печень, так и в периферические ткани. Центральную роль в регуляции концентрации глюкозы в крови играет гормон инсулин. Он синтезируется в поджелудочной железе В-клетками островков Лангерганса, и его поступление в кровь увеличивается при гипергликемии. Концентрация этого гормона в крови изменяется параллельно концентрации глюкозы; введение его быстро вызывает гипогликемию. К веществам, вызывающим секрецию инсулина, относятся аминокислоты, свободные жирные кислоты, кетоновые тела, глюкагон, секретин и лекарственный препарат толбутамид; адреналин и норадреналин, наоборот, блокируют его секрецию. Инсулин быстро вызывает увеличение поглощения глюкозы жировой тканью и мышцами за счет ускорения транспорта глюкозы через клеточные мембраны путем перемещения переносчиков глюкозы из цитоплазмы в плазматическую мембрану. Однако инсулин не оказывает прямого действия на проникновение глюкозы в клетки печени; это согласуется с данными о том, что скорость метаболизма глюкозы клетками печени не лимитируется скоростью ее прохождения через клеточные мембраны. Инсулин, однако, действует опосредованно, влияя на активность ферментов, участвующих в гликолизе и гликогенолизе (см. выше).
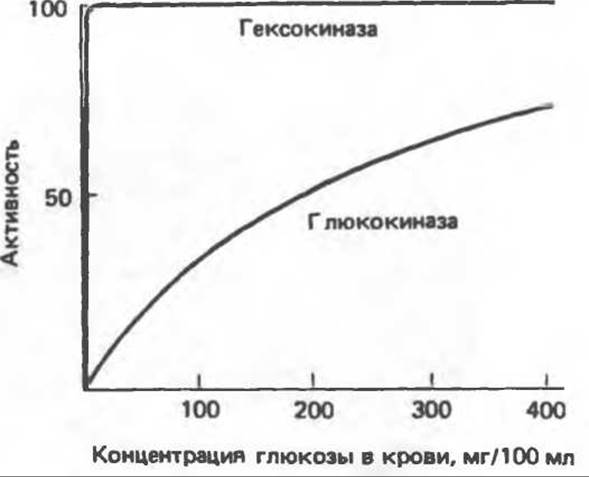
Рис. 22.7. Зависимость глюкозофосфорилирующей активности гексокиназы и глюкокиназы от концетрации глюкозы в крови. Значение Км для глюкозы у гексокиназы — 0,05 ммоль∙л-1 (0,9 мг/100 мл), а у глюкокиназы — 10 ммоль∙л-1 (180 мг/100 мл).
Передняя доля гипофиза секретирует гормоны, действие которых противоположно действию инсулина, т. е. они повышают уровень глюкозы в крови. К ним относятся гормон роста, АКТГ (кортикотропин) и, вероятно, другие «диабетогенные» факторы. Гипогликемия стимулирует секрецию гормона роста. Он вызывает уменьшение поступления глюкозы в некоторые ткани, например в мышцы. Действие гормона роста является до некоторой степени опосредованным, поскольку он стимулирует мобилизацию из жировой ткани свободных жирных кислот, которые являются ингибиторами потребления глюкозы. Длительное введение гормона роста приводит к диабету. Вызывая гипергликемию, он стимулирует постоянную секрецию инсулина, что в конечном счете приводит к истощению В-клеток.
Глюкокортикоиды (11-гидроксистероиды) секретируются корой надпочечников и играют важную роль в углеводном обмене. Введение этих стероидов усиливает глюконеогенез за счет интенсификации катаболизма белков в тканях, увеличения потребления аминокислот печенью, а также повышения активности трансаминаз и других ферментов, участвующих в процессе глюконеогенеза в печени. Кроме того, глюкокортикоиды ингибируют утилизацию глюкозы во внепеченочных тканях. В рассмотренных случаях глюкокортикоиды действуют подобно антагонистам инсулина.
Адреналин секретируется мозговым слоем надпочечников в ответ на стрессорные стимулы (страх, сильное волнение, кровотечение, кислородная недостаточность, гипогликемия и т. д.). Стимулируя фосфорилазу, он вызывает гликогенолиз в печени и мышцах. В мышцах из-за отсутствия глюкозо-6-фосфатазы гликогенолиз доходит до стадии лактата, в то время как в печени основным продуктом превращения гликогена является глюкоза, которая поступает в кровь, где уровень ее повышается.
Глюкагон является гормоном, секретируемым А-клетками островков Лангерганса в поджелудочной железе (его секреция стимулируется гипогликемией). Когда по воротной вене глюкагон поступает в печень, он, подобно адреналину, активирует фосфорилазу и вызывает гликогенолиз. Большая часть эндогенного глюкагона задерживается в печени. В отличие от адреналина глюкагон не влияет на фосфорилазу мышц. Этот гормон усиливает также глюконеогенез из аминокислот и лактата. Гипергликемический эффект глюкагона обусловлен как гликогенолизом, так и глюконеогенезом в печени.
Следует отметить, что гормон щитовидной железы также влияет на содержание глюкозы в крови. Экспериментальные данные свидетельствуют о том, что тироксин обладает диабетогенным действием, а удаление щитовидной железы препятствует развитию диабета. Было отмечено, что гликоген полностью отсутствует в печени животных с тиреотоксикозом. У людей с усиленной функцией щитовидной железы содержание сахара в крови при голодании повышено, а у людей с пониженной функцией щитовидной железы оно снижено. При гипертиреозе глюкоза, по-видимому, расходуется с нормальной или повышенной скоростью, а при гипотиреозе способность утилизировать глюкозу понижена. Следует отметить, что пациенты с гипофункцией щитовидной железы менее чувствительны к действию инсулина, чем здоровые люди и пациенты с гипертиреозом.
Почечный порог для глюкозы, глюкозурия
Когда содержание глюкозы в крови достигает относительно высокого уровня, в процесс регуляции включаются и почки. Глюкоза фильтруется почечными клубочками и обычно полностью возвращается в кровь в результате реабсорбции (обратного всасывания) в почечных канальцах. Процесс реабсорбции глюкозы связан с расходованием АТР в клетках почечных канальцев. Максимальная скорость реабсорбции глюкозы в почечных канальцах около 350 мг∙мин-1. При повышенном содержании глюкозы в крови клубочковый фильтрат содержит больше глюкозы, чем может быть реабсорбировано в канальцах. Избыток глюкозы выводится с мочой, т. е. возникает гликозурия. У здоровых людей гликозурия наблюдается в том случае, если содержание глюкозы в венозной крови превышает 170—180 мг/100 мл; этот уровень называют почечным порогом для глюкозы.
У подопытных животных можно вызвать гликозурию с помощью флоридзина, ингибирующего реабсорбцию глюкозы в почечных канальцах. Такую гликозурию, обусловленную нарушением реабсорбции глюкозы, называют почечной гликозурией. Причиной почечной гликозурии может быть наследственный дефект почек, или же она может развиться в результате ряда заболеваний. Гликозурия часто является указанием на заболевание сахарным диабетом.

Рис. 22.8. Проба на толерантность к глюкозе. Кривые содержания глюкозы в крови у здорового и больного диабетом человека после приема 50 г глюкозы. Обратите внимание на то, что у больного диабетом исходное содержание глюкозы в крови повышено. Показателем нормальной толерантности является возвращение к исходному уровню глюкозы в крови в течение двух часов.
Толерантность к глюкозе
О способности организма использовать глюкозу можно судить по его толерантности к ней. После введения определенного количества глюкозы строят кривые динамики содержания глюкозы в крови (рис. 22.8), которые характеризуют толерантность к глюкозе. При сахарном диабете она понижена из-за уменьшения количества секретируемого инсулина; при этом заболевании содержание глюкозы в крови повышается (гипергликемия), возникает гликозурия, могут происходить изменения в обмене жиров. Толерантность к глюкозе снижается не только при диабете, но и при некоторых состояниях, сопровождающихся нарушением функции печени, при ряде инфекционных заболеваний, ожирении, действии ряда лекарственных препаратов, а иногда и при атеросклерозе. Снижение толерантности к глюкозе может также наблюдаться при гиперфункции гипофиза или коры надпочечников вследствие антагонизма между гормонами, секретируемыми этими железами внутренней секреции, и инсулином.
Инсулин повышает толерантность организма к глюкозе. При его введении содержание глюкозы в крови снижается, а ее потребление и содержание в виде гликогена в печени и мышцах увеличиваются. При введении избытка инсулина может возникнуть тяжелая гипогликемия, сопровождающаяся судорогами; если в этом состоянии быстро не ввести глюкозу, то может наступить летальный исход. У человека гипогликемические судороги появляются при быстром снижении содержания глюкозы в крови до 20 мг/100 мл. Повышенная толерантность к глюкозе наблюдается при недостаточной функции гипофиза или коры надпочечников; это является следствием снижения антагонистического эффекта гормонов, секретируемых этими железами, по отношению к инсулину. В результате «относительное содержание» инсулина в организме увеличивается.
Литература
Cohen Р. Control of Enzyme Activity, 2nd ed. Chapman and Hall, 1983.
Hers H. G. The control of glycogen metabolism in the liver, Annu. Rev. Biochem., 1976, 45, 167.
Hers H. G., Hue L. Gluconeogenesis and related aspects of glycolysis. Annu. Rev. Biochem., 1983, 52, 617.
Hers H. G., Van Schaftingen E. Fructose 2-6-bisphosphate two years after its discovery, Biochem. J., 1982, 206, 1.
Hue L., Van de Werve G. (eds). Short-Term Regulation of Liver Metabolism, Elsevier/North Holland, 1981.
Newsholme E. A., Crabtree B. Flux-generating and regulatory steps in metabolic control, Trends Biochem. Sсi., 1981, 6, 53.
Newsholme E. A., Start C. Regulation in Metabolism. Wiley, 1973.
Storey К. B. A re-evalution of the Pasteur effect, Mol. Physiol., 1985, 8, 439.