Биохимия человека Том 1 - Марри Р. 1993
Структура и функции белков и ферментов
Белки: миоглобин и гемоглобин
Гемопротеины - миоглобин и гемоглобин
На примере миоглобина и гемоглобина очень четко прослеживается связь между структурой и функцией белков вообще и глобулярных белков в особенности. Эти два сложных белка содержат в качестве простетической группы гем — циклический тетрапиррол, присутствием которого объясняется и красный цвет этих белков, и их способность запасать кислород (миоглобин) и обеспечивать его транспорт (гемоглобин). Тетрапирролы состоят из четырех молекул пиррола (рис. 6.1), связанных четырьмя а-метиленовыми мостиками с образованием плоской кольцевой структуры. Что при этом образуется — гем или какое-то родственное соединение — зависит от природы ß-заместителей в пиррольных кольцах. Замещающими группами в геме являются метальная (М), винильная (V) и пропионатная (Рr) группы, расположенные в таком порядке: М, V, М, V, М, Pr, Pr, М (рис. 6.2). В центре плоского кольца находится один атом железа в ферро-состоянии (Fe2+). Тетрапиррольные простетические группы и связанные с ними ионы металлов содержат и другие белки: цитохромы (Fe2+ и Fe3+), некоторые ферменты, например каталаза, триптофанпирролаза, и хлорофиллсодержащие белки (Mg2+). В цитохромах происходит попеременное окисление и восстановление атома железа, играющее определяющую роль в их функционировании (транспорт электронов; см. гл. 12). Напротив, в миоглобине и гемоглобине окисление Fe2+ приводит к потере их биологической активности.
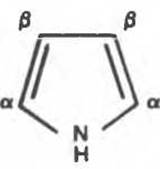
Рис. 6.1. Пиррол. Атомы а-углерода соединены метиленовыми мостиками с образованием тетрапиррола. При атомах ß-углерода находятся заместители, характерные для того или иного тетрапиррола, в частности гема.
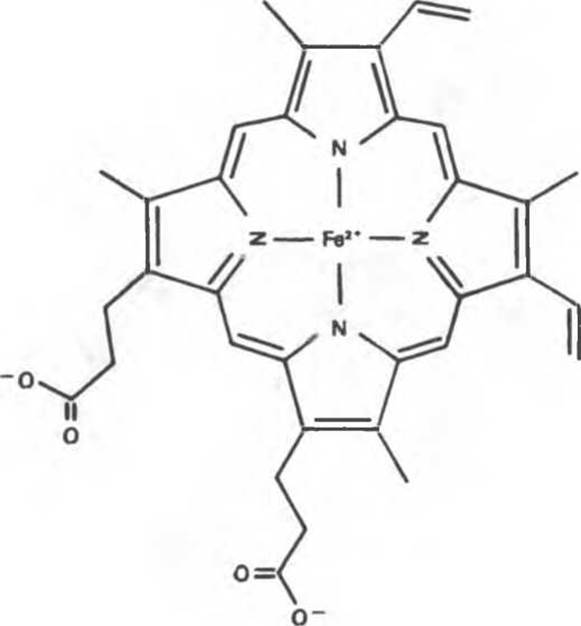
Рис. 6.2. Гем. Пиррольные кольца и атомы углерода, участвующие в образовании метиленовых мостиков, находятся в одной плоскости; почти не выходит из этой плоскости и атом железа (Fe2+). Пятое и шестое координационные положения находятся выше и ниже плоскости гемового кольца на линии, перпендикулярной плоскости. Обратите внимание на природу заместителей при ß-атомах углерода пиррольных колец: полярная часть гема в молекуле миоглобина обращена в сторону ее поверхности (на рисунке — слева внизу).