Биохимия человека Том 2 - Марри Р. 1993
Биохимия внутри- и межклеточных коммуникаций
Гормоны коры надпочечников
Биосинтез стероидных гормонов надпочечников
Предшественники стероидов и основные этапы ферментативных превращений
Стероидные гормоны надпочечников образуются из холестерола, который главным образом поступает из крови, но в небольшом количестве синтезируется in situ из ацетил-СоА через промежуточное образование мевалоната и сквалена. Значительная часть холестерола подвергается в надпочечниках этерификации и накапливается в цитоплазме в липидных капельках. При стимуляции надпочечников посредством АКТГ (или сАМР) происходит активация эстеразы и образующийся свободный холестерол транспортируется в митохондрии, где фермент цитохром Р-450, отщепляющий боковую цепь (Р- 450обп), превращает его в прегненолон. Отщепление боковой цепи включает в себя две реакции гидроксилирования: сначала при С-22, затем при С-20; последующее расщепление боковой связи (удаление 6-углеродного фрагмента изокапроальдегида) приводит к образованию 21-углеродного стероида (рис. 48.2). АКТГ-зависимый белок может связывать и активировать холестерол или Р-450обп. Мощным ингибитором Р-450обп, и биосинтеза стероидов является аминоглутэтимид.
У млекопитающих все стероидные гормоны синтезируются из холестерола через промежуточное образование прегненолона в ходе последовательных реакций, которые протекают в митохондриях либо эндоплазматическом ретикулуме клеток надпочечников. Важную роль в стероидогенезе играют гидроксилазы, катализирующие реакции с участием молекулярного кислорода и NADPH; в определенных этапах процесса участвуют дегидрогеназы, изомераза и лиаза. В отношении стероидогенеза клетки проявляют определенную специфичность. Так, 18-гидроксилаза и 18-гидроксистероид-дегидрогеназа — ферменты, необходимые для синтеза альдостерона, — присутствуют только в клетках клубочковой зоны и потому только они продуцируют этот минералокортикоид. На рис. 48.3 схематически изображены пути синтеза трех основных классов стероидов надпочечников. Названия ферментов заключены в рамочки, превращения на каждом из этапов выделены цветом.
Синтез минералокортикоидов
Синтез альдостерони протекает по специфичному для минералокортикоидов пути и локализован в клубочковой зоне надпочечников. Превращение прегненолона в прогестерон происходит в результате действия двух ферментов гладкого эндоплазматического ретикулума — 3β-гидроксистероид-дегидрогеназы (3β-ОН-СД) и ∆5,4-изомеразы. Далее прогестерон подвергается гидроксилированию по положению С-21 и образуется 11-дезоксикортикос герои (ДОК), являющийся активным минералокортикоидом (задерживает Na+). Следующее гидроксилирование (по С-11) приводит к образованию кортикостерона, обладающего глюкокортикоидной активностью и в малой степени — минералокортикоидной (менее 5% от активности альдостерони). У некоторых видов (например, у грызунов) кортикостероид — самый мощный глюкокортикоидный гормон. Гидроксилирование по С-21 необходимо для проявления как глюко-, так и минералокортикоидной активности, но наличие гидроксильной группы при С-17 ведет в большинстве случаев к тому, что стероид обладает в большей мере глюкокортикоидной активностью и в меньшей степени — минералокортикоидной. В клубочковой зоне фермент гладкого эндоплазматического ретикулума 17а-гидроксилаза отсутствует, но есть митохондриальная 18-гидроксилаза. Под действием этого последнего фермента кортикостерон превращается в 18-гидроксикортикостерон, из которого далее образуется альдостерон — путем окисления спиртовой группы при С-18 в альдегидную. Уникальный набор ферментов в клубочковой зоне и специфический характер ее регуляции (см. ниже) позволили ряду ученых не только рассматривать надпочечники как две эндокринные железы, но и кору надпочечников — как два фактически разных органа.
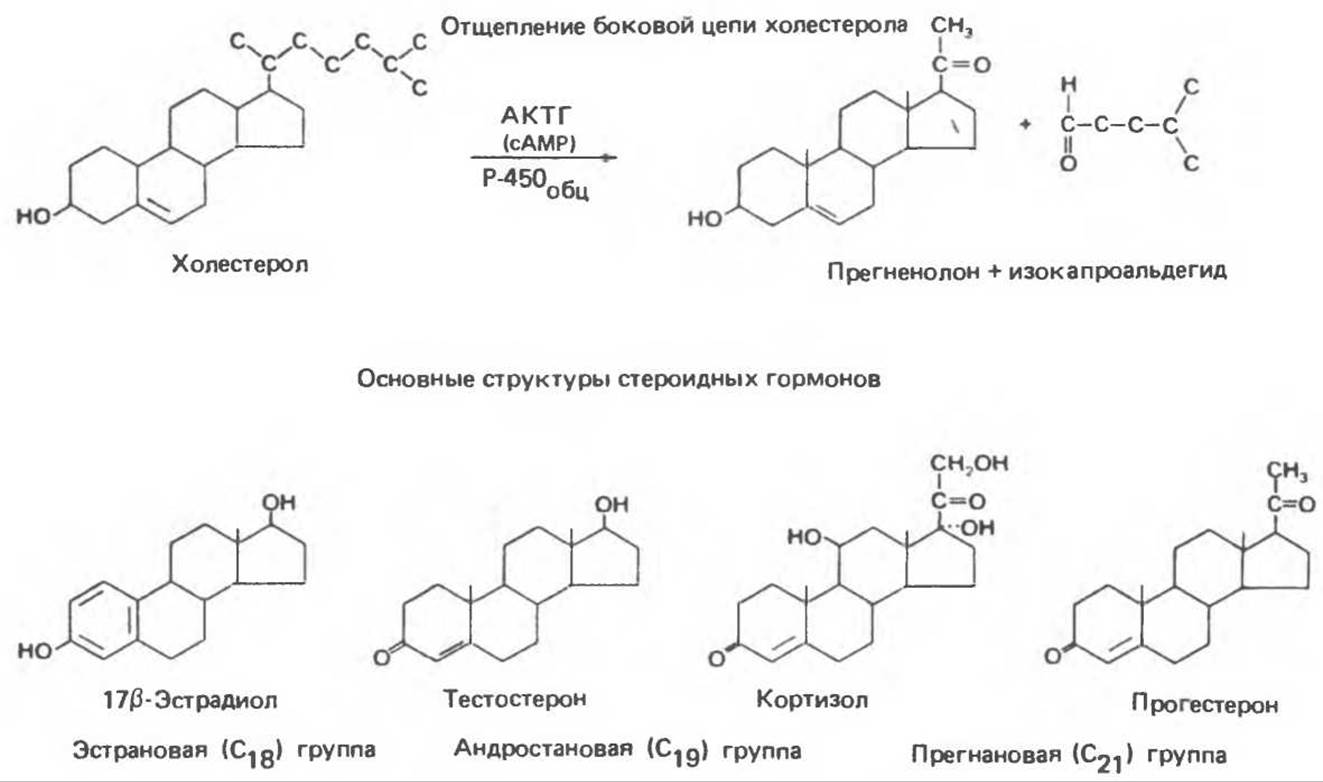
Рис. 48.2. Отщепление боковой цени холестерола и основные структуры стероидных гормонов.
Синтез глюкокортикоидов
Для синтеза кортизола необходимы три гидроксилазы, воздействующие последовательно на положения С-17, С-21 и С-11. Первые две реакции идут очень быстро, тогда как гидроксилирование по С-11 относительно медленно. Если сначала происходит гидроксилирование по С-21, то это создает препятствие для действия 17а-гидроксилазы и синтез стероидов направляется по минералокортикоидному пути (образование альдостерона или кортикостерона в зависимости от типа клеток). 17а-Гидроксилаза — фермент гладкого эндоплазматического ретикулума, воздействующий либо на прогестерон, либо (чаще) на прегненолон. Продукт реакции — 17а-гидроксипрогестерон — далее гидроксилируется по С-21 с образованием 11-дезокси-кортизола. Гидроксилирование последнего по С-11 дает кортизол — самый мощный из природных глюкокортикоидных гормонов человека. 21-Гидроксилаза — фермент гладкого эндоплазматического ретикулума, а 11ß-гидроксилаза — митохондриальный фермент. Из этого следует, что во-время стероидогенеза в клетках клубочковой и пучковой зон происходит челночное движение субстратов: их вход в митохондрии и выход из них (рис. 48.4).
Синтез андрогенов
Основной андроген или, точнее, предшественник андрогенов, вырабатываемый корой надпочечников, — это дегидроэпиандростерон (ДЭА). Большая часть 17-гидроксипрегненолона направляется на синтез глюкокортикоидов, но небольшая его доля подвергается окислению с отщеплением двухуглеродной боковой цепи под действием 17,20-лиазы. Этот фермент выявлен в надпочечниках и гонадах; его субстратом служат только 17а-гидрокси- соединения. Продукция андрогенов заметно возрастает, если нарушается биосинтез глюкокортикоидов из-за недостаточности одной из гидроксилаз (см. ниже, адреногенитальный синдром). Большая часть ДЭА быстро модифицируется путем присоединения сульфата, причем примерно половина ДЭА сульфатируется в надпочечниках, а остальная часть в печени. Сульфатированный ДЭА биологически неактивен, но удаление сульфатной группы восстанавливает активность. ДЭА — это в сущности прогормон, поскольку под действием 3β-ОН-СД и ∆5,4- изомеразы этот слабый андроген превращается в более активный андростендион. В небольшом количестве андростендион образуется в надпочечниках и при воздействии лиазы на 17а-гидроксипрогестерон. Восстановление андростендиона по положению С-17 приводит к образованию тестостерона — самого мощного андрогена надпочечников. Однако по этому механизму в надпочечниках синтезируется лишь малое количество тестостерона, а в основном это превращение протекает в других тканях.
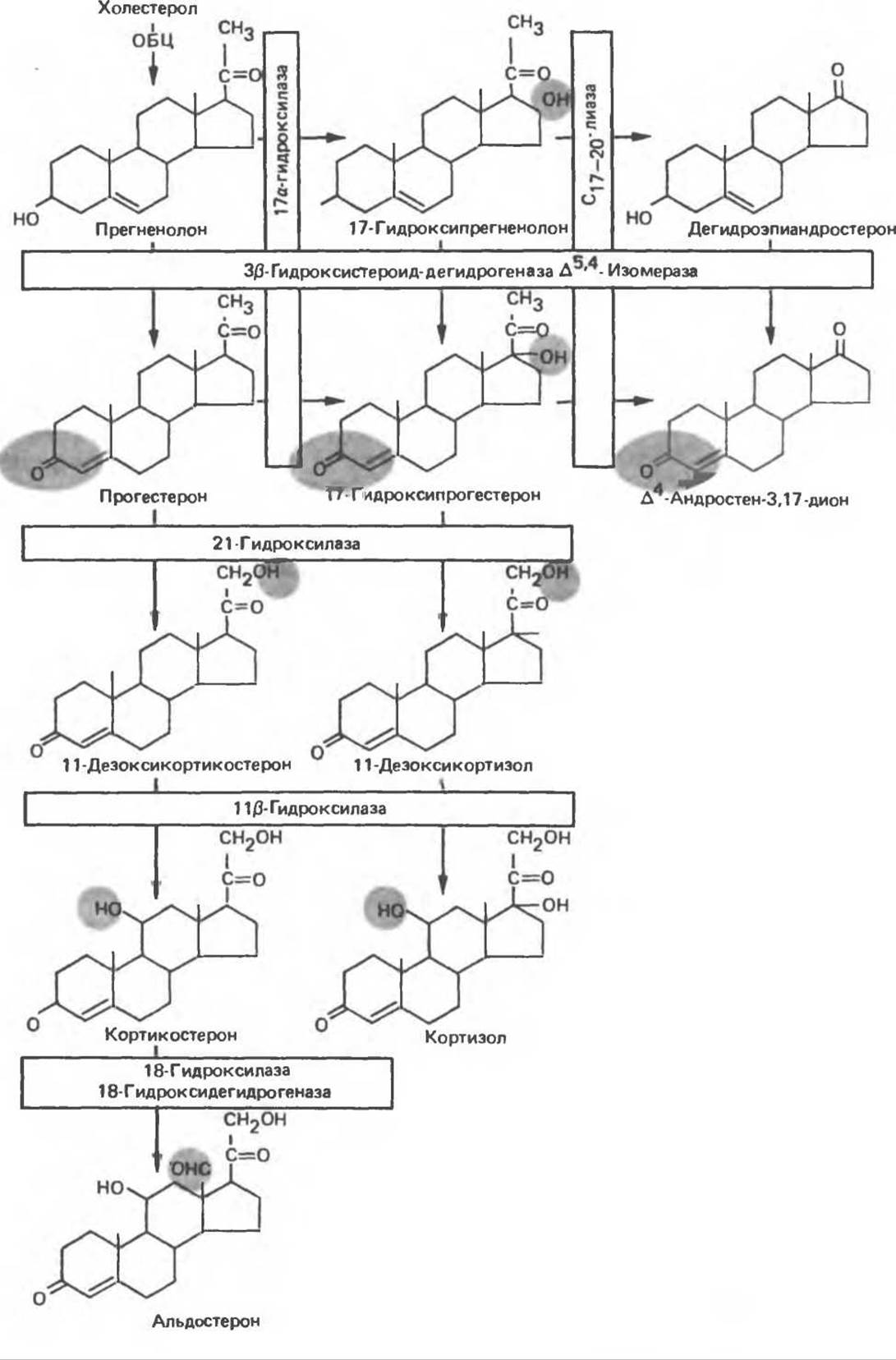
Рис. 48.3. Последовательности реакций, обеспечивающие синтез трех основных классов стероидных гормонов. Участвующие ферменты обведены рамкой; произошедшие на каждом этапе модификации выделены цветом. (Slightly modified and reproduced, with permission from Harding B. W. Page 1135 in Endocrinology v.2, Debroot L. Y. [editor], Grune and Stratton. 1979.)

Рис. 48.4. Внутриклеточная локализация последовательных этапов биосинтеза глюкортикоидов. В ходе стероидогенеза в клетках надпочечников происходит челночное движение предшественников гормонов между митохондриями и эндоплазматическим ретикулумом. Участвующие ферменты: 1) С20-22-лиаза, 2) 3ß-гидроксистероид-дегидрогеназа и ∆5,4-изомераза, 3) 17а-гидроксилаза, 4) 21-гидроксилаза, 5) 11ß-гидроксилаза. (Slightly modified and reproduced, with permission from Hardind B.W. Page 1135 in Endocrinology v.2, Debroot L. Y [editior]. Crune and Stratton, 1979.)
Из венозной крови, оттекающей от надпочечников, можно выделить в небольших количествах и другие стероиды, в том числе 11-дезоксикортикостерон, прогестерон, прегненолон, 17а-гидроксипрогестерон и очень немного эстрадиола, образованного путем ароматизации тестостерона. Продукция этих гормонов надпочечниками столь низка, что не играет существенной роли на фоне продукции других желез.