Биохимия аминокислот - А. Майстер 1961
Промежуточный обмен аминокислот
Триптофан
Биосинтез
Биосинтез триптофана изучали у Escherichia coli, Neurospora crassa и других микроорганизмов. Тот факт, что у некоторых микроорганизмов индол и антраниловая кислота могут замещать триптофан как фактор роста, согласуется с ранее высказанной гипотезой о том, что эти соединения являются предшественниками триптофана [721, 722]. Позднее было обнаружено, что индол и антраниловая кислота накапливаются в культурах некоторых мутантов N. crassa и Е. coli, для роста которых необходим триптофан [118, 723]. Получены другие мутанты, которые могут расти только в присутствии индола, но не антраниловой кислоты. Экспериментальные данные позволяют предполагать, что антраниловая кислота переходит в индол [724, 1127]. Возможно, однако, что антраниловая кислота и индол образуются из общего промежуточного продукта, быть может из соединения «Z1», описанного Дэвисом (стр. 349). Найдено, что карбоксильная группа антраниловой кислоты не участвует в образовании индола и переходит главным образом в углекислоту. Имеются данные, указывающие на то, что атом С-1 бензольного ядра антраниловой кислоты принимает участие в замыкании пирролового кольца при образовании индола [725, 726]:
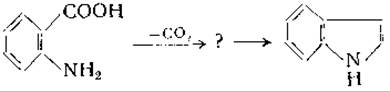
Опубликованы данные, указывающие на возможность образования индол-3-глицерофосфата в результате реакции между антраниловой кислотой и 5-фосфорибозилпирофосфатом. Высказано предположение, что индол-3-глицерофосфат может расщепляться на индол и триозофосфат [1128]1. Антраниловая кислота может образоваться из шикимовой кислоты, а также как продукт распада кинуренина под действием кинурениназы (стр. 401). Имеются данные, согласно которым при определенных условиях предшественником индола может служить фенилаланин [724]. В культурах мутантов, нуждающихся в триптофане, накапливаются различные неидентифицированные соединения, и при изучении роста таких мутантов отмечены явления, еще не поддающиеся объяснению [118]; ввиду этого путь образования антраниловой кислоты нельзя считать полностью установленным.
1 Возможно, что в биосинтезе триптофана свободный индол в нормальных условиях не участвует; по данным Яновского (С. Janofsky et al., Biochim. Biophys. Acta, 28, 640, 1958; Proc. Nat. Acad. Sсi. USA, 44, 1161, 1958), представляется вероятным, что остаток индола переносится к ß-углеродному атому серина от индол-3-глицерофосфата непосредственно или через промежуточный комплекс (индолил-фермент). — Прим. ред.
Много внимания было уделено изучению заключительного этапа биосинтеза триптофана, а именно реакции конденсации индола с серином [727, 729]:
![]()
Фермент, катализирующий эту реакцию, — триптофандесмолаза (триптофансинтетаза) — получен в очищенном виде; найдено, что в его действии участвует пиридоксальфосфат. Возможно, что в этой системе какую-то роль играет цинк [730]. Для изучения механизма синтеза триптофана из индола и серина был применен препарат серина, меченного дейтерием в а- и ß-положениях, С14 в ß-углеродном атоме и N15. Установлено, что в процессе конденсации освобождается половина атомов дейтерия. Эти данные указывают на внутримолекулярную дегидратацию серина, за которой следует присоединение индола к двойной связи образовавшейся а-аминоакриловой кислоты [729]. По-видимому, в ходе реакции возникает шиффово основание, состоящее из аминоакриловой кислоты и пиридоксальфосфата [731].