Биохимия аминокислот - А. Майстер 1961
Промежуточный обмен аминокислот
Триптофан
Другие превращения кинуренина и его производных
В гомогенатах печени мыши 3-оксикинуренин превращается в 4,8-диоксихинолин, вероятно, следующим путем [821]:
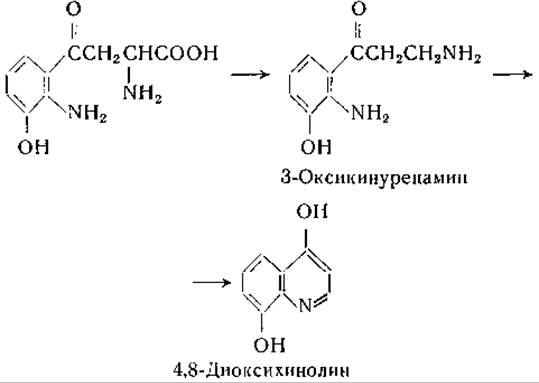
Полагают, что при этом превращении декарбоксилированию подвергается именно 3-оксикинуренин, а не ксантуреновая кислота, поскольку последняя при внесении в исследуемую систему не превращается в диоксихинолин.
Известно, что 3-оксикинуренин является у насекомых предшественником некоторых глазных пигментов [781, 822], представляющих собой комплексы металлов с продуктами конденсации 3-оксикинуренина [805, 823, 824].
Образование кинуреновой кислоты из кинуренина происходит в результате реакции переаминирования (стр. 237), протекающей при участии пиридоксальфосфата. Кинуренинтрансаминазу удалось отделить от кинурениназы, также принадлежащей к пиридоксальфосфат-ферментам. При переаминировании кинуренина, очевидно, образуется о-аминобензоилпировиноградная кислота, которая путем спонтанной циклизации переходит в кинуреновую кислоту. Образование ксантуреновой кислоты из 3-оксикинуренина также происходит в результате реакции переаминирования. Механизм реакции аналогичен превращению кинуренина:
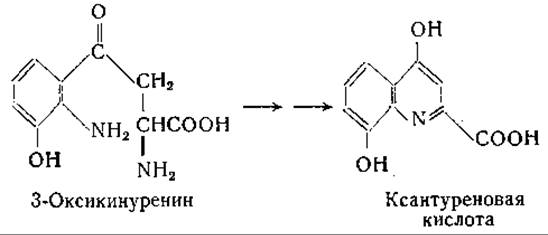
Антраниловая кислота у микроорганизмов может превращаться в индол (стр. 396) или по так называемому «ароматическому пути» окисляться в ß-кетоадипиновую кислоту. Образование ß-кетоадипиновой кислоты из триптофана наблюдали в опытах с экстрактами бактерий. Экспериментальные данные указывают на следующий путь образования ß-кетоадипиновой кислоты [825—835, 839]:
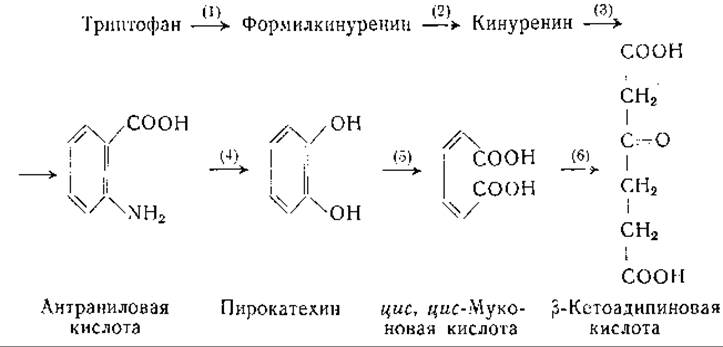
Эти данные были получены в опытах с экстрактами из адаптированных и неадаптированных клеток Pseudomonas. Фермент, катализирующий реакцию (5), — пирокатехаза — был очищен. Оказалось, что для его действия необходимы ионы закисного железа. Продукт, образующийся при действии пирокатехазы, по-видимому, перегруппировывается с присоединением воды в β-кетоадипиновую кислоту; последняя подвергается дальнейшим превращениям с образованием янтарной кислоты и ацетил- кофермента А [1130].