Биохимия - Химические реакции в живой клетке Том 1 - Д. Мецлер 1980
Молекулы, из которых мы состоим
Сахара и полисахариды
Структура и свойства сахаров
Сахара подразделяются на полиоксиальдегиды (альдозы) и полиоксикетоны (кетозы). Карбонильная группа обладает высокой реакционной способностью; типичной реакцией является присоединение групп, содержащих избыточные электроны, в частности —ОН-группы (гл. 7, разд. 3). Если сахарная цепочка достаточно длинна (4—6 атомов углерода), к карбонильной группе может присоединяться одна из гидроксильных групп той же молекулы с образованием циклического полуацеталя — кольцевой формы, находящейся в равновесии со свободной альдегидной или кетонной формой [уравнение (2-10)]. Образованные таким образом шестичленные кольца (пиранозные кольца) особенно устойчивы, но в некоторых углеводах встречаются и пятичленные фуранозные кольца. Естественная тенденция пяти- и шестиуглеродных сахаров (пентоз и гексоз) к циклизации обеспечивает образование устойчивых полимеров из чрезвычайно реакционноспособных неустойчивых мономеров.
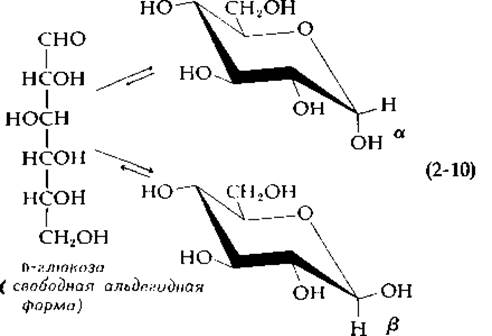
При циклизации сахара возникает новый хиральный центр при атоме углерода (аномерном атоме углерода), ранее входившем в состав карбонильной группы. Две конфигурации относительно этого атома обозначаются как а- и ß-конфигурации [уравнение (2-10)]. Равновесие для большинства сахаров сдвинуто в сторону образования циклических форм. Так, для глюкозы при 25°С в воде в равновесии содержится ∼0,02% свободного альдегида, 38% а-пиранозной формы, 62% ß-пиранозной формы и менее 0,5% каждой из гораздо менее устойчивых фуранозных форм. Хотя полисахариды образованы, как правило, из циклических остатков, промежуточными метаболическими соединениями являются иногда формы с открытой цепью.
Сахара содержат несколько хиральных центров, и различным диастереомерам даны разные названия. Так, глюкоза, манноза и галактоза — это попросту три из восьми возможных диастереомерных альдогексоз (другими являются аллоза, альтроза, гулоза, идоза и талоза) [6]. Каждый из этих сахаров представлен парой форм (энантиомеров) — D и L, являющихся зеркальным отображением одна другой. Для иллюстрации взаимоотношений между сахарами часто пользуются проекционными формулами Фишера (разд. А.4), как это показано на рис. 2-13. Проекционные формулы удобны для сопоставления структур сахаров, но они дают весьма смутное представление о их трехмерной структуре. Согласно указанию Фишера, вертикальные связи при каждом атоме углерода следует представлять уходящими за данный атом. В действительности молекула такую конформацию иметь не может. Сравните, например, трехмерную структуру рибита (разд. А.6), образующегося при восстановлении глюкозы, с его формулой Фишера.

РИС. 2-13. Структурные формулы некоторых сахаров (моносахаридов) согласно правилу Фишера.
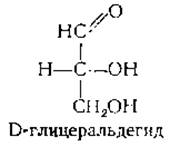
Моносахариды относятся к D- или L-форме в зависимости от конфигурации относительно хирального центра, наиболее удаленного от карбонильной группы (рис. 2-13). Если в молекуле сахара, ориентированной по правилу Фишера, —ОН-группа при этом атоме углерода находится справа, то сахар относят к D-семейству. Простейшим из всех хиральных сахаров является глицеральдегид.
Циклические формы сахаров часто тоже изображают в соответствии с правилом Фишера. Например, a-D-глюкопираноза выглядит так:
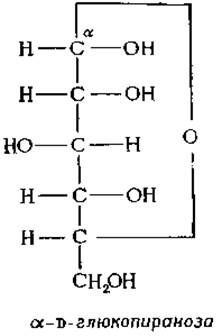
При данном способе изображения гидроксил при аномерном атоме углерода в молекуле a-формы у семейства D-сахаров находится справа, а у семейства L-сахаров — слева. Таким образом, a-D-глюкопираноза и a-L-глюкопираноза являются энантиомерами.
Чтобы упростить изображение конфигурации циклических сахаров, часто применяют структурные формулы Хеуорса:
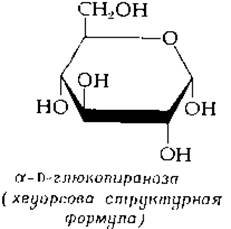
Нижнюю часть кольца (жирные линии) нужно представлять выступающей к наблюдателю, противоположный же край — лежащим за плоскостью рисунка. Структуры Хеуорса довольно просто рисовать, они однозначно указывают конфигурацию, но не отображают взаимного пространственного расположения групп, присоединенных к кольцу. По этой причине часто применяются конформационные формулы, представленные на рис. 2-14.
Большинство сахаров имеет конформацию кресла, при которой большая часть замещающих групп располагается в экваториальной плоскости. Для D-альдоз обычно наблюдается «Сl»-конформация (стр. 108), тогда как для L-альдоз характерна иная форма кресла (форма «1C»), Из этого правила имеются исключения. Так, a-D-идопираноза, по-видимому, принимает 1С-конформацию. Полезно также отметить, что в кольцах для замещающих групп при аномерном атоме углерода предпочтительной оказывается аксиальная ориентация [35].
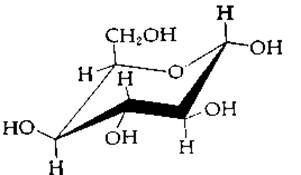
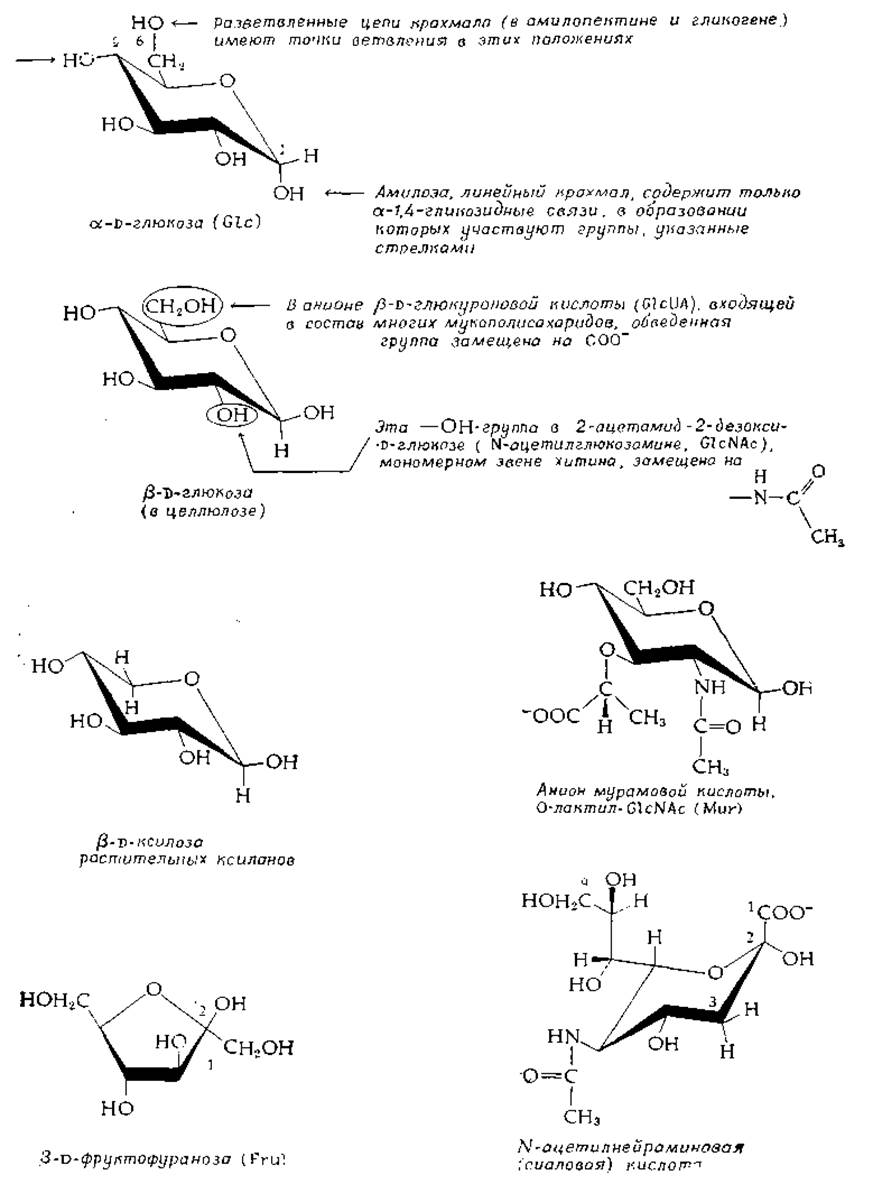
РИС. 2-14. Структура некоторых циклических сахаров, входящих в состав полисахаридов.
Восстановление карбонильной группы сахара (например, боргидридом натрия) приводит к образованию сахарного спирта, например рибита (разд. А.6) или сорбита [он получается при восстановлении глюкозы; уравнение (11-8)]. Альдегидные группы альдоз могут окисляться множеством реагентов, образуя карбоновые кислоты, известные как альдоновые кислоты. Этим объясняется редуцирующий характер альдоз. Например, в щелочной среде альдозы восстанавливают ионы одновалентной меди до закиси меди, ионы серебра — до свободного металла, феррицианид — до ферроцианида. Последняя реакция может послужить основой для создания чувствительного аналитического метода. Даже с учетом того, что альдозы в основном существуют в форме полуацеталей [уравнение (2-10)], их восстановительные свойства совершенно очевидны. В то время как восстановление реагентами, содержащими металл, обычно проходит через образование свободного альдегида, окисление гипобромитом (Вr2 в щелочной среде) приводит к образованию лактона, как это наблюдается, например, в ферментативной реакции, описываемой уравнением (а), табл. 8-4.
Многие производные сахаров встречаются в природе. Среди них можно назвать альдоновые кислоты [например, 6-фосфоглюконовая кислота; уравнение (9-12)], а также уроновые кислоты, содержащие — СООН-группу в концевом положении (в положении 6 глюкуроновой кислоты; рис. 2-14), Группа —ОН во 2-м положении молекулы глюкозы может быть замещена на —NН2-группу с образованием 2-амино-2-дезоксиглюкозы, обычно именуемой глюкозамином (GlcN), или на —NH—СО—СН3-группу с образованием N-ацетилглюкозамина
(GlcNAc). Аналогичные производные есть и для других сахаров. Во многих полисахаридах к сахарным звеньям посредством эфирной связи присоединены сульфатные группы.
Широко распространены два 6-дезоксисахара (лишенные кислорода при атоме С-6) — рамноза и фукоза1. Оба имеют «неестественную» L-конфигурацию, хотя метаболически происходят соответственно от D-глюкозы и D-маннозы.

1 Этот тип соединений называется также 5-метилпеитозами. — Прим. ред.