Биохимия - Химические реакции в живой клетке Том 1 - Д. Мецлер 1980
Молекулы, из которых мы состоим
Сахара и полисахариды
Конформация полисахаридных цепей
Несмотря на все многообразие мономерных звеньев и типов их связывания, конформационные возможности углеводных цепей довольно ограниченны. Сахарное кольцо представляет собой жесткую структурную единицу, и соединение двух колец может быть описано двумя торсионными углами, φ и ψ, подобно тому как это делается для пептидов [48, 49]. Правда, четкие соглашения по поводу того, какой конформации полисахарида должны соответствовать значения φ и ψ, равные 0°, отсутствуют. Вообще говоря, имеется примерное общее правило такого рода для всех полимеров [18], но оно очень неудобно, когда речь идет о полисахаридах. По-видимому, лучше всего считать, что φ и ψ равны 0°, если плоскости, разделяющие сахарные кольца пополам, копланарны:

Эти плоскости проходят через атомы, отмеченные на рисунке звездочками, и в общем случае не перпендикулярны плоскости колец. Систематическое исследование возможных значений φ и ψ для целлюлозы (поли-β-D-глюкозы) показывает, что эти углы ограничены очень узким интервалом значений, при которых расположение мономерных звеньев отвечает почти полностью вытянутой конформации.
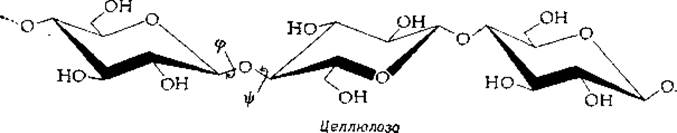
Каждое звено глюкозы оказывается повернутым относительно предыдущего на 180°. Полимер имеет винтовую ось второго порядка, причем плоскости колец идут с небольшим зигзагом [50, 51]. Напомним, что у глюкозы в конформации кресла все ОН-группы лежат в экваториальной плоскости и способны образовывать водородные связи с соседними цепями. Эта особенность вместе с жесткостью конформации, обусловленной ß-конфигурацией мономерных звеньев, несомненно, объясняет способность целлюлозы к формированию прочных волокон.
В крахмале и гликогене цепь тоже образована остатками глюкозы, но на этот раз используется а-1,4-связь. Вытянутая конформация уже невозможна, и цепи скручиваются в спираль. Из спиральных структур, образуемых биополимерами, одной из первых (в 1943 г.) [52] была открыта левая спираль амилозы, идущая вокруг молекул иода (I2) в хорошо известном комплексе иода с крахмалом (рис. 2-17). Число остатков на виток равно 6, шаг спирали — 0,8 нм, диаметр — около 14 нм [53, 54].
Для амилозы была предложена еще одна структура — более сильно закрученная двойная спираль [55]. Предполагается, что в такой спирали каждая цепь содержит 6 остатков на виток и обе цепи идут либо в том же, либо в противоположных направлениях. Молекула амилозы содержит в среднем 1000 остатков глюкозы и может быть вытянута в тонкую цепь 500 нм длиной, что превышает размеры кристаллических областей в гранулах крахмала. Следовательно, цепи в гранулах должны как-то складываться (например, в виде шпилек):

Агароза (мол. вес. — 120 000) представляет собой углеводный полимер с чередующейся последовательностью звеньев.
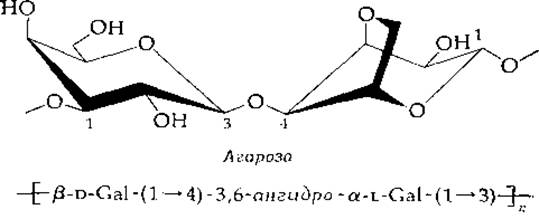
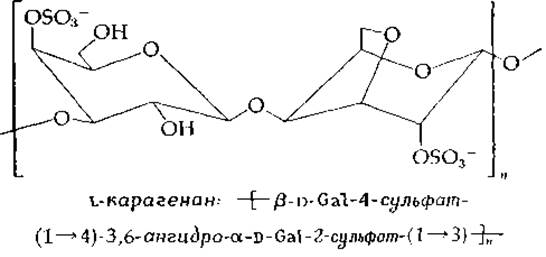
Она является главным компонентом агара и определяет в значительной мере способность этого замечательного вещества образовывать гель. Возможно образование твердого агарового геля, содержащего 99,5% воды. Молекулярная структура агарозы строится на основе левой двойной спирали, имеющей винтовую ось третьего порядка; шаг спирали равен 1,90 нм, ее внутренняя полость заполнена водой [57]. Сходную структуру имеют гельобразующие карагенаны из красных морских водорослей. По рентгеновским данным, в этом случае три дисахаридных звена образуют один виток правой спирали с шагом 2,6 нм. Вторая цепь идет параллельно, но со сдвигом на полоборота, накручиваясь на первую спираль [58]. В местах пересечения двуспиральных областей образуются «узлы», которые представляют собой центры гелеобразования [59] (рис. 2-18). В боковом направлении попарно отходят сульфатные группы, служащие местом связывания ионов кальция, которые стабилизируют гель.
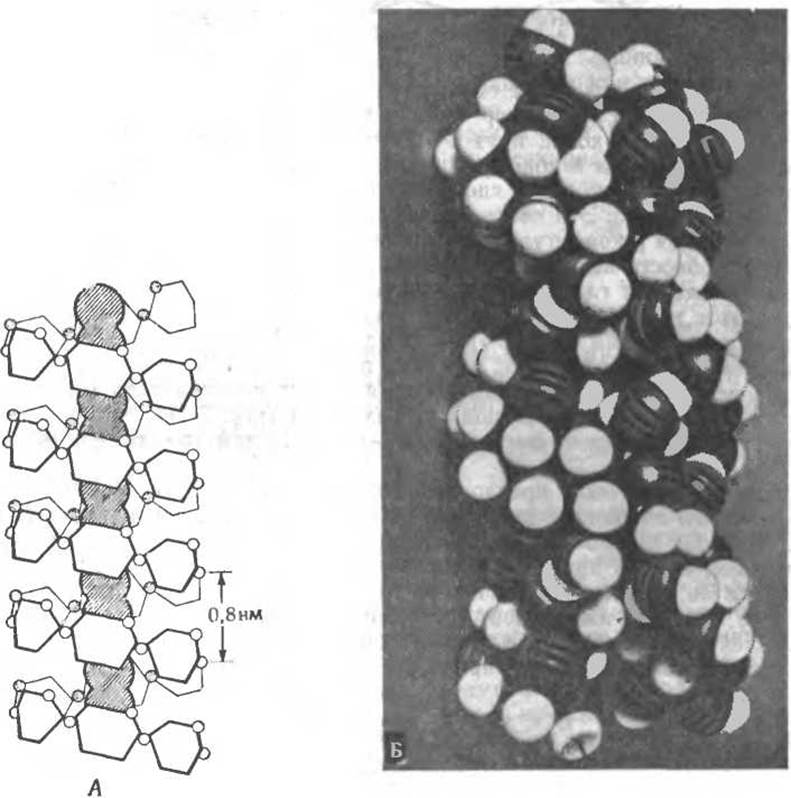
РИС. 2-17. А. Структура спирального комплекса амилозы с иодом (I2). Молекулы иода располагаются вдоль оси спирали, образуемой остатками глюкозы, по шесть остатков на виток. Б. Модель двойной спирали, составленной из двух параллельных цепей. В каждой цепи содержится по 6 остатков глюкозы на виток. Периодичность, согласно модели, равна 2,1 нм (через 6 остатков глюкозы вдоль любой цепи). (С любезного разрешения D. French.)
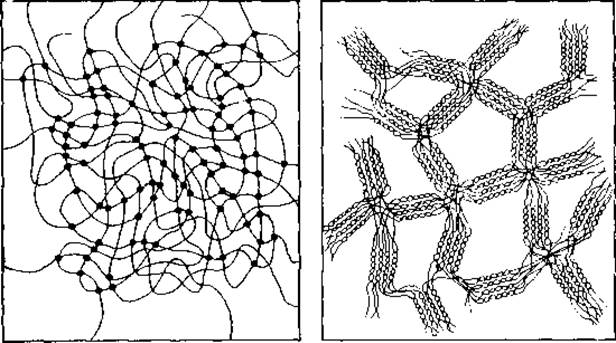
РИС.2-18. Схематическое изображение сетчатой структуры агарозного геля (справа) и показанной для сравнения сетки из беспорядочно свернутых цепей (такая сетка, в частности, характерна для сефадекса). Агарозные гели содержат агрегаты из 10— 104 спиралей; меньшее же число спиралей, как это показано здесь, обычно не наблюдается [58].
Эпизодическое появление в этих полимерах избыточных сульфатных групп порождает изломы цепи (так как модифицированные пиранозные кольца принимают конформацию кресла другого типа). Эти изломы препятствуют образованию полисахаридом единой регулярной спирали [59а].
Ксилан высших растений, ß-1,3-полимер D-ксилозы, по-видимому, представляет собой трехцепочечную правую тройную спираль [60]. Предполагается, что гиалуроновая кислота имеет двуспиральную структуру [61]. Хондроитинсульфаты состоят из одиночных спиралей различного типа [62].
Дополнение 2-Б
Кремний — необходимый микроэлемент
Общеизвестно, что в клетках диатомовых водорослей, скелет которых построен из SiO2, идет активный метаболизм кремния. Накапливать кремний способны радиолярии, некоторые высшие растения и губки; у моллюсков, именуемых блюдечками, он составляет основу зубцовa. Несмотря на все эти факты, метаболизм кремния не очень интересовал исследователей, и лишь недавно было показано, что этот элемент жизненно важен для роста и развития высших животныхб-д, в частности у цыплят кремний обнаружен в местах активного обызвествления формирующихся костейг. Во внутренних органах млекопитающих кремний присутствует лишь в небольших количествах, однако в коже, хрящах и связках его содержание достигает —0,01 %. Шварц3 установил, что кремний входит в состав мукополисахаридов, таких, как хондроитин-4-сульфат, дерматансульфат и гепаринсульфат. Все они содержат ~0,04% кремния, т. е. на 130—280 повторяющихся звеньев полисахаридов приходится один атом этого элемента. У представителей растительного царства содержание кремния в пектинах примерно в пять раз выше. Кремний в полисахаридах очень прочно связан, по-видимому, посредством эфирной связи. Шварц предположил, что ортокремневая кислота Si(ОН)4 реагирует с гидроксильными группами углеводов, в результате чего образуются эфирные связи, которые могут играть роль мостиков между цепями:
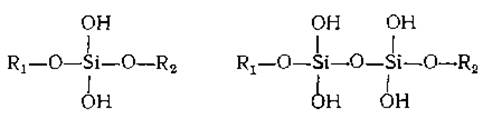
Отметим, что в каждой из этих структур имеются незамещенные ОН-группы при атоме кремния, вследствие чего сразу между несколькими полисахаридными цепями могут образовываться поперечные связи. Исходя из этих результатов, носящих, правда, предварительный характер, можно предположить, что биологическая роль кремния в соединительной ткани состоит в его способности обеспечивать образование поперечных связей (см. также гл. 11, разд. Д.З).
а Schwarz К., PNAS, 70, 1608—1612 (1973).
6 Schwarz К. In: Trace Element Metabolism in Animals (Mills F., ed.), pp. 25—38, Livingstone, Edinburgh, 1970.
в Schwarz К., Milne D. B., Nature (London), 239, 333—334 (1972).
r Carlisle E. M., Science, 178, 619—621 (1972).
д Hoekstra W. H., Suttie J. W., Ganther H. E., Mertz W. eds., Trace Element Metabolism in Animals — 2, Univ. Park Press, Baltimore, Maryland, 1974.