Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Коферменты - особые природные специализированные реагенты
Пиридиннуклеотидные коферменты и дегидрогеназы
Прямой перенос атомов водорода
Хотя было ясно, что при превращении NAD+ в NADH пиридиновое кольцо восстанавливается, положение, в котором присоединяется водород, оставалось неизвестным вплоть до 1944 г., когда впервые в биохимических исследованиях начали использовать изотопные метки. Если NAD+ восстанавливался дитионитом в среде 2Н2O [уравнение (6-65)], в восстановленное пиридиновое кольцо включался атом 2Н, который, как было показано химической деградацией кольца, находился в положении 4, т. е. в пара-положении относительно азота кольца [68] (рис. 8-10). Позднее Вестхаймер с сотрудниками показали, что в ходе ферментативного восстановления NAD+ при взаимодействии с СН3—С2Н2ОН один из атомов 2Н [уравнение (6-65)] переносится на образующийся NADH, что свидетельствует о прямом переносе атома водорода [69]. Кроме того, когда полученный таким образом NAD2H реокисляли ферментативно ацетальдегидом с регенерацией NAD+ и этанола, 2Н полностью удалялся.
Это был один из первых примеров, иллюстрирующих способность фермента делать выбор между двумя идентичными атомами в прохиральном центре (гл. 6, разд. Г, 2). Два атома водорода в 4-м положении NADH были обозначены как НА (ныне называемый пpo-R) и НВ (пpo-S), а две стороны никотинамидного кольца — как А и В. Алкогольдегидрогеназа всегда удаляет водородный атом НА (пpo-R). Малат-, изоцитрат-, лактат- и D-глицератдегидрогеназы избирают этот же атом водорода [70]. Между тем дегидрогеназы, действующие на глюкозо-6-фосфат, глутамат, 6-фосфоглюконат и 3-фосфоглицериновый альдегид, удаляют пpo-S-водород1):
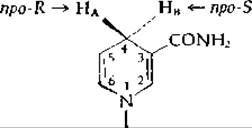
Если атом водорода переносится ферментом из 4-го положения NADH или NADPH на альдегид или кетон с образованием алкоголя, то местонахождение атома водорода в спирте также является стереоспецифическим. Так, алкогольдегидрогеназа при действии на NAD2H превращает ацетальдегид в (R)-моно-[2Н]-этанол [уравнение (6-65)]. Подобным образом пируват восстанавливается лактатдегидрогеназой до L-лактата и т. д.
Было предпринято множество попыток выяснить, является ли лимитирующей стадией для дегидрогеназ перенос гидрид-иона или атома водорода. В одной работе [71] паразамещенные бензальдегиды восстанавливались NADH и NAD2H с использованием в качестве катализатора алкогольдегидрогеназы дрожжей. Это позволило применить уравнение Гаммета [уравнение (3-66)] для анализа кинетических данных. Для ряда бензальдегидов, в котором широко изменялось значение σ+, получено значение р = +2,2 для констант скорости как с NADH, так и с NAD2H. Таким образом, электроно-акцепторные заместители в пара-положении ускоряют реакцию. Хотя значение этого наблюдения не очень ясно [71], относительно низкое значение р, вероятно, несовместимо с механизмом, который требует полного переноса одного электрона от NADH к ацетальдегиду в первой стадии реакции. Первичный изотопный эффект для констант скорости составляет 3,6; это указывает, что связь С—Н в молекуле NADH разрывается на стадии, лимитирующей скорость. Тот факт, что изотопный эффект одинаков для всех замещенных бензальдегидов, свидетельствует в пользу переноса гидрид-иона [71].
1) Более подробные сведения о стереоспецифнчности NAD-зависимых дегидрогеназ читатель может найти в опубликованном недавно обзоре You К., Arnold L. J., Jr., Allison W. S, Kaplan N. О. (1978). Trends Biochem. Sсi., З, 265. — Прим, перев.