Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Коферменты - особые природные специализированные реагенты
Пиридиннуклеотидные коферменты и дегидрогеназы
Некоторые необычные химические свойства пиридиннуклеотидов
Несмотря на кажущуюся простоту структуры NAD+ и NADP+, химические свойства никотинамидного кольца в этих коферментах удивительно разнообразны. Например, NAD+ чрезвычайно неустойчив в щелочных растворах, тогда как HADH неустойчив как раз в слабокислых средах. Эти обстоятельства, а также способность NAD+ вступать в реакции конденсации с другими соединениями приводили иногда к серьезным ошибкам в интерпретации экспериментов. Указанные особенности NAD+ и NADH могут иметь также значение и для проявления их биологических функций.
а. Присоединение к NAD+ и NADP+
Многие нуклеофильные реагенты обратимо присоединяются в пара-положение никотинамидного кольца с образованием аддуктов, структура которых напоминает структуру восстановленных коферментові
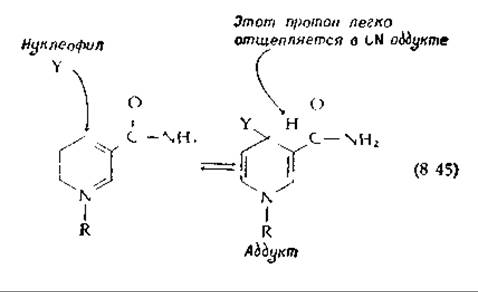
Реакция образования цианидного аддукта, имеющего максимум поглощения при 327 нм, используется для введения дейтерия в пара-положение пиридиннуклеотидов. В этом аддукте протон, прилегающий к сильно поляризованной группе C≡N, легко отщепляется в виде свободного протона. Другие анионы, такие, как —S-, бисульфит и дитионит, также способны присоединяться. Присоединение может происходить и в два орго-положения.
Аддукты с ОН- во 2-м или 4-м положении NAD+ претерпевают раскрытие кольца:
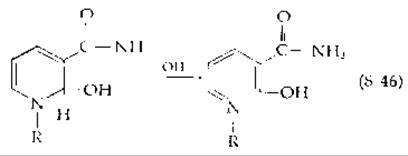
За этими реакциями, катализируемыми основаниями, может следовать дальнейшая деградация [87—89].
Другой катализируемой основанием реакцией является присоединение енолят-анионов, полученных из кетонов, в положение 4 никотинамидного кольца пиридиннуклеотидов:

Аддукты подвергаются циклизации и в присутствии кислорода медленно превращаются во флуоресцирующий продукт. Эти реакции лежат в основе удобного аналитического метода определения NAD+ (с использованием 2-бутанона). Однако эти реакции могут приводить также к образованию ингибитора фермента, очень осложняющего работу: присутствие следов ацетона в коммерческом препарате NADH приводит к искажению результатов экспериментального исследования [90].
Реакции типа (8-47) протекают неферментативным путем только в присутствии сильного основания. В то же время дегидрогеназы часто обеспечивают относительно быстрое и обратимое протекание подобных реакций конденсации. Эти реакции специфичны для тех кетонов, которые возникают в реакциях, катализируемых дегидрогеназами: пируват ингибирует только лактатдегидрогеназу, а-кетоглутарат — глутаматдегидрогеназу и т. д. [91] Мы уже видели (гл. 6, разд А, 9), что ингибирование продуктом является одним из типичных факторов регуляции метаболизма; явления, которые мы здесь обсуждали, могут быть частью таких механизмов регуляции.
б. Модификация NADH в кислоте
Восстановленные пиридиннуклеотиды быстро разрушаются в разбавленной НСl и более медленно при pH 7; эти реакции катализируются кислотами, содержащимися в буферных растворах [92—95]. По- видимому, кольцо восстановленного никотинамида вначале протонируется при атоме С-5, а затем нуклеофил Y-присоединяется в положение 6:

Нуклеофилом может быть ОН-, и в таком случае образующийся аддукт может подвергаться дальнейшим превращениям. Вода может, например, присоединяться также ко второй двойной связи, после чего соединение может подвергаться дециклизации по любую сторону от атома азота. Начальные стадии реакции модификации частично обратимы, однако суммарная реакция необратима. Продукт с неожиданной структурой, возникающий в результате кислотной модификации NADH, был охарактеризован путем определения структуры его кристаллов [96]:

Группой Y на схеме (8-48) является 2'-гидроксил рибозного кольца. Чтобы этот гидроксил мог вступить в реакцию, ß-конфигурация гликозидной связи должна измениться в a-конфигурацию. Читатель может пытаться объяснить, каков возможный механизм катализируемой кислотой эпимеризации при С-1', предшествующей присоединению.
Упомянутые выше реакции привлекли значительный интерес, поскольку глицеральдегид-3-фосфат — дегидрогеназа в побочной реакции превращает NADH в соединение, обозначаемое как NADH-Х, свойства которого сходны со свойствами продукта кислотной модификации. В этом случае реакция NADH-X с АТР и ферментом из дрожжей приводит к регенерированию NADH. Часто обсуждается возможность участия подобных химических превращений в процессе окислительного -фосфорилирования [уравнение (10-14)].
в. Другие реакции пиридиннуклеотидов
Щелочной раствор феррицианида окисляет NAD+ и NADP+ до 2-, 4- и 6-пиридонов. Подобные пиридоны, в особенности 6-пиридон N-метилникотинамида, являются общеизвестными продуктами экскреции никотиновой кислоты у млекопитающих:
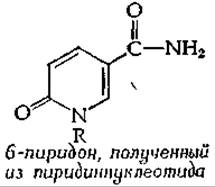
Реокисление NADH и NADPH соответственно в NAD+и NADP+ может быть проведено с помощью феррицианида, хинонов и рибофлавина, но не с помощью Н2O2 или O2. При нагревании в 0,1 н щелочи при 100 °С в течение 5 мин NAD+ гидролизуется до никотииамида и аденозиндифосфатрибозы.