Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
О том, как электроны встречаются с кислородом, как при этом образуется ATR и о некоторых родственных явлениях
Цепь переноса электронов и окислительное фосфорилирование
Термодинамика и «обращенный поток электронов»
Значение ∆G' для окисления кислородом 1 моль NADH (при давлении 1 атм) равно —219 кДж (табл. 3-7). В тканях давление О2 равно ~10-2 атм, и ∆G' составляет ~—213 кДж. Однако, когда эта реакция сопряжена с синтезом трех молекул ATP (∆G' = +34,5 кДж∙моль-1), изменение свободной энергии в суммарной реакции становится равным —110 кДж∙моль-1. Величина по-прежнему остается сильно отрицательной. Однако мы должны помнить, что концентрации ATP, ADP и Pi могут быть далеки от соотношения 1:1:1, которое подразумевается при расчете изменений стандартной свободной энергии. Интересный эксперимент состоит в том, чтобы предоставить окислительному фосфорилированию возможность идти до тех пор, пока митохондрии не достигнут состояния 4, а затем измерить возникающее «соотношение действующих масс» [ATP]/[ADP] ∙ [Рi]. Выражаемая таким образом степень фосфорилирования1) (см. дополнение 3-А) может достигать значений 104 М-1 и более [73, 76]. В результате значение ∆G для окисления NADH в сопряженной цепи переноса электронов оказывается менее отрицательным, чем ∆G0. Действительно, если перенос электронов сопряжен с синтезом трех молекул АТР, то система достигнет равновесия при Rp = 106,4 (25°С); различие между ∆G и ∆G0 составляет 3RTlnRр = 3∙5,708∙6,4=110 кДж∙моль-1.
Едва ли можно настолько повысить Rp, чтобы достичь истинного равновесия между NADH, О2 и адениловой системой; однако на ограниченных участках цепи равновесие возможно. Можно даже заставить поток электронов идти в обратном направлении. Рассмотрим прохождение электронов вдоль цепи, начиная от NADH и обратно к фумарату — окисленной форме пары сукцинат — фумарат. Изменение свободной энергии ∆G' (pH 7) для окисления NADH фумаратом равно —67,7 кДж∙моль-1. В разобщенных митохондриях поток электронов будет всегда идти от NADH к фумарату. Однако в жестко сопряженных митохондриях, в которых на участке 1 вырабатывается АТР, суммарное значение ∆G' становится значительно менее отрицательным. При Rр = 104 М-1∆G' для сопряженного процесса становится примерно равным нулю (—67,7 + 68 кДж∙моль-1). Поток электронов может быть легко обращен так, что сукцинат будет восстанавливать NAD+. Такое обеспечиваемое АТР обращение потока при определенных физиологических условиях может действительно наблюдаться в митохондриях живых клеток. Как мы увидим позднее, у некоторых анаэробных бактерий весь NADH вырабатывается в результате обращения потока электронов.
1) Эту величину также называют фосфатным потенциалом или потенциалом фосфорилирования. Однако некоторые под фосфатным потенциалом понимают свободную энергию образования АТР в данных конкретных условиях, т. е. +34,5 кДж∙моль-1 + RT ln ([ATP]/[ADP]∙[Pi]). Логично потенциал измерять в вольтах, как в уравнении (3∙64). Во избежание путаницы этими терминами лучше не пользоваться.
Другой экспериментальный подход, также основанный на равновесии в цепи переноса электронов, сводится к измерению «наблюдаемого потенциала» переносчика, входящего в состав цепи, в зависимости от концентраций ATP, ADP и Pi. Наблюдаемый потенциал Е рассчитывают, исходя из значения lg([окисл.]/[восстан.]), согласно уравнению (10-12), в котором Е0' представляет собой известный потенциал «средней точки» сопряженной пары (табл. 3-7), а n — число электронов, необходимое для восстановления одной молекулы переносчика:
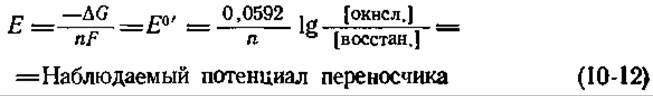
Уравновешивая систему добавлением «окислительно-восстановительного буфера», представляющего собой смесь компонентов пары, легко уравновешиваемой с цепью переносчиков (гл. 3, разд. В,1), можно устанавливать Е на каком-то заранее выбранном уровне [73]. Например, смесь сукцината и фумарата в отношении 1:1 фиксирует Е равным + 0,03 В, тогда как пара ß-оксибутират — ацетоацетат в отношении 1 : 1 зафиксирует Е на значении, равном Е0’ = —0,266 В. Рассмотрим потенциал одного из цитохромов b, который Вильсон с сотрудниками обозначали как bК. Для цитохрома bК Е0’ = 0,030 В. Подставляя это значение в уравнение (10-12) и фиксируя Е = —0,266 В (уравновешивая цепь ß-оксибутиратом и ацетоацетатом), получим, как читатель легко проверит сам, что в равновесии для цитохрома bK отношение [окисл.]/[восстан.] составит около 10-5. Другими словами, в разобщенных митохондриях в отсутствие О2 этот цитохром будет почти целиком находиться в восстановленной форме.
Однако если цепь переноса электронов на участке от ß-оксибутирата до цитохрома bК жестко сопряжена с синтезом одной молекулы АТР, то наблюдаемый потенциал переносчика будет определяться не только приложенным потенциалом Ei уравновешивающей системы, но также и степенью фосфорилирования адениловой системы [уравнение (10-13)]:
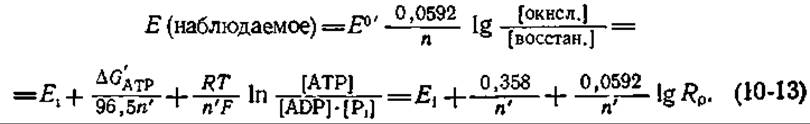
Здесь ∆G'ATP — это потенциал переноса (—∆G' гидролиза) АТР при pH 7 (табл. 3-5), а n' — число электронов, проходящих по цепи, необходимое для синтеза одной молекулы АТР. Заметим, однако, что в верхней части уравнения n — это число электронов, необходимых для восстановления переносчика; для цитохрома bK оно равно единице. Из уравнения (10-13) следует, что при высокой степени фосфорилирования значительная часть цитохрома bK при равновесии по-прежнему остается в восстановленной форме. Так, если Rp = 104, Е0’ цитохрoма bK = 0,030 В, n' = 2 и потенциал Е установлен с помощью оксибутират-ацетоацетатной пары на значении —0,25 В, то по уравнению (10-13) можно рассчитать, что отношение [окисл.]/[восстан.] для цитохрома bK будет равно 1,75. Если теперь варьировать значение Rp, то наблюдаемый потенциал переносчика будет меняться в соответствии с уравнением (10-13). Эти изменения наблюдались экспериментально [73]. При десятикратном изменении Rp наблюдаемый потенциал цитохрома bK изменится на 0,030 В, как и можно было предсказать для n = 2. Наблюдаемый потенциал цитохрома с при каждом десятикратном изменении Rр изменяется на 0,059 В, как можно было легко предсказать, учитывая, что n' = 2 и что перенос электронов до цитохрома с сопряжен с синтезом двух молекул АТР. Тем самым мы имеем дополнительное экспериментальное подтверждение довольно интересного явления. Даже при функционировании одноэлектронных переносчиков, таких, как Цитохромы, для синтеза одной молекулы АТР требуется прохождение по цепи двух электронов. Кроме того, из подобных экспериментов можно заключить, что участки фосфорилирования расположены примерно так, как показано на рис. 10-11.
Таблица 10-6 Электродные потенциалы митохондриальных переносчиков электронов и изменении свободной алергии, связанные с переносом алектроновa
|
Переносчик електронов |
Е0' (pH 7) в изолированном состоянии |
Е0' (pH 7,2) в митохондриях |
∆G (кДж∙моль-1) д ля перевеса 2е— на молекулу O2 при 10-3 атм (переносящей находятся при pH 7) |
|
|
Группа I |
NADH/NAD+ |
—0,320 |
—213 |
|
|
∼ —0,30 в |
Флавопротеид |
—0,30 |
||
|
Fe—S-белок |
∼—0,305 |
|||
|
ß-Оксибутиратацетоацетат |
—0,266 |
—203 |
||
|
Лактат-пируват |
—0,185 |
—187 |
||
|
Сукцинат-фумарат |
0,031 |
—146 |
||
|
Группа II |
Флавопротеид |
∼—0,045 |
||
|
0 в |
Цитохром bК |
—0,030 |
||
|
Cu |
0,001 |
|||
|
Fe—S-белок |
0,030 |
|||
|
Цитохром bK |
0,030 |
|||
|
Убихинон |
0,10 |
0,045 |
—132 |
|
|
Цитохром a3+АТР |
0,155 |
|||
|
Группа III |
Цитохром c1 |
0,215 |
||
|
~0,22 В |
Цитохром с |
0,254 |
0,235 |
—102 |
|
Цитохром bT+АТР |
0,245 |
|||
|
Цитохром а |
0,29 |
0,210 |
||
|
Сu |
0,245 |
|||
|
Fe—S-белок |
0,28 |
|||
|
Группа IV |
Цитохром а3 |
0,385 |
—77 |
|
|
О2 (10-2 атм) |
0,785 |
0,0 |
||
|
О2 (1 атм) |
0,815 |
a По данный Вильсона н др. [72, 73].
Еще один тип экспериментов основан на уравновешивании цепи переноса электронов с внешней окислительно-восстановительной парой, потенциал которой известен, с использованием разобщенных митохондрий. Значение Е0' для данного переносчика можно затем определить по отношению [окисл.]/[восстан.] согласно уравнению (10-12). В то время как изменения в значении уравновешивающего потенциала Е отразятся на отношении [окисл.]/[восстан.], значение Е0' останется постоянным. Для Fe—S-белков и атомов меди (в белках) в цепи переноса электронов значения E0' можно получить, уравновешивая митохондрии, а затем быстро замораживая их в жидком азоте. Отношений [окисл.]/[восстан.] далее рассчитываются из спектров ЭПР, снятых при 77 К. Результаты таких измерений, опубликованные Вильсоном и др. [72—75]|, приведены в табл. 10-6.
По значениям Е0' митохондриальные переносчики разбиваются на четыре изопотенциальные группы с потенциалами ∼—0,30, ~0, ~0,22 и ~0,39 В (табл. 10-6). Когда жестко сопряженные митохондрии переходят в состояние 4 (низкое содержание ADP, высокое содержание АТР, присутствие О2, но низкая скорость дыхания), наблюдаемые потенциалы изменяются. У самой низкой изопотенциальной группы, включающей NAD+/NADH, потенциал снижается до —0,38 В, что соответствует состоянию восстановления переносчиков слева от первого участка фосфорилирования на рис. 10-11. Группы 2 и 3 остаются вблизи их потенциалов средней точки ~—0,05 и +0,26 В. В этих условиях разность потенциалов между последовательными группами переносчиков составляет ~ 0,32 В, чего вполне достаточно для образования одной молекулы АТР на каждую перенесенную пару электронов, при отношении Rр ≈ 104 М-1 [уравнение (10-13)].
Два цитохрома ведут себя особым образом и представлены в табл. 10-6 дважды. Потенциал цитохрома bT в средней точке Е0' меняется от —0,030 В в отсутствие АТР до +0,245 В при высоких концентрациях АТР. С другой стороны, значение Е0’ для цитохрома а3 = +0,385 В снижается в присутствии АТР до 0,155 В. Этот сдвиг потенциала дает основание думать, что с синтезом АТР сопряжено окисление высокоэнергетической восстановленной формы цитохрома a3. В присутствии высоких концентраций АТР образование этого промeжуточного соединения путем восстановления оказывается более трудным (разд. Д, 9,а). Противоположное по направлению изменение Е0' для цитохрома bT свидетельствует о том, что высокоэнергетической в этом случае является окисленная форма [уравнение (10-11)]. Правомерность таких выводов зависит от точности и достоверности, с какой спектроскопические методы позволяют измерять отношение [окисл.]/[восстан.]. На основании этих результатов делали даже вывод о том, что цитохромы bT и а3 непосредственно участвуют в процессе окислительного фосфорилирования [72—75]. Однако с этим далеко не все согласны [77].