Биохимия - Химические реакции в живой клетке Том 3 - Д. Мецлер 1980
Метаболизм азотсодержащих соединений
Метаболизм пиримидинов и пуринов
Биосинтез пуринов
Первые убедительные эксперименты, пролившие свет на процесс биосинтеза пуринов, были проведены на голубях, активно образующие мочевую кислоту. Эксперименты с использованием изотопной метки позволили расшифровать сложную схему происхождения пуринов, показанную на вставке в левом верхнем углу рис. 14-31. Два атома углерода поступают из глицина, один — из СО2 и два — из формиата. Один aтом азота происходит из глицина, два — из глутамина и один — из аспартата. В случае аденина группа 6-NH2 тоже происходит из аспартата.
Весь путь биосинтеза, идущего с участием ферментов, которые удалось выделить и охарактеризовать, представлен на рис. 14-31. Первая «определяющая стадия» в синтезе пуринов — это реакция PRPP с глутамином, приводящая к образованию фосфорибозиламина (стадия а). Здесь мы сталкиваемся еще с одним примером аминирования за счет глутамина. Пирофосфат вытесняется аммиаком, отщепляющимся от глутамина (стр. 97). Аминогруппа образующегося при этом промежуточного соединения присоединяется обычным путем к глицину (стадия б), и полученный продукт формилируется 5,10-метенилтетрагидро фолиевой кислотой. При образовании последней используется свободный формиат согласно схеме, приведенной на вставке рис. 14-31.
1) Не путать с наринтином (гл. 9, разд. А.6).
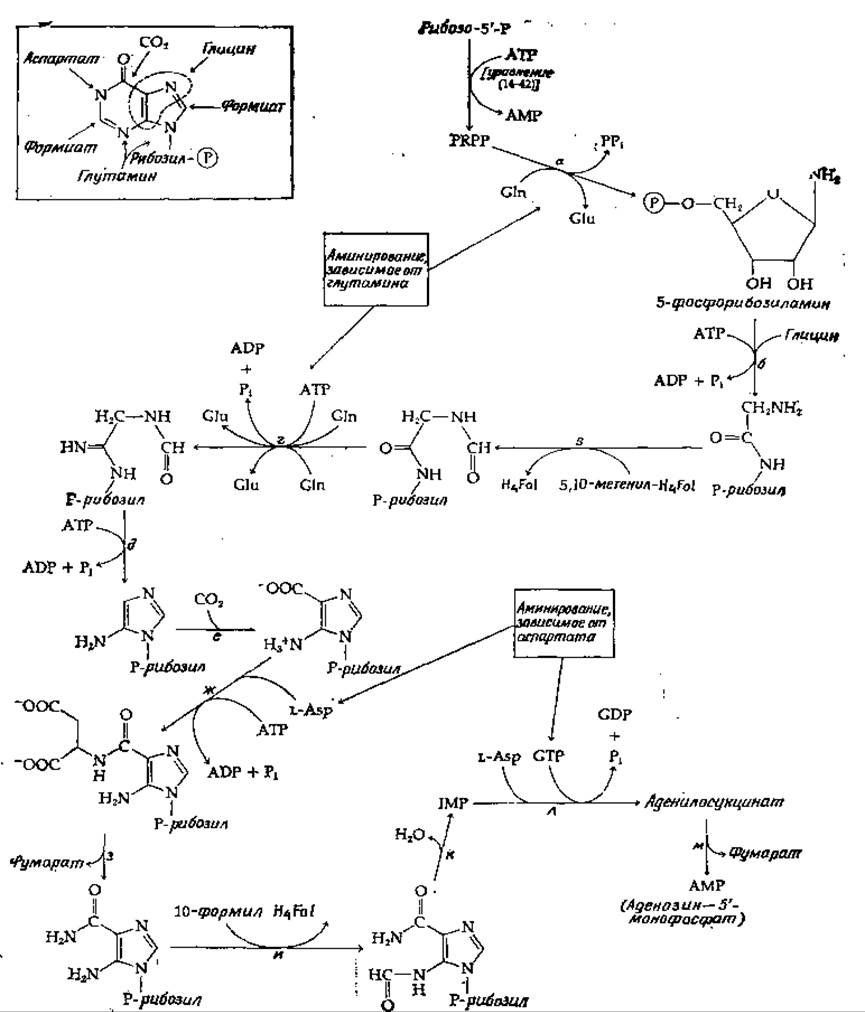
РИС. 14-31. Биосинтез пуриновых нуклеотидов из рибозо-5'-фосфата.
На стадии г (рис. 14-31) осуществляется второе аминирование за счет глутамина — возможно, путем аминолиза промежуточного енолфосфата. Циклизация при участии АТР и таутомеризация (стадия д) завершают образование имидазольного кольца. Затем происходит включение СО2 (стадия е), которое осуществляется в результате несколько необычной реакции карбоксилирования. Далее следует двукратное аминирование (стадии ж и з), в ходе которого происходит перенос азота из аспартата; процесс строго соответствует тому, что наблюдается при синтезе мочевины, сопровождающемся образованием аргининянтарной кислоты в качестве промежуточного продукта (рис. 14-4). Как и при образовании мочевины, углеродный остов молекулы аспартата элиминируется в виде фумарата (стадия з), оставляя азот в составе предшественника пуринов. Последний атом углерода поступает из 10-формилтетрагидрофолиевой кислоты (стадия и). Не совсем ясно, почему в этом случае фермент использует 10-формилтетрагидрофолат, тогда как на стадии в используется близко родственный 5,10-метенилтетрагидрофолат, далее за самопроизвольной циклизацией следует дегидратация, приводящая к образованию инозиновой кислоты (инозин-5'-фосфата, IMP). Этот начальный пуриновый продукт затем превращается в АМР в результате второго двухстадийного аминирования за счет аспартата, проходящего через промежуточное образование аденилосукцината.

РИС. 14-32. Превращение инозин-5'-фосфата в аденин- и гуанинрибонуклеотиды и дезоксирибонуклеотиды.
Стадии, ведущие от IMP к АМР и далее к ADP, АТР и соответствующим дезоксирибонуклеотидам, показаны схематически на рис. 14-32. Кроме того, указано превращение в гуаниловые и дезоксигуаниловые нуклеотиды. IMP в результате NАD+-зависимого окисления превращается в соответствующий ксантиирибонуклеотид, который аминируется, как показано на рисунке, за счет амидной группы глутамина.
Синтез пуринов контролируется сложной системой регуляторных факторов. Некоторые из механизмов, обнаруженных у бактерий, приведены в общих чертах на рис. 6-17. И в этом случае у бактерий все нуклеотиды, образующиеся как конечные продукты, ингибируют начальную реакцию — стадию а на рис. 14-31.