Химия белка. Структура, свойства, методы исследования - Шендрик А.Н. 2022
Методы экспериментального исследования структуры белков
Методы определения молекулярной массы белков
Определение молекулярной массы методом светорассеяния
Если пропустить луч света через белковый раствор в затемненной комнате, то его путь через сосуд становится видимым. Это свойство коллоидных растворов хорошо изучено и известно как опалесценция. Явление опалесценции обусловлено рассеянием света, а сам эффект назван эффектом Тиндаля.
Если известны длина волны падающего света, интенсивность рассеянного излучения, показатели преломления растворителя, а также показатель преломления и концентрация растворенного вещества, то можно рассчитать его молекулярную массу.
Существует два методических подхода. Первый используют, если размер растворенных молекул в 10-20 раз меньше длины волны облучающего света. В этом случае молекула выступает как один рассеивающий излучение центр.
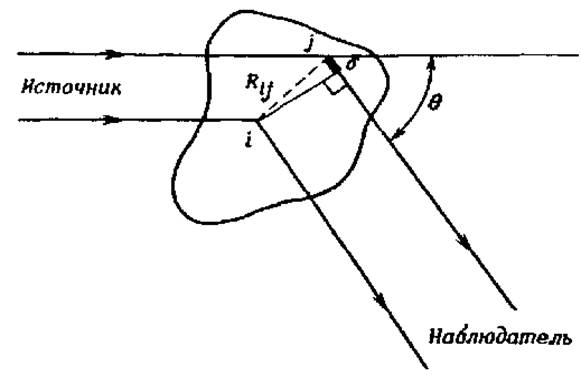
Второй подход применяется когда длина волны излучения сравнима с размером молекул или больше. Тогда, в одной и той же молекуле может быть несколько независимых осцилляторов и необходимо учитывать интерференцию световых лучей рассеянных различными участками одной и той же молекулы (см рис.).
Для первого случая применимо уравнение Релея для зависимости интенсивности рассеянного под углом 0 света от расстояния до рассеивающей частицы:
![]()
где R0 - приведенная интенсивность или число Релея;
I0,I0 - интенсивность падающего и рассеянного света соответственно;
r - расстояние от рассеивающей частицы до приемника света.
Для идеальных разбавленных растворов величина R0 пропорциональна ММ растворенного вещества (М) и его весовой концентрации (с):
R0 = KMc
Коэффициент пропорциональности (К) является функцией, имеющей вид:
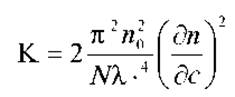
где n0, n - показатель преломления растворителя и раствора соответственно; N - число Авогадро.
Величины Rθ, n0, dn/dc определяют экспериментально и подстановкой в уравнение рассчитывают молекулярную массу белка.
Для неидеальных растворов пользуются эмпирическим соотношением:
![]()
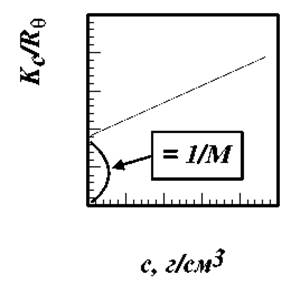
где В - эмпирическая постоянная, и строят зависимость в координатах:
![]()
Отсекаемый на оси ординат отрезок равен обратной величине молекулярной массы (см. уравнение, рисунок).
Если размеры молекул белка соизмеримы с X, то в уравнение вносятся дополнительные поправки:
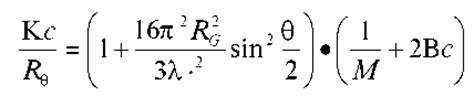
где R2G - так называемый радиус инерции.
Для различных форм белковых молекул (сфера, цилиндр, клубок и т.д.) существуют специальные формулы для расчета величин R2G. Если при подстановке рассчитанного для определенной формы молекулы значения R2Gв уравнение экспериментальные данные укладываются на прямую в координатах:
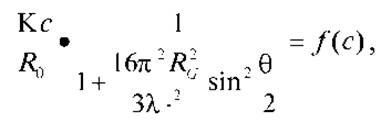
то считают, что форма молекулы, и соответственно R2G, выбраны верно.
Рассеяние света уменьшает интенсивность излучения прошедшего через раствор. Для растворов с размером частиц значительно меньше длинны падающего света выполняется соотношение аналогичное закону Ламберта-Бугера-Бера:
![]()
где т - мутность.
Величину т измеряют с помощью нефелометров.