БИОХИМИЯ - Л. Страйер - 1984
ТОМ 1
ЧАСТЬ I. КОНФОРМАЦИЯ И ДИНАМИКА
ГЛАВА 5. МОЛЕКУЛЯРНЫЕ БОЛЕЗНИ: СЕРПОВИДНОКЛЕТОЧНАЯ АНЕМИЯ
5.2. Дезоксигеннрованный серповидноклеточный гемоглобин имеет пониженную растворимость
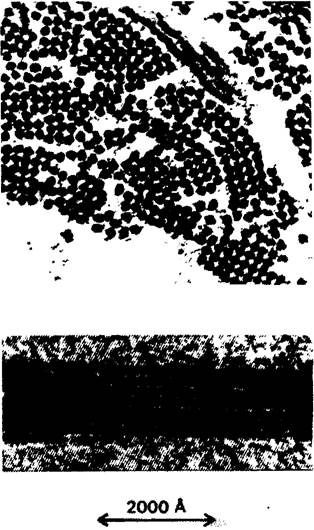
Херрик высказал правильное предположение о локализации первичного дефекта, обусловливающего серповидноклеточную анемию. При снижении концентрации кислорода эритроциты больного приобретают серповидную форму на предметном стекле in vitro. Оказалось, что в этих клетках дефектен сам гемоглобин. Растворимость дезоксигемоглобина серповидных клеток примерно в 25 раз ниже растворимости нормального гемоглобина. При дезоксигенировании концентрированного раствора гемоглобина серповидных клеток образуется волокнистый осадок (рис. 5.3). Именно такой осадок деформирует эритроцит, придавая ему серповидную форму. Гемоглобин серповидных клеток принято обозначать как гемоглобин S (Hb S) в отличие от гемоглобина А (Нb А)-нормального гемоглобина взрослого человека.
Рис. 5.3. Электронная микрофотография волокон дезоксигенированного гемоглобина серповидных клеток. На верхнем рисунке-поперечный срез, на нижнем-продольный срез. Толщина волокон -170 А
5.3. Гемоглобин S отличается от гемоглобина А по электрофоретической подвижности
В 1949 г. Полинг (Pauling) и его сотрудники изучали физико-химические свойства гемоглобина в норме, при носительстве признака серповидноклеточности и при заболевании серповидноклеточной анемией. Использованный ими экспериментальный подход состоял в следующем: они сопоставляли подвижность исследуемых гемоглобинов в электрическом поле. Метод определения подвижности в электрическом поле называется электрофорезом. Скорость миграции (V) белка (или какого-либо другого соединения) в электрическом поле зависит от напряженности электрического поля (E), общего заряда белка (Z) и сопротивления трения (f). Сопротивление трения определяется размером и формой белка. Указанные величины связаны между собой соотношением
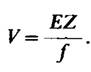 (1)
(1)
Изоэлектрическая точка белка-это значение pH, при котором данный белок не несет электрического заряда. При таком значении pH электрофоретическая подвижность равна нулю, поскольку Z — 0 [уравнение (1)]. При pH ниже изоэлектрической точки молекула белка заряжена положительно; при значениях pH, лежащих выше изоэлектрической точки, белок заряжен отрицательно. Гемоглобин, серповидных клеток отличается от нормального по изоэлектрической точке:

Как видно из приведенной таблицы, различие между серповидноклеточным и нормальным гемоглобином для окисленной и восстановленной форм одинаково.
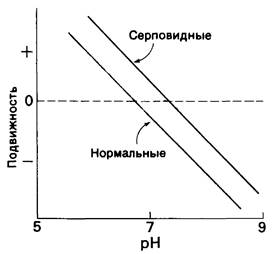
Различие в электрофоретической подвижности гемоглобина А и S может объясняться изменением либо общего заряда Z, либо коэффициента трения / Сам по себе эффект трения (обусловленный изменением формы) выразился бы в том, что одно вещество двигалось бы медленнее другого во всем диапазоне pH. В рассматриваемом случае этого не происходило, судя по тому, что кривые зависимости электрофоретической подвижности от pH имели одинаковый угол наклона (рис. 5.4). Кроме того, другие физико-химические исследования, а именно определение скорости седиментации и свободной диффузии показали, что коэффициенты трения оксигенированных форм гемоглобина А и гемоглобина Sбыли одинаковы.
Рис. 5.4. Зависимость от pH электрофоретической подвижности нормального гемоглобина и гемоглобина серповидных клеток
На основании этих наблюдений был сделан вывод о различии в числе или типе ионизированных групп в сравниваемых гемоглобинах. Сколько таких групп в каждом из гемоглобинов? Ответ дает кривая кислотно-основного титрования гемоглобинов. В области pH 7 эта кривая почти линейна. Изменение pH раствора гемоглобина на единицу создает разницу почти на 13 зарядов. Стало быть, различие в изоэлектрических точках на 0,23 соответствует примерно трем зарядам в молекуле гемоглобина. Отсюда следует, что гемоглобин серповидных клеток отличается от нормального, наличием дополнительных 2-4 положительных зарядов.
С чем связано это отличие: с изменением состава полипептидной цепи или с изменением гема? Из серповидноклеточного гемоглобина был выделен порфирин; по данным определения точки плавления и рентгеноструктурного анализа он оказался идентичен порфирину нормального гемоглобина. Это показывает, что различие между двумя гемо глобинами заключается в особенностях состава полипептидных цепей.
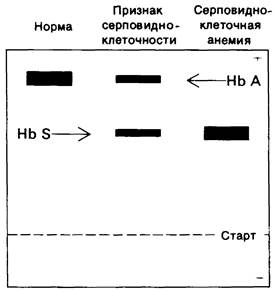
У больных серповидноклеточной анемией (всегда гомозиготных по дефектному гену) имеется гемоглобин 5 и нет гемоглобина А. В то же время у носителей признака серповидноклеточности (которые гетерозиготны по гену серповидноклеточности) оба гемоглобина содержатся примерно в равных количествах (рис. 5.5). Таким образом, в работе Полинга был выявлен бесспорный случай изменения молекулы белка при изменении аллелей кодирующего его гена. Это был первый пример молекулярной болезни.
Рис. 5.5. Электрофорез на крахмальном геле при pH 8,6 гемоглобина здорового человека, гемоглобина носителя признака серпо- видноклеточности и гемоглобина больного серповидноклеточной анемией