БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ III. БИОСИНТЕЗ ПРЕДШЕСТВЕННИКОВ МАКРОМОЛЕКУЛ
ГЛАВА 21. БИОСИНТЕЗ АМИНОКИСЛОТ И ГЕМА
21.3. Аминокислоты синтезируются из промежуточных продуктов цикла трикарбоновых кислот и других важных метаболитов
До сих пор мы рассматривали превращение N2 в NH4+и включение NH4+в состав глутамата и глутамина. Теперь обратимся к биосинтезу других аминокислот. Бактерии, например, E. coli, могут синтезировать все двадцать аминокислот, входящие в основной набор, тогда как в организме человека образуется лишь половина из них. Аминокислоты, которые должны попадать в организм с пищей, называются незаменимыми, а остальные-заменимыми (табл. 21.1). Эти названия отражают потребность организма при определенных условиях. Например, в цикле мочевины синтезируется достаточно аргинина, чтобы удовлетворить потребности организма взрослого, но не растущего ребенка. Недостаточное содержание хотя бы одной аминокислоты приводит к отрицательному азотистому балансу. При этом в организме больше белка разрушается, чем синтезируется, и потому больше азота выводится, чем усваивается.
Таблица 21.1. Двадцать аминокислот основного набора

Пути биосинтеза аминокислот разнообразны. Однако они обладают одним важным общим свойством: углеродный скелет аминокислот происходит из промежуточных продуктов гликолиза, пентозофосфатного пути или цикла трикарбоновых кислот. Кроме того, ситуация упрощается тем, что аминокислоты подразделяются всего лишь на шесть биосинтетических семейств (рис. 21.4).
Рис. 21.4. Биосинтетические семейства аминокислот. Основные метаболические предшественники показаны голубым. Аминокислоты, из которых образуются другие аминокислоты, показаны красным. Незаменимые аминокислоты отмечены звездочками
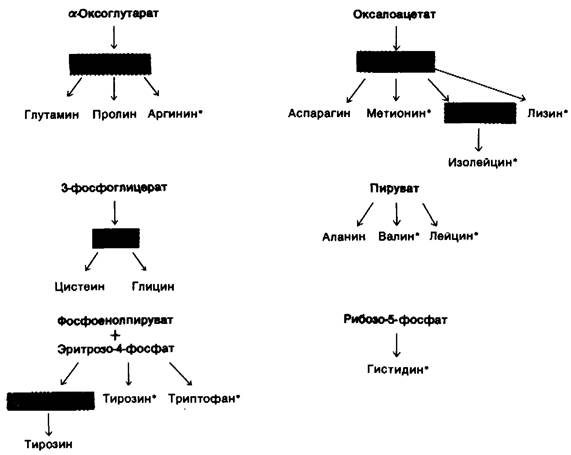
Заменимые аминокислоты синтезируются с помощью весьма простых реакций, тогда как пути биосинтеза незаменимых аминокислот очень сложны. Например, заменимые аминокислоты аланин и аспартат синтезируются в одну стадию из пирувата и оксалоацетата соответственно. Обе аминокислоты получают свою аминогруппу от глутамата в реакции трансаминирования с пиридоксальфосфатом в качестве кофактора (разд. 18.2);
Пируват + Глутамат ⇄ Аланин + α-Оксоглутарат,
Оксалоацетат + Глутамат ⇄ Аспартат + α-Оксоглутарат.
После этого аспарагин может быть синтезирован путем амидирования аспартата:
Аспартат + NH4+ + ATP→ Аспарагин + AMP + PPi + H+.
У млекопитающих донором азота при синтезе аспарагина является глутамин, а не NH4+.
Еще один одностадийный синтез заменимой аминокислоты - гидроксилирование фенилаланина (незаменимой аминокислоты) с образованием тирозина. Данная реакция происходит в организме млекопитающих:
Фенилаланин + O2 + NADPH + Н+ → Тирозин + NADP+ + H2O.
Эта реакция катализируется фенилаланин- гидроксилазой, монооксигеназой, которая рассматривалась выше (разд. 18,16). Следует отметить, что для животных, не имеющих этого фермента, тирозин является незаменимой аминокислотой.
21.4. Глутамат-предшественник глутамина и пролина
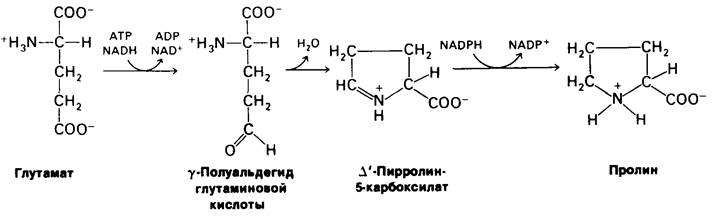
Синтез глутамата путем восстановительного аминирования α-оксоглутарата уже обсуждался (разд. 21.2), равно как и превращение глутамата в глутамин (разд. 21.2). Глутамат-предшественник еще одной заменимой аминокислоты, пролина. Сначала у-карбоксильная группа глутамата реагирует с АТР, образуя ацилфосфат. Этот смешанный ангидрид восстанавливается до альдегида. γ-Полуальдегид глутамата циклизуется с отщеплением Н2O и образует ∆'-пирролин-5-карбоксилат, который восстанавливается NADPH с образованием пролина.
21.5. Серин синтезируется из 3-фосфоглицерата
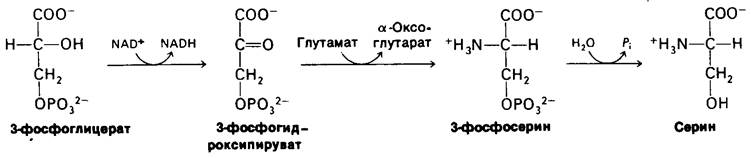
Серин синтезируется из 3-фосфоглицерата, промежуточного продукта гликолиза. Первая стадия - окисление 3-фосфогидроксипи- рувата. Эта α-оксокислота подвергается трансаминированию с образованием 3-фос- фосерина, который затем гидролизуется с образованием серина.
В другом случае гидролиз фосфатной группы может предшествовать окислению и трансаминированию:
3-фосфоглицерат→ Глицерат → Гидроксипируват → Серин
Серин - предшественник глицина и цистеина. При образовании глицина β-углеродный атом боковой цепи серина переносится на тетрагидрофолят, переносчик одноуглеродных фрагментов, который мы рассмотрим ниже:
Серин + Тетрагидрофолят → Глицин + Метилентетрагидрофолят + H2O.
Это превращение катализируется серин-гидроксиметилтрансферазой -ферментом, роль простетической группы которого выполняет пиридоксальфосфат. Связь между α- и β- углеродными атомами серина лабилизуется из-за образования шиффова основания между серином и пиридоксальфосфатом. Затем Р-углеродный атом серина переносится на тетрагидрофолят. Глицин также может образовываться из СO2, NН4+ и метиленте- трагидрофолята в результате реакции, катализируемой глицин-синтазой. Для превращения серина в цистеин должно произойти замещение атома кислорода боковой цепи на атом серы, происходящий из метионина. Соответствующую последовательность реакций мы рассмотрим после обсуждения метаболизма одноуглеродных фрагментов.
21.6. Тетрагидрофолят переносит активированные одноуглеродные фрагменты с различной степенью окисления
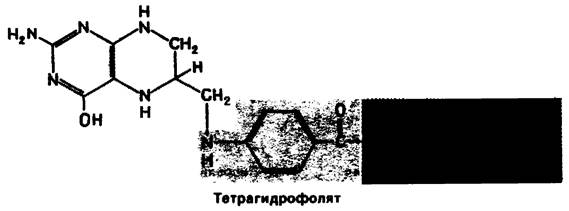
Тетрагидрофолят (его называют также тетрагидроптероилглутамат) - многоцелевой переносчик одноуглеродных фрагментов. Молекула тетрагидрофолята состоит из трех структурных единиц: замещенного птеридина, n-аминобензоата и глутамата. Млекопитающие неспособны синтезировать кольца птеридина. Они получают птеридин с пищей или от микроорганизмов кишечной флоры.
Одноуглеродный фрагмент, переносимый тетрагидрофолятом, связывается с атомом азота N-5 или N-10 (они обозначаются N5и N10) или с обоими. Этот фрагмент может иметь три степени окисления (табл, 21.2). Наиболее восстановленная форма - метильная группа, промежуточная - метиленовая группа. Наиболее окисленные формы - метенильная, формильная или формимино- группа. Одноуглеродный фрагмент с максимально возможной степенью окисления, СО2, переносится не тетрагидрофолятом, а биотином (разд. 15.15).
Эти одноуглеродные фрагменты способны к взаимопревращениям (рис. 21.5). N5, N10-метилентетрагидрофолят может быть восстановлен до N5-метилтетрагидрофолята или окислен до N5 -метенилтетрагидрофолята. N5, N10-метенилтетрагилрофолят может превратиться в N5-формиминотетрагидрофолят и N10-формилтет- рагидрофолят, в которых углерод находится в одной и той же степени окисления. N10-формилтетрагидрофолят может быть также синтезирован из формиата и АТР:
Формиат + АТР + Тетрагидрофолят ⇄ N10-формилтетрагидрофолят + ADP + Pi.

Эти производные тетрагидрофолята служат донорами одноуглеродных фрагментов в самых различных биосинтетических реакциях. Метионин синтезируется из гомоцистеина путем переноса метальной группы N5-метилтетрагидрофолята, как будет описано ниже. Некоторые атомы углерода пуринов происходят из N5, N10-метенильного и N10-формильного производных тетрагидрофолята. Метильная группа тимина (пиримидинового основания) происходит из N5, N10-метилентетрагидрофолята. Это производное тетрагидрофолята служит также донором одноуглеродного фрагмента при синтезе глицина из СO2 и NH4+ в реакции, катализируемой глицин-синтазой:
СO2 + NH4+ + N5, N10-метилентетра- гидрофолят + NADN ⇄ Глицин + Тетрагидрофолят + NAD+.
Итак, в биосинтетических реакциях используются одноуглеродные фрагменты всех трех степеней окисления. Кроме того, тетрагидрофолят служит акцептором одноуглеродных фрагментов в катаболических реакциях. Основной источник одноуглеродных фрагментов-реакция превращения серина в глицин, в результате которой, как уже говорилось, образуется N5, N10-метилентетрагидрофолят. Серин может образовываться из 3-фосфоглицерата (разд. 21.5); таким образом, благодаря этой последовательности реакций клетка имеет возможность образовывать одноуглеродные фрагменты из углеводов de novo. При распаде гистидина образуется N-формиминоглутамат, который переносит свою формиминогруппу на N5-aтом тетрагидрофолята.
Таблица 21.2. Одноуглеродные группы, переносимые тетрагидрофолятом

Рис. 21.5. Превращения одноуглеродных единиц, присоединенных к тетрагидрофоляту

Рис. 21.6. Пространственная модель S- аденозилметионина
