БИОХИМИЯ - Л. Страйер - 1984
ТОМ 3
ЧАСТЬ V. МОЛЕКУЛЯРНАЯ ФИЗИОЛОГИЯ
ГЛАВА 33. ИММУНОГЛОБУЛИНЫ
33.8. Антитела образуются под действием отбора или инструкции?
Специфичность ферментов вырабатывалась на протяжении миллионов лет эволюции. Специфические антитела появляются в крови животного всего лишь через несколько недель после воздействия чужеродной детерминанты. Каким же образом обеспечивается образование специфических антител в столь короткое время?
1. В 1940 г. Лайнус Полинг (Linus Pauling) предложил так называемую инструктивную теорию, согласно которой антиген действует как матрица, определяющая конформацию новообразованной полипептидной цепи антитела. При этом предполагалось, что молекулы антител с данной последовательностью аминокислот обладают потенциальной способностью к образованию антигенсвязывающих участков самой разнообразной специфичности; возникновение же определенной специфичности зависит от природы антигена, присутствующего во время свертывания полипептидной цепи. Согласно инструктивной теории, специфическое антитело не может образоваться в отсутствие соответствующего антигена.
2. Селекционная теория (теория отбора), которую в 50-х годах выдвинули Макферлейн Вернет и Нильс Ерне (Macfarlane Bumet, Niels Jerne), постулирует, что антиген регулирует только количество синтезируемых специфических антител. Согласно этой теории, антигенсвязывающие участки специфических антител полностью детерминированы еще до встречи с антигеном.
33.9. Конец инструктивной теории
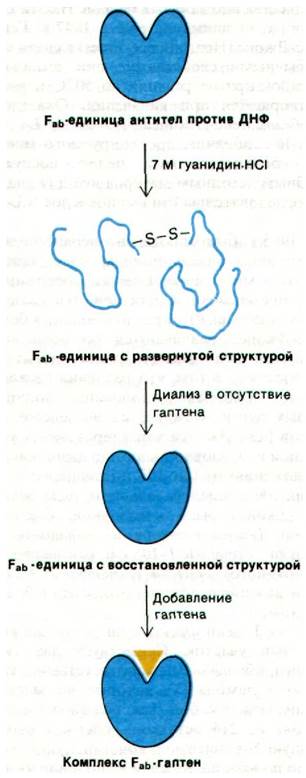
Инструктивная теория предсказывала, что если молекула антитела будет развернута (денатурирована), а затем вновь свернется (ренатурируется), то ее специфичность будет утрачена. Этому предсказанию противоречили экспериментальные данные по ренату- рации рибонуклеазы, полученные в лаборатории Христиана Анфинсена (Christian Anfinsen). Вспомним, что денатурированная рибонуклеаза спонтанно восстанавливает исходную трехмерную структуру, специфичность и каталитическую активность после удаления денатурирующего агента (разд. 2.12). Для ренатурации присутствие субстрата не требуется. Этот принципиально важный факт относительно рибону-клеазы послужил стимулом для постановки аналогичных опытов с антителами (рис. 33.11). Были взяты Fab-фрагменты антител против ДНФ; использование фрагментов относительно небольшого размера, а не целых антител значительно упрощает эксперимент. Fab-фрагмент обрабатывали высокоэффективным денатурирующим агентом - 7М солянокислым гуанидином. Денатурированный таким образом Fab-фрагмент терял сродство к гаптену (ДНФ). Данные гидродинамического и оптического анализа свидетельствовали о том, что конформация денатурированного Fabбыла близка к случайному клубку. Далее гуанидин-HCl удаляли путем диализа; при этом денатурированный Fab восстанавливал исходную пространственную структуру в отсутствие гаптена ДНФ. Самым поразительным было то, что ренатурированный Fab обладал высоким сродством к динитрофенольным гаптенам. Поскольку ренатура- ция происходила в отсутствие гаптена, не оставалось сомнений, что специфичность участка связывания антигена определяется только последовательностью аминокислот белка-антитела. Результат этого эксперимента свидетельствовал в пользу отбора и противоречил основному предсказанию инструктивной теории. Более того, было обнаружено, что клетки, продуцирующие антитела, способны синтезировать их в большом количестве в отсутствие антигена. Это окончательно подтвердило основной тезис селекционной теории: антиген влияет на количество продуцируемых специфических антител, но не на их аминокислотную последовательность или трехмерную структуру.
Рис. 33.11. Fab-Фрагмент анти-ДНФ-антител восстанавливает способность к связыванию ДНФ после денатурации (развертывания структуры) и последующей ренатурации (восстановления исходной структуры) в отсутствие антигена. Этот опыт показывает, что специфичность определяется природой последовательности аминокислот
33.10. Иммуноглобулины миеломы и гибридомы гомогенны
Как же могут синтезироваться специфические антитела до появления антигенов? Гетерогенность антител и трудности анализа смеси их молекул на протяжении многих лет служили препятствием к изучению этой проблемы. Выйти из этого положения удалось путем использования такого объекта исследования, как множественная миелома - злокачественное перерождение клеток, продуцирующих антитела. При этом виде рака происходит перерождение одного лимфоцита или плазматической клетки, что ведет к неконтролируемому клеточному делению. Следовательно, в этом случае образуется большое число клеток одного типа. Они составляют клон, т.е. происходят от одной клетки и имеют одни и те же свойства. Такие опухоли секретируют большие количества какого-то одного иммуноглобулина. Иммуноглобулины миеломы обладают нормальной структурой и во всех отношениях соответствуют норме, но каждый из них представляет собой гомогенный образец одного из многочисленных антител, присутствующих в данном организме. Миеломы развиваются у мышей. Эти опухоли можно трансплантировать другим мышам; после пересадки от одной мыши другой опухоль пролиферирует. Более того, в таких продуцирующих антитела опухолях из поколения в поколение синтезируется одно и то же антитело. Именно это обстоятельство привело к тому, что основные достижения молекулярной иммунологии связаны с изучением гомогенных миеломных иммуноглобулинов.
Сезар Милстайн и Джордж Кёлер (Cesar Milstein, Georges Kohler) обнаружили, что можно получить в большом количестве антитела практически любой заданной специфичности посредством слияния клетки, продуцирующей антитело, с клеткой миеломы. Для этого мышь иммунизируют определенным антигеном и спустя несколько недель удаляют у нее селезенку. Далее берут смесь иммунокомпетентных клеток этой селезенки и in vitro вызывают их слияние с клетками миеломы. Затем выделяют гибридные клетки путем культивирования смеси всех клеток в среде, поддерживающей рост только гибридных (но не исходных) клеток. В некоторых из полученных гибридных клеток сохраняются неопластические свойства миеломных клеток, и при этом они синтезируют антитела заданной специфичности. Такие клетки гибридомы как в первом, так и во всех последующих поколениях устойчиво продуцируют большие количества гомогенных антител со специфичностью, детерминированной исходной клеткой селезенки. К настоящему времени таким путем получено много различных моноклональных антител, которые используются в аналитических целях как высокоспецифические реагенты. Например, моноклональные антитела против определенного лекарственного средства или гормона позволяют определить его содержание в жидкостях тела даже при крайне низкой концентрации.
Рис. 33.12. Легкая цепь иммуноглобулина состоит из вариабельной и константной областей
